第2节 研究物质性质的方法和程序 知识点题库
①生成白色沉淀 ②生成红褐色沉淀 ③有气泡产生④因为Na2O2具有漂白性,所以FeCl3溶液褪色.
-
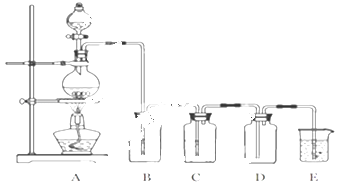
(1) 若利用如图装置制备纯净、干燥的氯气,装置A中反应的化学方程式为;装置C中试剂的作用是.
-
(2) 若利用如图装置实现碳和浓硫酸的反应,并进行如下验证:
①装置B、C、D、E中分别装有品红溶液、酸性KMnO4溶液、品红溶液、澄清石灰水,则D装置中品红溶液的作用是,证明气体中有CO2的现象是.
②若证明SO2具有氧化性,同时证明碳酸的酸性比硅酸的强,B、C、D中分别装有Na2S溶液、足量酸性KMnO4溶液、品红溶液.
则:B中的现象,E中应加入溶液.
-
(1) 工业上,将苏打和硫化钠以1:2的物质的量之比配成溶液,再通入SO2气体,可制得Na2S2O3 , 同时放出CO2。写出该反应的化学方程式。硫化钠溶液在空气中久置,会生成淡黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的化学式。
-
(2) Na2S2O3标准液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高,用离子方程式表示其原因。
-
(3) 工业上用大苏打溶液吸收工业废气中的氯气,其氧化产物为SO42- , 写出离子方程式。
-
(4) 工业上常用苏打和盐酸除去锅炉中水垢中的硫酸钙。先用饱和苏打溶液浸泡锅垢,然后用盐酸清洗。“浸泡”的目的是。(并用离子方程式表示)
-
(5) 在密闭的容器中投入一定量的Na2O2和NaHCO3固体,在300℃下充分反应。若残留固体为纯净物,则起始时n(NaHCO3):n(Na2O2)满足的条件是。
-
(1) 切下的钠块表面变暗,其反应的化学方程式为。
-
(2) 将其中一块钠放入坩埚中加热,反应现象为:,反应的化学方程式是。
-
(3) 过氧化钠是钠的一种重要化合物,其中一种用途是用于呼吸面具或潜水艇中氧气的来源,涉及的主要反应的化学方程式为。若15.6gNa2O2参加反应,则最多可制得标准状况下氧气的体积为L。
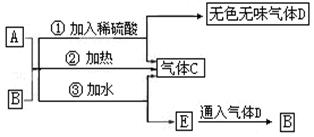
根据以上关系,回答下列问题:
-
(1) A的电子式为.
-
(2) A投入FeCl2溶液中的反应为(请用一个化学方程式表示)
-
(3) 若A、B按物质的量之比1:1.5混合在密闭容器中加热充分反应后,排出气体,则剩余的固体为(写化学式)
-
(4) 氢能被视为21世纪最具发展潜力的清洁能源,试回答下列问题:
①与化石燃料相比,氢气作为燃料的优点是(答两点)。
②施莱辛(Sehlesinger)等人提出可用NaBH4与水反应制氢气,写出NaBH4与水反应的化学方程式。
①钠与水反应生成NaOH和H2;高温下铁与水反应也生成碱和H2
②氢氧化铝加热分解为金属氧化物和水;氢氧化镁、氢氧化铁也能加热分解生成相应的金属氧化物和水
③碳酸钠、碳酸氢钠溶液均显碱性;钠盐溶液均能使酚酞变红
④铝和硫反应生成Al2S3;铁与硫反应生成Fe2S3
-
(1) I.化学兴趣小组的同学为测定Na2CO3和NaCl混合物中Na2CO3的质量分数,进行了如图实验。
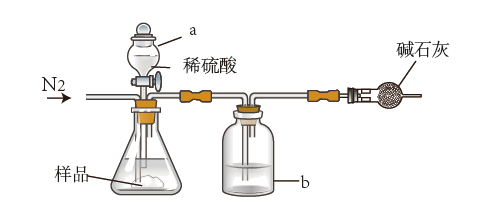
甲同学取一定质量(x g)的样品,用上图示装置测定CO2的质量。反应前先打开弹簧夹,通入一段时间的N2 , 然后关闭弹簧夹,接上总质量为m g的干燥管,再打开分液漏斗的活塞,滴加稀硫酸进行反应。待锥形瓶中不再有气泡产生,关闭分液漏斗的活塞,打开弹簧夹,再通入一段时间的N2.然后取下干燥管称得其质量为n g。
①仪器a的名称是,洗气瓶b中盛放的液体是。(写名称)
②锥形瓶中发生的反应的化学方程式为。
③两次通入N2的作用分别是、。
-
(2) 乙同学用图中所示方法和步骤进行实验:
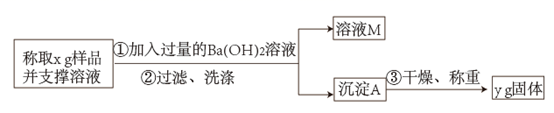
乙同学测得样品中Na2CO3的质量分数为。
-
(3) II.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
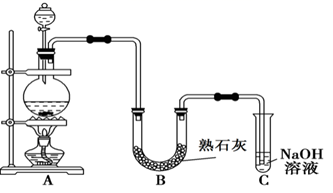
A中反应的化学方程式为。装置C的作用是,反应的化学方程式为。
-
(4) 漂白粉将在U形管中产生,此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2 , 为避免此副反应的发生,需控制B的温度在0~5℃,可采取的措施是。
②为避免另一副反应的发生,可将装置作何改进。
| 选项 | X | Y | Z | W | |
| A | Al | Cu | CuO | CuCl2 | |
| B | HCl | NaCl | Na2CO3 | NaOH | |
| C | H2O2 | O2 | H2O | H2CO3 | |
| D | Fe2O3 | FeCl3 | Fe(OH)3 | Fe |
-
(1) 欧洲一些国家用NaClO3氧化浓盐酸来制取ClO2 , 同时有Cl2生成,且Cl2的体积为ClO2的一半。这一反应的化学方程式是。
-
(2) 浓盐酸在上述反应中显示出来的性质是_______________(填写编号)。A . 只有还原性 B . 还原性和酸性 C . 只有氧化性 D . 氧化性和酸性
-
(3) 若上述反应产生0.1 mol Cl2 , 转移电子的物质的量为mol。
-
(4) 我国广泛采用将经干燥空气稀释的氯气通入填有固体亚氯酸钠(NaClO2)的柱内制得ClO2 , 表示这一反应的化学方程式是。和欧洲的方法相比,我国这一方法的主要优点是。
-
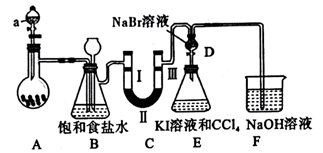
(1) 仪器a的名称是。
-
(2) 实验室常用二氧化锰和浓盐酸制备氯气,发生反应的化学方程式为。
-
(3) 装置B中饱和食盐水的作用是;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:。
-
(4) 装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ应依次加入(填字母)。
选项
a
b
c
d
Ⅰ
干燥的有色布条
干燥的有色布条
湿润的有色布条
湿润的有色布条
Ⅱ
浓硫酸
硅胶
无水氯化钙
碱石灰
Ⅲ
湿润的有色布条
湿润的有色布条
干燥的有色布条
干燥的有色布条
-
(5) 装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。反应一段时间后,D中溶液逐渐变为棕红色,该实验现象说明了氯的氧化性(填“>”或“<”)溴的氧化性:打开活塞,将装置D中少量溶液加入装置E中,振荡、静置,观察到的现象为,根据实验现象不能说明溴、碘的氧化性强弱,原因是。
-
(6) 装置F用于吸收余氯,相应的离子反应方程式为。
①Na2O2投入到紫色石蕊试液中溶液先变蓝,后褪色;
②Na2O 和Na2O2投入到水中都能生成NaOH;
③质量相等的NaHCO3与Na2CO3分别与相同浓度盐酸完全反应时,产生CO2的物质的量相等;
④为了除去粗盐中的Ca2+、Mg2+、SO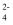 及泥沙,可将粗盐溶于水;然后按下列顺序进行操作∶加过量BaCl2溶液一加过量的NaOH溶液-过量 Na2CO3溶液-过滤一加过量盐酸-加热煮沸
及泥沙,可将粗盐溶于水;然后按下列顺序进行操作∶加过量BaCl2溶液一加过量的NaOH溶液-过量 Na2CO3溶液-过滤一加过量盐酸-加热煮沸
⑤区别NaHCO3与 Na2CO3溶液,可用Ca(OH)2溶液;
⑥NaHCO3固体可以做干粉灭火剂,金属钠起火可以用它来灭火;
⑦NaHCO3粉末中混有Na2CO3可配制成溶液通入过量的CO2 , 再低温结晶得到提纯。
- 目前人类比较容易利用的淡水资源是:( )A.陆地上的冰川 B.江河水、湖泊水、浅层地下水
- E The earth is getting warmer. The planet is suffering. But
- 3.(12分,计算能力挑战题)豌豆子叶的黄色(Y)对绿色(y)为显性,圆粒种子(R)对皱粒种子(r)为显性。某人用黄色圆
- 如图2所示,四个相同的玻璃瓶内装有深度不同的水。用筷子轻轻敲击瓶口或用嘴贴着瓶口吹气,会发出不同的声音。下列关于所发出声
- 如果直线ax+2y+2=0与直线3x-y-2=0平行,那么系数a= (A) (B) (C) (D)
- 已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉
- —Excuse me.Is this the right way to the Water World?—Sorry!I
- 下列对铯及其化合物的预测正确的是( ) A.铯的熔点很高 B.在自然界中,铯能以游离态存在 C.氯化铯易溶
- 下列各项不能用2n来表示的是( ) A.一个DNA分子复制n次后,子代DNA分子数B.含有n个碱基对的DNA分子的
- 历史地图是展现前人活动与地理空间结合的重要史料。观察地图,解读准确的是 A.美苏操纵欧洲,北约与华约对峙 B.柏
- 每组加点的词意义和用法都相同的一组是()。 A.今日往而不反者,竖子也 夺项王天下者必沛公也 B.然郑 亡,子亦有不利焉
- 我国科学家袁隆平院士利用野生水稻和普通水稻的多次杂交,培育出了高产的杂交水稻新品种,这是利用了生物多样性的哪一层次的价值
- 等比数列的公比q,前n项和,若成等差数列,则q=
- 下列国家中都属于地跨两大洲的国家是( ) A. 俄罗斯和中国 B. 土耳其和埃及 C. 美国和加拿大
- People, _______ in that country, enjoy such food all the mor
- 阅读下面语段,按要求回答问题: 白话文、英文、德文并不一定代表______.文言文也不一定代表______。在文言文的世
- 关于我国年降水量分布总趋势的描述,最准确的一项是 ( )A、自北向南递减 B、自西向东递减 C、自西北
- 根据光合作用的表达式,回答下列问题:(5分) (1)绿色植物细胞中的 是进行光合
- 已知之间的几组数据如下表: 1 2 3 4 5 60 2 1 3 3 4假设根据上表数据所得线性回归直线方程为中的前两组
- (1)证明 因为D,C,E,F分别是AQ,BQ,AP,BP的中点,所以EF∥AB,DC∥AB.所以EF∥DC. 又EF



