第2节 研究物质性质的方法和程序 知识点题库
把2.1g的CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加 ( )
A . 2.1g
B . 3.6g
C . 7.2g
D . 无法确定
钠应用于电光源上是由于( )
A . 高压钠灯发出的黄光射程远,透雾力强
B . 钠很软
C . 钠是一种电的良导体
D . 钠燃烧发出黄色火焰
现有NaCl、Na2O2、Fe2O3、NaHCO3和Al2O3等多种重要化合物.请用化学式填空:
(1)常作为潜水艇和呼吸面具中氧气的淡黄色固体是 ;
(2)常用于焙制糕点,也可用作抗酸药的是 ;
(3)属于两性氧化物的是 ;
(4)属于红棕色固体是 .
下列各物质中,不能由组成它的两种元素的单质直接化合得到的是( )
A . FeS
B . FeCl2
C . FeCl3
D . Fe3O4
关于NaHCO3溶液,下列表述不正确的是( )
A . c(Na+)=c(HCO3﹣)+c(CO32﹣)+c(H2CO3)
B . c(Na+)+c(H+)=c(HCO3﹣)+c(CO32﹣)+c(OH﹣)
C . HCO3﹣的水解程度大于HCO3﹣的电离程度
D . c(H+)+c(H2CO3)=c(OH﹣)+c(CO32﹣)
下列有关氨水和氯水的说法正确的是( )
A . 含有的微粒种类数相同
B . 久置后溶液的pH均可能减小
C . 都能与SO2发生氧化还原反应
D . 均具有强氧化性
下列说法正确的是( )
A . 用丁达尔效应鉴别氢氧化铁胶体和氯化铁溶液
B . 因为SO2有漂白性,所以它可使紫色石蕊溶液褪色
C . 氯化钠溶液在电流作用下电离成Na+离子和Cl﹣离子
D . 等质量的碳酸钠和碳酸氢钠与足量盐酸反应时,碳酸钠产生的CO2多
某无色透明的混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种气体.现将此混合气体通过品红溶液后,品红溶液褪色,向剩余气体中通入空气,很快变为红棕色.下列对于原混合气体成分的判断中正确的是( )
A . 肯定没有SO2和NO
B . 肯定没有Cl2、O2和NO2
C . 可能有Cl2和O2
D . 肯定只有NO
下列各组物质相互混合反应,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液
②过量NaOH溶液和明矾溶液
③Na2O2投入FeCl2溶液.
A . ①
B . ③
C . ②③
D . ①③
学法题
重要知识点 | 主要物理性质 | 重要的化学性质 | 主要用途(至少2条) |
过氧化钠 | |||
二氧化硫 | |||
氨气 |
下列气体中,呈黄绿色的是( )
A . CH4
B . NO2
C . CO2
D . Cl2
下列化合物中,不能由单质直接化合而得到的是( )
A . HCl
B . Na2O
C . FeCl3
D . FeCl2
有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06g Na2CO3和0.84g NaHCO3 , A、B中分别有10mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
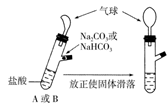
A . B装置的气球膨胀的体积大
B . 最终两试管中NaCl的物质的量一定相同
C . 若最终两气球体积不同,则盐酸的浓度一定小于或等于1mol/L
D . 若最终两气球体积相同,则盐酸的浓度一定大于或等于2mol/L
某小组利用氯酸钾与10 mol·L-1盐酸反应制氯气并进行氯气性质的探究,实验装置如图所示:
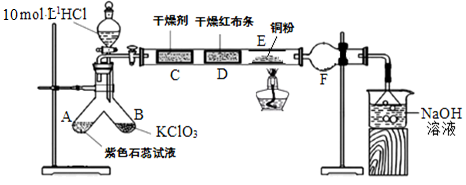
请回答:
-
(1) 装置F的名称是。
-
(2) E中实验现象是。
-
(3) 根据相关实验现象就可以证明起漂白作用的不是氯气而是次氯酸,相关现象是。
-
(4) 现要配制240mL 10 mol·Lˉ1所需盐酸,请回答下列问题:
①所用的仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要的仪器是。
②配制好的盐酸放入试剂瓶中后,需要贴上标签,请你在图标签上填好所配溶液的信息。

③配制过程中有下列实验操作步骤,其正确的顺序为。
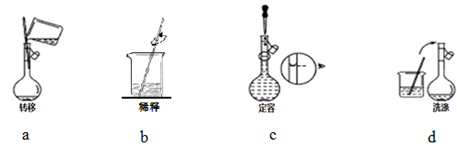
④下列操作会使配制结果偏高的是。
A.容量瓶洗净后未干燥直接用来配制溶液
B.反复摇匀后发现液面低于刻度线,继续加水至刻度线
C.定容时俯视读数
D.用量筒量取浓盐酸配制所需盐酸时,量筒仰视读数
A,B,C是中学化学常见物质(纯净物或水溶液),其转化关系如下(部分反应物或产物未标出;反应条件未标出)。回答下列问题:
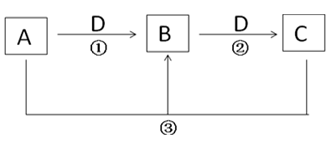
-
(1) 若D为气体,在标况下的密度为1.964g·L-1;A为强碱溶液,其焰色反应为黄色,则反应②的化学方程式为.
-
(2) 若B为白色胶状沉淀,D为强碱溶液.则反应③的离子方程式为
-
(3) 若A为黄绿色的气体,D为目前使用量最大的金属单质,则检验B物质中的阳离子时发生的离子方程式为.
-
(4) 若A为一种金属单质,常温下D浓溶液不能溶解A,D稀溶液能溶解A,但不产生H2 . 则反应②的离子方程式为.
-
(5) 若D为O2 , 要实现上面的转化,A、C分别可以是(各填一种,填化学式) .
将某碳酸钠和碳酸氢钠混合物 2.74 g加热到质量不再变化时,剩余物质的质量为 2.12 g,求混合物中碳酸钠的质量分数。(写出简要的计算过程)
-
(1) 碳酸氢钠的质量为克?
-
(2) 碳酸钠的质量分数为?
下列实验中,依据实验操作及现象,得出的结论正确的是( )
| 操 作 | 现 象 | 结 论 | |
| A | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| B | 将稀硝酸加入过量铁粉中,充分反应后再滴加KSCN溶液 | 有气体生成,溶液不呈血红色 | 稀硝酸将Fe氧化为Fe2+ |
| C | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭 | 浓硫酸具有吸水性 |
| D | 向5 mL KI溶液中加入1 mL相同浓度FeCl3溶液,充分反应后滴入KSCN溶液 | 溶液变血红色 | KI与FeCl3的反应有一定限度 |
A . A
B . B
C . C
D . D
化学与生活息息相关,下列说法错误的是( )
A . “84消毒液”的主要有效成分是NaClO,NaClO通过氧化灭活病毒
B . 铁粉和氧化铝发生的铝热反应可用于焊接铁轨
C . 疫苗一般应冷藏存放,以避免蛋白质变性
D . “红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味”文中的“气”是指乙烯
下列关于氯气及其化合物的说法正确的是( )
A . 可用钢瓶储存、运输液氯
B . 氢气可以在盛有氯气的集气瓶中燃烧,瓶口上方产生白色烟雾
C . 铁在氯气中燃烧的产物和铁与盐酸反应产生的氯化物相同
D . 新制氯水滴加至有色布条上,布条褪色说明溶液中存在Cl2
以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的步骤如下:
步骤1:将电石渣与水混合,形成浆料。
步骤2:控制电石渣过量,75℃时向浆料中通入Cl2 , 该过程会生成Ca(ClO)2 , Ca(ClO)2会进一步转化为Ca(ClO3)2 , 少量Ca(ClO)2分解为CaCl2和O2 , 过滤。
步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25℃结晶,得KClO3。
下列说法正确的是( )
A . 控制通入Cl2的速率,可以提高Cl2的利用率
B . 25℃时,Ca(ClO3)2的溶解度比KClO3的溶解度小
C . 步骤2中,过滤所得滤液中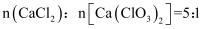 D . 生成 Ca(ClO)2的化学方程式为
D . 生成 Ca(ClO)2的化学方程式为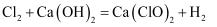
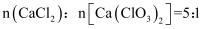 D . 生成 Ca(ClO)2的化学方程式为
D . 生成 Ca(ClO)2的化学方程式为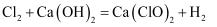
最近更新
- 一个地区从某年起几年之内的新生婴儿数及其中的男婴数如下:时间范围1年内2年内3年内4年内新生婴儿数55449607135
- a和b属于同一动物体内的两个细胞,通过对其核内DNA分子含量的测定,发现a细胞中DNA含量是b细胞的两倍,最可能的解释是
- 下列内容中,可以证明“1966—1976年的‘’是一场内乱”的是 ( ) ①掀起夺取党和政府领导权的狂潮 ②迫害
- 1938年国民政府电文称:查第二期抗战开始以及我备战区本运动战、游击战相配合积小胜为大胜之最高原则,以攻为守指导作战,屡
- We are in great need of a more capable manager,________ with
- 世界市场开始出现于 A.资本主义萌芽产生后 B.新航路开辟后 C.第一次工业革命后
- 如图所示,上端开口的光滑圆柱形气缸竖直放置,截面积为40cm2的活塞将一定质量的气体封闭在气缸内。在气缸内距缸底60cm
- 食物中储存的化学能来自于光能的转化,这种转化主要是通过植物细胞中的哪种结构实现的?( ) A.细胞核
- 下图为巴斯德的“鹅颈瓶实验”,该实验说明()A.微生物只能来自空气中的微生物 B.微生物必须在有氧条件下才能产生 C.微
- 在西北地区荒漠化土地面积中,导致荒漠化的第一大人为因素是: A.过度放牧 B.过度开垦 C.过度樵采
- 第二次工业革命期间新兴的工业部门有( ) ①汽车制造业;②钢铁工业;③电力工业;④电讯 工业;⑤化学工业 A.①②
- 阅读下面一段文章,用一句话概括其要点。(不超过20个字) 小说不是论文,它的主题思想不能直说,也不能硬贴上去。好的小说总
- 已知△ABC的面积S=,a=2,b=2,解三角形.
- 23.请简要概括下表所包含的主要信息,表述中不得出现具体数字。
- 请对下面两个病句提出修改意见(或作出修改)。(4分) (1)父亲从头到脚凝视着儿子,激动得热泪盈眶,一句话也说不出
- 如图6所示,边界MN与PQ平行,其间有垂直纸面向里的匀强磁场,矩形导线框框面与磁场方向垂直,其边与边界MN平行,若导线
- 短文改错(共10小题;每小题1分,满分10分) 下面短文中有10处语言错误。请在有错误的地方增加、删除或修改某个单词。
- 如图是“东南亚部分区域图”,读后回答下列问题:(共8分)(1)A国居民中绝大部分是________人。这里属______
- 已知a2-a-1=0,则a3-2a+2011=_______.
- 我舰在敌岛A南偏西50°相距12海里的B处,发现敌舰正由岛沿北偏西10°的方向以10海里/时的速度航行.问我舰需以多大速



