3.2 离子键 知识点题库
下列各组物质气化或熔化时,所克服的粒子间的作用力属于同种类型的是( )
A . 二氧化硅和生石灰的熔化
B . 氯化钠和铁的熔化
C . 碘和干冰的升华
D . 氯化铵受热气化和苯的气化
下列性质中,可以证明某化合物形成的晶体一定是离子晶体的是( )
A . 可溶于水
B . 具有较高的熔点
C . 水溶液能导电
D . 熔融状态能导电
下列物质中含有离子键的是( )
A . CO2
B . NaCl
C . HCl
D . CH4
下列说法正确的是( )
A . 在离子化合物中,可能含共价键
B . 在共价化合物中,可能含离子键
C . 含共价键的化合物一定是共价化合物
D . 含离子键的化合物不一定是离子化合物
下列关于离子键、共价键的叙述中正确的是( )
A . 非极性键只存在于双原子的单质分子(如Cl2)中
B . 在共价化合物里,可能存在离子键
C . 在离子化合物里,只存在离子键,没有共价键
D . 化学反应的实质是旧键的断裂,新键的形成
有关晶体的结构如下图所示,则下列说法中错误的是( )
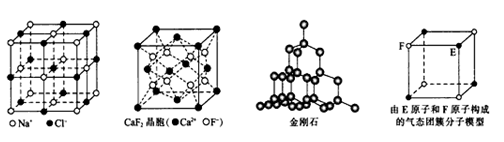
A . 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B . 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C . 在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D . 该气态团簇分子的分子式为EF或FE
二茂铁[(C5H5)2Fe]是由一个二价铁离子和2个环戊烯基负离子构成,它的发现可以说是有机金属化合物研究中具有里程碑意义的事件,它开辟了金属有机化合物研究的新领域。已知:二茂铁熔点是173 ℃(在100 ℃时开始升华),沸点是249 ℃,不溶于水,易溶于苯、乙醚等非极性溶剂。下列说法正确的是( )
A . 二茂铁属于离子晶体
B . 在二茂铁结构中,C5H5-与Fe2+之间形成的化学键类型是离子键
C . 已知:环戊二烯的结构式为: 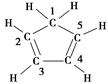 ,则其中碳环上有2个π键和5个σ键
D . 二价铁离子的基态电子排布式为:[Ar]3d44s2
,则其中碳环上有2个π键和5个σ键
D . 二价铁离子的基态电子排布式为:[Ar]3d44s2
 ,则其中碳环上有2个π键和5个σ键
D . 二价铁离子的基态电子排布式为:[Ar]3d44s2
,则其中碳环上有2个π键和5个σ键
D . 二价铁离子的基态电子排布式为:[Ar]3d44s2
下列说法正确的是( )
A . 只要含有金属元素的化合物一定是离子化合物
B . 全部元素都由非金属元素构成的化合物一定是共价化合物
C . 离子化合物一定是电解质
D . 共价化合物一定是非电解质
已知①Na2O2 ②O2 ③HClO ④H2O2 ⑤Cl2 ⑥NaClO ⑦O3 七种物质都具有强氧化性。请回答下列问题:
-
(1) 上述物质中互为同素异形体的是 ( 填序号,下同)。
-
(2) 含非极性键的共价化合物是。
-
(3) 属于离子化合物的有种。
-
(4) Na2O2、HClO、H2O2均能用于制备O2。
①HClO在光照条件下分解生成O2和HCl,用电子式表示HCl的形成过程。
②写出Na2O2与H2O反应的方程式并标出电子转移方向和数目。
③H2O2在二氧化锰催化作用下可以制备O2。若6.8 g H2O2参加反应,则转移电子数目为,
生成标准状况下O2体积为L。
下列叙述正确的是( )
①两种原子构成的分子中的化学键都是极性键
②两种不同非金属元素原子间形成的化学键都是极性键
③含有共价键的化合物一定是共价化合物
④只要是离子化合物,其熔点就比共价化合物的熔点高
⑤难失去电子的原子,易形成阴离子
⑥单质分子中不存在化学键,化合物的分子中才存在化学键
⑦离子化合物中一定含有离子键
A . 只有①⑦
B . 只有②⑦
C . 只有⑦
D . 只有①⑤⑦
下列说法正确的是( )
A . 只含有共价键的物质属于共价化合物
B . 所有物质中都含有化学键
C . 含有离子键的物质肯定含金属元素
D . 只要含离子键的化合物就属于离子化合物
下列叙述正确的是( )
A . 离子化合物中不可能含共价键
B . 活泼金属与活泼非金属化合时能形成离子键
C . 由非金属元素形成的化合物一定是共价化合物
D . 共价化合物不可能含有离子键,熔融状态可以导电
下面有关分子性质和晶体结构的叙述中,错误的是( )
A . 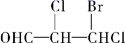 分子中含有2个手性碳原子
B . 无机含氧酸可以用(HO)mROn表示,n值越大,则该含氧酸的酸性越强
C . 氯化铯晶体中,每个Cs+周围紧邻且距离相等的Cl-有6个
D . 金刚石为空间网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子
分子中含有2个手性碳原子
B . 无机含氧酸可以用(HO)mROn表示,n值越大,则该含氧酸的酸性越强
C . 氯化铯晶体中,每个Cs+周围紧邻且距离相等的Cl-有6个
D . 金刚石为空间网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子
下列叙述正确的是( )
A . 元素周期表中所有元素都是在自然界中发现的,过渡元素都是金属元素
B . 同一周期元素的原子,半径越小越容易失去电子
C . 元素的性质呈周期性变化的根本原因是核外电子排布呈周期性变化
D . 第IA族元素与第VIIA族元素形成的化合物都是离子化合物
X、Y、Z均为短周期元素,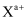 、
、 、
、 简单离子的电子层结构相同,下列说法正确的是( )
简单离子的电子层结构相同,下列说法正确的是( )
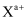 、
、 、
、 简单离子的电子层结构相同,下列说法正确的是( )
简单离子的电子层结构相同,下列说法正确的是( )
A . 原子序数:X>Y>Z
B . 离子半径: C .
C . 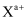 的氧化性一定大于
的氧化性一定大于 D . X与Z可能形成既含离子键又含共价键的化合物
D . X与Z可能形成既含离子键又含共价键的化合物
 C .
C . 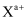 的氧化性一定大于
的氧化性一定大于 D . X与Z可能形成既含离子键又含共价键的化合物
D . X与Z可能形成既含离子键又含共价键的化合物
下列含有共价键的离子化合物是( )
A . CaO
B . NaClO
C . MgCl2
D . HCl
研究低温超导体材料的性能对解决能源危机有重要意义。金属K与 和形成的一种低温超导材料的立方晶胞结构如图所示,晶胞边长为
和形成的一种低温超导材料的立方晶胞结构如图所示,晶胞边长为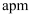 , K原子位于晶胞的内部和棱上。下列说法错误的是( )
, K原子位于晶胞的内部和棱上。下列说法错误的是( )
 和形成的一种低温超导材料的立方晶胞结构如图所示,晶胞边长为
和形成的一种低温超导材料的立方晶胞结构如图所示,晶胞边长为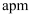 , K原子位于晶胞的内部和棱上。下列说法错误的是( )
, K原子位于晶胞的内部和棱上。下列说法错误的是( )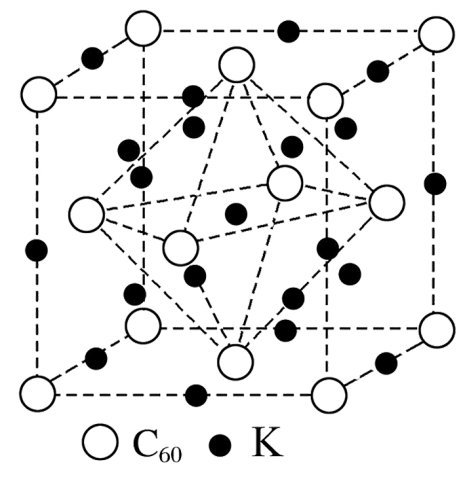
A . 该物质的化学式为 B . 棱上K原子处在
B . 棱上K原子处在 构成的四面体空隙中
C . 每个
构成的四面体空隙中
C . 每个 周围紧邻且距离相等的
周围紧邻且距离相等的 分子有12个
D .
分子有12个
D .  与
与 间的最短距离为
间的最短距离为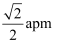
 B . 棱上K原子处在
B . 棱上K原子处在 构成的四面体空隙中
C . 每个
构成的四面体空隙中
C . 每个 周围紧邻且距离相等的
周围紧邻且距离相等的 分子有12个
D .
分子有12个
D .  与
与 间的最短距离为
间的最短距离为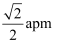
下列说法正确的是( )
A . 元素电负性由大到小的顺序:O>N>C
B . 一个乙烯分子含2个π键和4个σ键
C . 氯化钠和氯化铯晶体中氯离子的配位数相同
D . 第一电离能的大小:Al>Mg>Na
不同主族的短周期元素X、Y、Z、W其原子序数依次增大,X、Y的简单离子的电子层结构相同,短周期主族元素原子中Y的原子半径最大,Z原子最外层电子数是K层的3倍。下列说法错误的是( )
A . 熔化YW时离子键被破坏
B . X的简单氢化物可作制冷剂
C . 离子的还原性:Z>W
D . Y的氧化物为离子化合物,不含共价键
水溶液呈酸性,且属于离子化合物的是( )
A . H2SO4
B . NaCl
C . CH3COONa
D . NH4Cl
最近更新
- 温度升高时,温度计内的酒精柱会上升,从微观角度分析,其原因是A.酒精分子的体积变大 B.酒精分子的
- “Where is Zunyi?” “It is in ____ .” A.Guizhou B
- 已知⊙O中,AC为直径,MA、MB分别切⊙O于点A、B. (1)如图①,若∠BAC=25°,求∠AMB的大小; (2)如
- 下图中图1为我国某河流河道示意图,甲为一河心沙洲,图2为该沙洲一年内面积变化统计图,读图完成1—2题。1.该河位于我国的
- 阅读下面的材料,根据要求作文。(60分) 朱自清先生说:“在中等及中等以上的教育里,经典阅读应该是一个必要的项目。其价
- 如图,滑块A放在木板B的左端,开始A、B都静止。已知,滑块A与长板B之间的动摩擦因数,B与水平地面的动摩擦因数.现启动电
- 下列有关天气特点的叙述,错误的是A.天气是反映一个地方短时间里的大气状况B.同一时刻,不同地方的天气可能差别很大 C.天
- W、X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z- ,Y+和Z-离子具有相同的电子层
- L市政协就市政府起草的《L市大气污染防治条例(草案)》开展协商,提出数百条建议,在最终提交给市人代会审议的草案中,有8
- 下列关于细胞主要化学成分的叙述中,不正确的是( ) A.蛋白质的多样性与氨基酸的种类、数目、排序等有关B.脱氧核
- 两位同学帮助老师整理实验室时,在标有“单质”的药柜中发现一瓶失去标签的黑色粉末A,在标有“氧化物”的药柜中发现另一瓶失去
- 数列满足,(),是常数.(Ⅰ)当时,求及的值;(Ⅱ)数列是否可能为等差数列?若可能,求出它的通项公式;若不可能,说明理由
- 人民网·中国新闻网正式推出“直通中南海——中央领导人和中央机构留言板”。该留言板突出互动性,旨在让广大网友对中央领导人倾
- 1.下列各句中,加点的成语使用恰当的两项是( ) A.诗歌解读就是专家也未必在行,特别是将汉以前的古体诗拿给讲授古
- 观察等式:, 和, ……,由此得出以下推广命题不正确的是 A. B. C.D.
- 古罗马的《民法大全》规定:“任何人不能仅因为思想而受惩罚。”其体现的司法原则是( ) A.没有证据不能定罪
- 克伦威尔为巩固资产阶级革命成果,采取措施包括( ) ①镇压平等派和掘地派 ②先后征服爱尔兰和苏格兰 ③颁布《航海
- 汉朝、宋朝和元朝加强中央集权的措施最相似的是( ) A 设立特务机构 B 改变和
- 氢—氧燃料电池是将H2和O2分别通入电池,穿过浸入20%~40%的KOH溶液的多孔碳电极,其电极反应式为:2H2+4OH
- 下图是一种生物体的某个细胞示意图,据图判断下列说法中,正确的是( ) A.这种生物体内所含的多糖是糖原B.此



