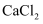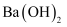3.2 离子键 知识点题库
下列说法中一定正确的是( )
A . 固态时能导电的物质一定是金属晶体
B . 熔融状态能导电的晶体一定是离子晶体
C . 水溶液能导电的晶体一定是离子晶体
D . 固态不导电而熔融状态导电的晶体一定是离子晶体
元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。下列说法中错误的是( )
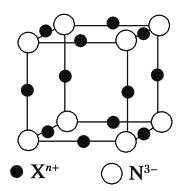
A . Xn+的核外电子数为19
B . 该晶体中阳离子与阴离子个数比为3:1
C . Xn+中n=1
D . 晶体中每个Xn+周围有2个等距离且最近的N3-
下列有关物质结构的叙述正确的是( )
A . 在离子化合物中不可能存在非极性共价键
B . 由电子定向移动而导电的物质一定是金属晶体
C . 有键能很大的共价键存在的物质熔沸点一定很高
D . 只含有共价键的物质不一定是共价化合物
在下列化合物中:H2O2、Na2O2、I2、NaCl、CO2、NH4Cl用化学式回答下列问题:
(1)只由非金属元素组成的离子化合物是
(2)只有极性共价键的共价化合物是 ;
(3)只含有非极性共价键的是 ;
(4)既有离子键又有非极性键的化合物是
下列化合物中既有离子键又有共价键的是( )
A . MgCl2
B . NaOH
C . HBr
D . N2
下列各项所述的数字不是6的是( )
A . 在NaCl晶体中,与一个Na+最近的且距离相等的Cl﹣的个数
B . 在金刚石晶体中,围成最小环的原子数
C . 在二氧化硅晶体中,围成最小环的硅原子数
D . 在CsCl晶体中,与一个Cs+最近的且距离相等的Cl﹣的个数
关于晶体的下列说法正确的是( )
A . 在晶体中只要有阴离子,就一定有阳离子
B . 在晶体中只要有阳离子,就一定有阴离子
C . 原子晶体的熔点一定比金属晶体的高
D . 分子晶体的熔点一定比金属晶体的高
下列有关说法正确的是( )
A . NaOH是只含离子键的离子化合物
B . HCl溶于水没有破坏共价键
C . 碳在O2中燃烧时,破坏碳和O2中化学键吸收的总能量大于形成CO2中化学键释放的总能量
D . 在Cl2+2NaBr=2NaCl+Br2反应过程中有离子键和共价键的断裂,也有离子键和共价键形成
下列说法中正确的是( )
A . 两个原子或多个原子之间的相互作用叫做共价键
B . 阴、阳离子间通过静电引力而形成的化学键叫做离子键
C . 分子晶体中一定含有共价键,离子晶体中一定含有离子键
D . 氯化钠晶体中含有阳离子,氯化钠溶液中也含有阳离子
下列说法正确的是( )
A . 金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属
B . 变价金属一定是过渡元素
C . 不含金属元素的化合物也可能是离子化合物
D . 显酸性的溶液中溶质只能是酸或强酸弱碱盐
下列说法正确的是( )
A . 共价化合物中可能含有离子键
B . 非金属原子不可能形成离子化合物
C . 不存在没有化学键的分子
D . 双原子单质分子中的共价键一定是非极性键
在CuSO4·5H2O晶体中( )
A . 存在水分子
B . 没有共价键
C . 只有离子键
D . 含有范德华力
下列说法正确的是( )
A . 互为同素异形体的物质必然具有相似的性质
B . 碳酸钠固体中不存在阴阳离子
C . 氢化锂三兄弟——LiH、LiD、LiT三种物质的质子数之比为4︰5︰6
D . 同分异构体之间的相互转化一定是化学变化
下列说法正确的个数为( )
①化学键断裂,一定发生化学变化
②任何物质中都存在化学键
③氢键是极弱的化学键
④离子键就是阴、阳离子之间的静电吸引力
⑤活泼金属与活泼非金属化合时能形成离子键
⑥任何共价键中,成键原子成键后均满足稳定结构
⑦验证化合物是否为离子化合物的实验方法是可以看其熔化状态下能否导电
⑧两种非金属元素形成的化合物不可能含有离子键
A . 1
B . 2
C . 3
D . 4
下列叙述正确的有( )个
①用电子式表示MgCl2的形成过程为: ![]()
②两个不同种非金属元素的原子间形成的化学键都是极性键
③离子化合物在熔融状态时能够导电
④含有非极性键的化合物一定是共价化合物
⑤元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
⑥次氯酸的电子式: ![]()
⑦离子化合物中一定含有离子键
A . 1
B . 2
C . 3
D . 4
下列晶体的分类正确的一组是( )
|
选项 |
离子晶体 |
共价晶体 |
分子晶体 |
金属晶体 |
|
A |
|
石墨 |
Ar |
Hg |
|
B |
|
金刚石 |
|
Ag |
|
C |
|
SiC |
|
Mg |
|
D |
|
Si |
|
NaH |
A . A
B . B
C . C
D . D
下列物质中,含有共价键的离子晶体是( )
A . 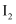 B . НСl
C . NaBr
D . KOH
B . НСl
C . NaBr
D . KOH
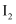 B . НСl
C . NaBr
D . KOH
B . НСl
C . NaBr
D . KOH
下列关于离子化合物的说法正确的是( )
A . 离子化合物一定能导电
B . 离子化合物不一定易溶于水
C . 能导电的物质一定是离子化合物
D . 溶于水能导电的化合物一定是离子化合物
下列叙述中正确的是 ( )
A . 含离子键的化合物一定是离子化合物
B . 含共价键的化合物一定是共价化合物
C . 全部由非金属元素形成的化合物一定是共价化合物
D . 在离子化合物中也可能含有金属键
铜的某种氧化物的晶胞结构如图所示。下列说法错误的是( )
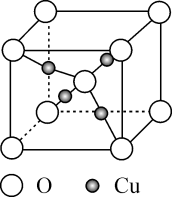
A .  位于元素周期表
位于元素周期表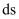 区
B . 该晶胞中
区
B . 该晶胞中 的配位数为4
C . 该物质的化学式为
的配位数为4
C . 该物质的化学式为 D . O位于
D . O位于 围成的四面体的体心
围成的四面体的体心
 位于元素周期表
位于元素周期表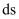 区
B . 该晶胞中
区
B . 该晶胞中 的配位数为4
C . 该物质的化学式为
的配位数为4
C . 该物质的化学式为 D . O位于
D . O位于 围成的四面体的体心
围成的四面体的体心
最近更新
- 如图表示生物圈中碳元素的循环过程,下列有关叙述不正确的是() A. 温室效应主要是由⑦过程造成的 B. 图中 A、B分别
- 金属钠着火时,可以灭火的物质是 A. 水 B. 沙子 C. 煤油 D. 二
- 《水经注》是一部记载( ) A.全国主要河流的专著 B.全国主要河流发源地的专著 C.
- I heard a terrible noise in his room and went to see what it
- 新版瓯剧《高机与吴三春》将昆曲精髓融入瓯剧表演中,在音乐、舞美、表演上进行大胆创新,使瓯剧焕发生机、历久弥新。这表明文化
- “白色污染”是指塑料袋、快餐盒塑料制品等形成的污染。为治理“白色污染”,消费者应该( )A、回收利用,使其化害为利,
- I don’t understand how you got a ticket.I always you
- 下列关于第②步和第③步的说法,正确的是 A.加入H2O2的主要作用是将溶液中的Fe2+氧化为Fe3+ B.CuSO4·5
- 胰岛素分子是一种蛋白质分子,现有如下材料: ①胰岛素含有2条多肽链,A链含有21个氨基酸,B链含有30个氨基酸,2条多肽
- 依次填入下列各句横线处的词语,最恰当的一组是 ①“非典”的袭击非但没有使我国人民_________,反而增强了全国人民万
- 纬度的变化规律是( ) A.从南向北逐渐增大B.从东向西逐渐增大 C.从赤道向两极逐渐增大D.从两极向赤道逐渐增
- 阅读下面这首唐诗,完成下题。 古风·登高望四海 李白 登高望四海,天地何漫漫。霜被群物秋,风飘大荒寒。 荣华东流水,万
- 继福建土楼后, 2011年10月3日,从联合国教科文组织在希腊莱斯沃斯岛召开的世界地质公园评审大会上传来消息,中国宁德地
- 血液的组成包括( ) A.血浆、红细胞 B.血浆、血细胞 C.血
- Feedthe worldWiththe global population expected to rise to 9
- 下列各句中加点的词语,使用恰当的一项是 A.被誉为“华夏民居第一宅”的王家大院,不仅拥有庞大的建筑群,还保存了大量卓尔不
- 对下列实验过程的评价,正确的是() A.某溶液中加稀硫酸生成无色气体,说明原溶液中一定有CO32﹣ B.某溶液中滴加Ba
- 某混合气体可能是CO、CO2、H2、H2O、CH4之中的一种或几种组成,为了验证混合气体的成分,设计了如右图所示的装置进
- 燕麦幼苗产生生长素部位、感受光刺激部位、向光弯曲部位依次为胚芽鞘的 ( ) A.尖端、尖端下面的一段、
- 下列各句中,没有语病的一句是 ( ) A. 部分学生