3.1 原子间的相互作用 知识点题库
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
A . NH4Cl→NH3↑+HCl↑
B . NH3+CO2+H2O→NH4HCO3
C . 2NaOH+Cl2→NaCl+NaClO+H2O
D . 2Na2O2+2CO2→2Na2CO3+O2
下面的排序不正确的是( )
A . 空间利用率:Cu>Na>Po
B . 熔点由高到低:金刚石>NaCl>K>CO2
C . 硬度由大到小:SiC>金刚石
D . 晶格能由大到小:NaF>NaCl>NaBr
下列说法正确的是( )
A . 化学键的形成一定伴随着电子的转移和能量变化
B . NaCl和SiC晶体熔化时,克服粒子间作用力的类型相同
C . 24Mg32S晶体中电子总数与中子总数之比为1:1
D . 某晶体固态不导电水溶液能导电,说明该晶体是离子晶体
你认为下列对化学知识概括合理的组合是( )
①金属晶体中存在离子,但却不存在离子键
②原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键
③原子晶体硬度一般比分子晶体大,分子晶体熔点不一定比金属晶体低
④固态能导电的一定是金属晶体
⑤NF3的沸点比NH3的沸点低是因为N﹣F比N﹣H键的键能小
⑥原子晶体一定由原子构成,由原子构成的晶体不一定是原子晶体
⑦共价化合物中可能含有离子键
⑧金属晶体中简单立方堆积的配位数是8,空间利用率最低.
A . 只有②③④
B . 只有②③⑦
C . 只有①③⑥
D . 只有⑤⑥⑧
[化学——选修3:物质结构与性质]
“摩尔盐”是分析化学中的重要试剂,化学式为(NH4)2Fe(SO4)2·6H2O。“摩尔盐”在一定条件下分解的方程式为:4[(NH4)2Fe(SO4)2·6H2O] ![]() 2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
-
(1) 铁元素在元素周期表中的位置为,其价层电子排布图为。
-
(2) 组成“摩尔盐”的非金属元素中第一电离能最大的元素为。“摩尔盐”的分解产物中属于非极性分子的化合物是。
-
(3) NH3的沸点比N2O的沸点(填“高”或“低”),其主要原因是。
-
(4) K3[Fe(CN)6]常用于检验Fe2+ , K3[Fe(CN)6]中除了离子键以外还存在的化学键为,与CN—互为等电子体的单质的分子式为_。HCN分子中σ键和π键的个数之比为。
-
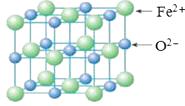
(5)
FeO晶胞结构如下图所示,FeO晶体中Fe2+配位数为,若该晶胞边长为acm,则该晶胞密度为。
下列各组分子中,都属于含极性键的非极性分子的是( )
A . CO2H2S
B . NH3 HCl
C . P4 CCl4
D . C2H4 CH4
关于化学键的下列叙述中,下列叙述不正确的是( )
A . 离子化合物可能含共价键
B . 共价化合物可能含离子键
C . 离子化合物中必含离子键
D . 共价化合物中不含离子键
下列微粒中同时具有离子键、共价键和配位键的化合物是( )
A . NH4Cl
B . Na2O2
C . H3O+
D . MgO
下列说法正确的是( )
A . Na2O2、NaClO中所含化学键类型完全相同
B . 只有活泼金属与活泼非金属元素之间才能形成离子键
C . D2O和T2O是同一物质
D . 氯气与NaOH反应的过程中,同时又离子键、极性键和非极性键的断裂和形成
下列关于化学键的叙述正确的是( )
A . 阴、阳离子通过静电吸引形成的强烈的相互作用
B . 只由非金属元素组成的化合物不可能是离子化合物
C . 金属元素与非金属元素化合时,不一定形成离子键
D . 只有活泼金属与活泼非金属之间才能形成离子键
下列说法正确的是( )
A . 有机化合物中只存在极性键
B . 碳原子最外层有4个电子,在形成化合物时必须与4个原子结合
C . 碳原子间可形成非极性键
D . 碳原子易失去或获得电子而形成阳离子或阴离子
下列物质中只含有离子键的是( )
A . H2O2
B . NaCl
C . KOH
D . Cl2
下列说法不正确的是( )
A . 纯碱和烧碱熔化时克服的化学键类型相同
B . 加热蒸发氯化钾水溶液的过程中有分子间作用力的破坏
C . CO2溶于水和干冰升华都只有分子间作用力改变
D . 石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏
下列变化中,既有旧化学键断裂,又有新化学键形成的是( )
A . 酒精溶解于水
B . 氯化钠受热熔融
C . 碘单质受热产生紫色气体
D . 碳酸氢铵受热产生刺激性气味
下列说法正确的是( )
A . 氯化氢气体溶于水破坏离子键,产生H+和Cl-
B . 硅晶体熔化与碘化氢分解需克服的化学键类型相同
C . NH3和HCl都极易溶于水,是因为都可以和H2O形成氢键
D . CO2和SiO2的熔沸点和硬度相差很大,是由于它们所含的化学键类型不同
下列叙述正确的是( )
①两种原子构成的分子中的化学键都是极性键
②两种不同非金属元素原子间形成的化学键都是极性键
③含有共价键的化合物一定是共价化合物
④只要是离子化合物,其熔点就比共价化合物的熔点高
⑤难失去电子的原子,易形成阴离子
⑥单质分子中不存在化学键,化合物的分子中才存在化学键
⑦离子化合物中一定含有离子键
A . 只有①⑦
B . 只有②⑦
C . 只有⑦
D . 只有①⑤⑦
“结构决定性质”是化学科学的重要理论。
-
(1) 下列关于基态O原子结构的相关描述中错误的是________。A . 轨道表达式(电子排布图)为
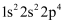 B . 有2个未成对电子
C . 电子占据最高能级的电子云轮廓图为哑铃(纺锤)形
D . 价电子数为4
B . 有2个未成对电子
C . 电子占据最高能级的电子云轮廓图为哑铃(纺锤)形
D . 价电子数为4
-
(2) Na的焰色反应为黄色,其原因是。
-
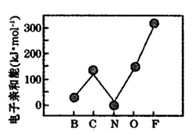
(3) 元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的电子亲和能E1变化趋势如图所示。氮元素的E1呈现异常的原因是。
-
(4) K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是。
-
(5) Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是。
下列叙述中,错误的是( )
A . 在共价化合物分子内,一定不存在离子键
B . HBr、CO2、H2O、CS2都只含极性共价键
C . NH3分子中所有原子均满足8e-稳定结构
D . CaO和NaCl晶体熔化时要破坏离子键
下列说法正确的是( )
A . 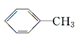 的一溴代物和
的一溴代物和 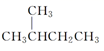 的一溴代物都有4种(不考虑立体异构)
B . Cu(OH)2是一种蓝色沉淀,既溶于盐酸、也能溶于氨水中,故为两性氢氧化物
C . 区别晶体与非晶体最科学的方法是对固体进行X−射线衍射实验
D . 乙烯脲的结构如图所示:
的一溴代物都有4种(不考虑立体异构)
B . Cu(OH)2是一种蓝色沉淀,既溶于盐酸、也能溶于氨水中,故为两性氢氧化物
C . 区别晶体与非晶体最科学的方法是对固体进行X−射线衍射实验
D . 乙烯脲的结构如图所示: 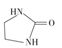 ,则该分子中含σ键与π键数目之比为8:1
,则该分子中含σ键与π键数目之比为8:1
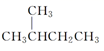 的一溴代物都有4种(不考虑立体异构)
B . Cu(OH)2是一种蓝色沉淀,既溶于盐酸、也能溶于氨水中,故为两性氢氧化物
C . 区别晶体与非晶体最科学的方法是对固体进行X−射线衍射实验
D . 乙烯脲的结构如图所示:
的一溴代物都有4种(不考虑立体异构)
B . Cu(OH)2是一种蓝色沉淀,既溶于盐酸、也能溶于氨水中,故为两性氢氧化物
C . 区别晶体与非晶体最科学的方法是对固体进行X−射线衍射实验
D . 乙烯脲的结构如图所示:
锰系氧化物催化降解甲醛具有去除效率高无二次污染等优点,其中一种催化机理如图所示。下列说法错误的是( )
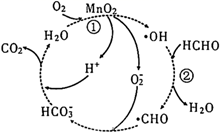
A .  为中间产物
B .
为中间产物
B .  降低了反应①的活化能
C . 反应②中有碳氧键断裂
D . 该机理的总反应的化学方程式为
降低了反应①的活化能
C . 反应②中有碳氧键断裂
D . 该机理的总反应的化学方程式为 
 为中间产物
B .
为中间产物
B .  降低了反应①的活化能
C . 反应②中有碳氧键断裂
D . 该机理的总反应的化学方程式为
降低了反应①的活化能
C . 反应②中有碳氧键断裂
D . 该机理的总反应的化学方程式为 
最近更新
- 某同学为探究不同浓度的生长素溶液对小麦种子萌发的影响,设计了如下实验。 材料用具:小麦种子若干,试管、培养皿、移液管、滤
- 对下列加点实词解释有误的一项是( ) A 暴秦之欲无厌厌:满足。 B 欲流之远者,必浚其泉源浚:疏通,深挖。 C 原庄宗
- 在△ABC中,M是BC的中点,AM=3,BC=10,则·=________ .
- We have known each other _______we were little babies.
- 2008年春节前夕,50年一遇的雪灾与冰冻肆虐大半个中国,尤其是从来都极少见到过雪的南方地区更为严重,春运形势“雪上加霜
- 如图,⊙O是△ABC的外接圆,P是⊙O外的一点,AM是⊙O的直径,∠PAC=∠ABC (1)求证:PA是⊙O的切线;
- 在南方谈话中指出:“改革开放胆子要再大一些,敢于试验,不能像小脚女人一样。看准了的,就大胆地试,大胆地闯。深圳的重要经验
- .基辛格在《论中国》中说写道“在外交政策中,政治家常常通过寻求共同利益来达到目的。却反其道而行之,对交叉重叠的敌意加以利
- 公元2世纪时,有一个国家的居民不出国,就可以游览地中海沿岸各地的风光,你知道他是哪国人?A.罗马帝国 B.奥斯曼土耳
- 已知的模分别为1、2、3,则的最大值为
- 人红细胞的渗透压与x浓度的食盐水相当,而浸在y浓度食盐水中的红细胞破裂;浸在z浓度食盐水中的红细胞收缩。则这三种食盐水的
- A tiny baby soon learns to ____ its mother’s face from other
- 下列说法或表达式正确的是( ) A.CaCO3的电离方程式:CaCO3Ca2++CO32- B.物质的量浓度相同,
- 如图,O是直线BD上一点,∠BOC=36º,∠AOB=108º则与∠AOB互补的角有
- 谚语:“大河有水小河满,大河无水小河干。”这句话生动说明 A.大河里的水和小河里的水关系密切 B.集体利益和个人利益是相
- 我国海关对凡入境的货物都进行严格检疫,严禁境外有害生物(包括虫卵和微生物)流入境内,若其一旦流入境内适宜的环境中,结果是
- ⒎下图表示人体内两种重要化合物 A与B的化学组成关系,相关叙述中正确的是 ( )
- 半径为R的四分之一圆弧支架竖直放置,圆弧边缘C处有一小定滑轮,一根长度大于2R的轻绳两端系着质量分别为m1、m2的物体,
- 某同学在做植物细胞质壁分离实验时,观察到紫色洋葱表皮细胞的中央液泡逐渐缩小,这说明() A.洋葱表皮细胞是活细胞
- 2009年我国财政安排了9500亿元赤字,其中包括2000亿元的地方债,该地方债为期三年,个人购买可免利息税。回答 发行



