3.1 原子间的相互作用 知识点题库
无水CoCl2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变成无水CoCl2 , 故常在实验室中用作吸湿剂和空气湿度指示剂.
CoCl2+H2O⇌CoCl2•xH2O
深蓝色 粉红色
现有65g无水CoCl2 , 吸水后变成CoCl2•xH2O 119g.
(1)水合物中x= .
(2)若该化合物中Co2+配位数为6,而且经定量测定得知内界和外界各占有Cl﹣个数为1:1,则其化学式可表示为
原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1.a﹣的电子层结构与氦相同,b和c的次外层有8个电子,c﹣和d+的电子层结构相同.下列叙述错误的是( )
A . 元素的非金属性次序为c>b>a
B . a和其他3种元素均能形成共价化合物
C . d和其他3种元素均能形成离子化合物
D . 元素a、b、c各自最高和最低化合价的代数和分别为0、4、6
下列各组物质气化或熔化时,所克服的微粒间的作用(力),属同种类型的是( )
A . 碘和干冰的升华
B . 二氧化硅和生石灰的熔化
C . 氯化钠和铁的熔化
D . 干冰和氯化铵变成气体
下列变化中,不需要破坏化学键的是( )
A . 氯化氢气体溶于水
B . 氯化钠溶于水
C . 加热氯酸钾使其分解
D . 碘升华
下表物质与其所含化学键类型、所属化合物类型不正确的一组是( )
选 项 | A | B | C | D |
物 质 | Na2O2 | H2O | HCl | NaCl |
所含化学键类型 | 离子键、共价键 | 共价键 | 离子键 | 离子键 |
所属化合物类型 | 离子化合物 | 共价化合物 | 离子化合物 | 离子化合物 |
A . A
B . B
C . C
D . D
下列分子中,所有原子的最外层均为8电子结构的是( )
A . BeCl2
B . H2S
C . NCl3
D . PCl5
下列物质晶体中,同时存在非极性键、极性键和氢键的是( )
A . CaC2
B . H2O
C . C2H4
D . H2O2
NaHSO4溶于水的过程中,发生变化的化学键有( )
A . 离子键
B . 共价键
C . 既有离子键又有共价键
D . 化学键未发生变化
下列过程中,共价键被破坏的是( )
①碘升华②溴蒸气被木炭吸附③酒精溶于水④HCl气体溶于水⑤冰融化⑥NH4Cl受热⑦氢氧化钠熔化⑧(NH4)2SO4溶于水
A . ④⑥
B . ④⑥⑧
C . ①②④⑤
D . ①④⑥⑦
有关晶体的结构如图所示,下列说法中错误的是( )
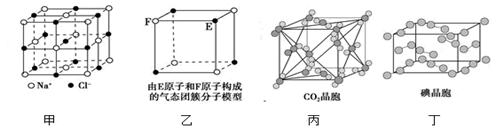
A . 在NaCl晶体(图甲)中,距Na+最近的Cl-围成正八面体
B . 该气态团簇分子(图乙)的分子式为EF或FE
C . 在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻
D . 在碘晶体(图丁)中,存在的作用力有非极性共价键和范德华力
熔融时需要破坏共价键的化合物是( )
A . 冰
B . 石英
C . 金刚石
D . 氢氧化钠
下列叙述正确的有( )个
①用电子式表示MgCl2的形成过程为: ![]()
②两个不同种非金属元素的原子间形成的化学键都是极性键
③离子化合物在熔融状态时能够导电
④含有非极性键的化合物一定是共价化合物
⑤元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
⑥次氯酸的电子式: ![]()
⑦离子化合物中一定含有离子键
A . 1
B . 2
C . 3
D . 4
秦兵马俑展现了我国古代科技文化的伟大成就。近年来人们研究发现秦俑彩绘所用的原料的主要成分为BaCuSi2O6 , 含有微量硫元素等。回答下列问题:
-
(1) 原子轨道是指电子在原子核外的。Cu原子核外电子占据最高能级的符号是,Cu原子核外最外层电子的电子云轮廓图形状为。
-
(2) 硫化硅为白色晶体,分子式为SiS2 , 遇水分解为SiO2及H2S气体,分解反应中所涉及的
所有元素的电负性由大到小的顺序为(填元素符号);SiS2的结构与CS2类似,则SiS2分子的空间构型为。
-
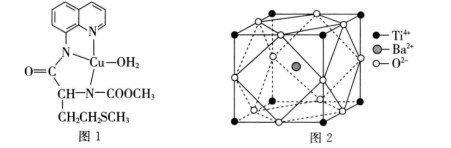
(3) 一种含Cu、S元素的有机物的结构简式如图1所示,该有机物中存在的作用力类型有 (填标号),N原子的杂化方式为。
a.极性键 b.离子键 c.非极性键 d.配位键 e.金属键
-
(4) TiO2与BaCO3一起熔融可制得钛酸钡(BaTiO3),晶胞结构如图2所示(O2−均与Ti4+、Ba2+相接触),已知O2−的半径为xpm,晶胞边长为ypm,则Ti4+、Ba2+的半径分别为pm、pm。
铝是地壳中含量最丰富的金属元素.铝及其化合物在航空、建筑、汽车等工业领域有着重要的应用.工业上以冰晶石为助熔剂电解熔融氧化铝冶炼铝.请根据物质结构与性质的相关知识回答下列问题:
-
(1)
 化学键中离子键的百分数为41%,则
化学键中离子键的百分数为41%,则  应作为晶体(填晶体类型)来处理.
应作为晶体(填晶体类型)来处理.
-
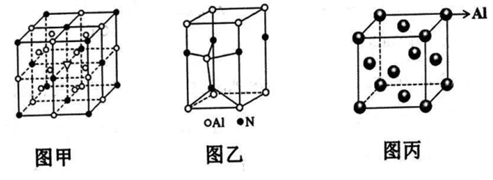
(2) 冰晶石
 能电离产生两种离子,晶体结构如图甲,“●”位于顶点和面心,“○”位于棱的中点和小立方体的体心,则大立方体的体心“
能电离产生两种离子,晶体结构如图甲,“●”位于顶点和面心,“○”位于棱的中点和小立方体的体心,则大立方体的体心“  ”所代表的微粒是.
”所代表的微粒是.
-
(3) 氯化铝的熔点为194℃,易升华,氯化铝属于晶体(填晶体类型).氯化铝常以二聚体的形式存在其结构模型为
 ,一个二聚体中含有配位键个,铝原子的杂化方式为.
,一个二聚体中含有配位键个,铝原子的杂化方式为.
-
(4)
 在一定条件下可制得熔点和硬度都很高的
在一定条件下可制得熔点和硬度都很高的 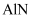 晶体,晶胞结构如图乙所示,则一个晶胞中含有个N原子,
晶体,晶胞结构如图乙所示,则一个晶胞中含有个N原子, 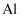 的配位数为.
的配位数为.
-
(5) 金属铝的晶胞如图丙所示:晶胞边长为
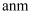 .设阿伏加德罗常数的值为
.设阿伏加德罗常数的值为 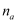 ,则
,则 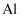 晶体的密度为
晶体的密度为 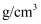 .
. 
La2CuO4在传感器、汽车尾气催化净化、氮氧化物催化消除、中温固体氧化物燃料电池等领域具有良好的应用前景,回答下列问题:
-
(1) 基态Cu原子的核外电子排布式为。
-
(2) 缩二脲[HN(CONH2)2]是一种有机化合物,分子中氮、碳的杂化类型分别是、。1 mol缩二脲中含有σ键的数目为,缩二脲能与Cu2+形成稳定离子,其原因是。
-
(3) 以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系La2CuO4的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。
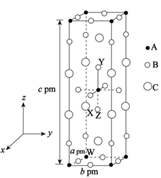
分数坐标
原子
x
y
z
W
0
0
0
X
0
0

Y


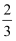
①B原子代表,C原子代表,与A原子距离最近的氧原子个数为。
②Z用分数坐标表示为。
③设阿伏加德罗常数的值为NA , 则La2CuO4的密度是g·cm-3(列出计算表达式)。
据文献报道:Pd-Mg/SiO2催化某反应的一种反应机理如图所示。下列说法错误的是( )
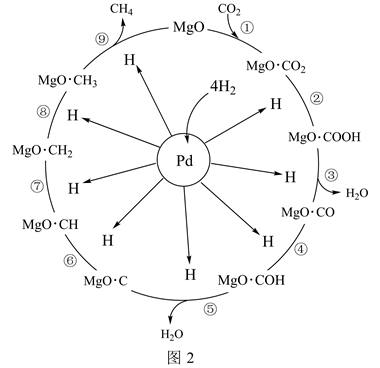
A . 该反应可消耗CO2产生清洁燃料CH4
B . H2在Pd催化剂的表面断裂H-H键
C . 该催化循环CO2变成了含镁的化合物
D . 使用催化剂可以大大降低该反应的活化能使反应快速进行
下列含有非极性键的化合物是( )
A .  B .
B .  C .
C . 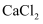 D .
D . 
 B .
B .  C .
C . 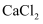 D .
D . 
下列有关晶体的说法正确的是( )
A . 任何晶体中都存在化学键
B . 固体SiO2一定是晶体
C . 分子晶体中共价键的键能越大,该分子晶体的熔点和沸点一定也越高
D . X射线衍射法是区分晶体及非晶体的最可靠的科学方法
下列有关叙述错误的是( )
A . N原子的第一电离能大于О原子
B . HF的热稳定性和沸点均大于 C .
C .  和
和 化学键类型相同
D . BN和SiC熔化克服的作用力相同
化学键类型相同
D . BN和SiC熔化克服的作用力相同
 C .
C .  和
和 化学键类型相同
D . BN和SiC熔化克服的作用力相同
化学键类型相同
D . BN和SiC熔化克服的作用力相同
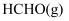 与
与 在催化剂
在催化剂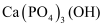 (简写为HAP)表面催化生成
(简写为HAP)表面催化生成 和
和 的历程示意图如下。已知该反应在一定条件下能自发进行。下列说法正确的是 ( )
的历程示意图如下。已知该反应在一定条件下能自发进行。下列说法正确的是 ( )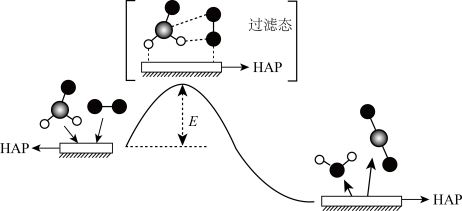
A . E=反应物的键能总和-生成物的键能总和
B . 羟基磷灰石(HAP)的作用是减小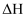 , 加快反应速率
C . 反应过程中既有极性键生成,也有非极性键生成
D . 反应
, 加快反应速率
C . 反应过程中既有极性键生成,也有非极性键生成
D . 反应 的
的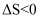
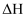 , 加快反应速率
C . 反应过程中既有极性键生成,也有非极性键生成
D . 反应
, 加快反应速率
C . 反应过程中既有极性键生成,也有非极性键生成
D . 反应 的
的
最近更新
- 婆罗门编造说:从造物神的嘴演化出婆罗门,从手生出刹帝利,从腿生出吠舍,从脚生出首陀罗。这就给种姓制度罩上神圣的色彩。该制
- 下列关于人体血糖平衡调节的叙述中,正确的是
- 罗马法是世界上内容最丰富、体系最完善、对后世影响最广泛的古代法律。罗马法中所蕴含的某种法律观念,具有超越时间、地域与民族
- I wonder what it feels like to be one of really ric
- 某班同学对南昌市市民对于“八一南昌起义”这件事的了解程度进行调查,他们将了解程度分为“清楚”、“了解”、“知道”“不知道
- 右图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列说法中不正确的是A.该实验证明空气中
- 近地人造卫星1和2绕地球做匀速圆周运动的周期分别为T1和T2,设在卫星1、卫星2各自所在的高度上的重力加速度大小分别为g
- 蒸馒头、炸油条时常用到一种白色物质,它既能中和面粉发酵过程产生的酸,又能起发泡作用,这种白色物质是( ) A.NaO
- ---It is said that a new zoo will bebuilt in our town. ---I’
- 阅读下列材料: 材料一 造纸术经阿拉伯人引入葡萄牙,在13世纪到达西方,廉价耐用的纸张很快取代了欧洲中世纪长期使用的书
- 由MgO、MgSO4和MgHPO4组成的混合物中镁元素的质量分数为33%,则混合物中氧元素的质量分数为_________
- (8分)被誉为东昌三宝之首的铁塔,始建于北宋时期,是我市现存的最古老的建筑.铁塔由塔身和塔座两部分组成.为了测得铁塔的高
- 反应NH4HS(s) NH3+H2S(g)在一定温度下达到平衡。下列各种情况下,不能使平衡发生移动的是( ) ①
- 阅读下面材料,按要求作文:我们经常说“沉默是金”,仔细想想,“沉默”的内含极其丰富,其寓意也发人深省。比如,对于思想者而
- 在标准状况下,2.24L的某气态烷烃和具有一个双键的烯烃的混合气体完全燃烧后,将高温下产生的气体缓慢通过浓硫酸,浓硫酸增
- “削峰填谷”调节分配是个人所得税的一项基本功能。我国新的个人所得税法实施以来,6 000万人免交个税。此举( )
- 20世纪,美、英政府经济职能经历了几次转变,以下比喻体现了70年代以来,两国政府经济职能定位的是
- 下列符号既可表示一个原子,又可表示一种元素,还能表示一种物质的是( ) A、H2 B、2N C、Cu
- 写出下列物质的电离方程式: H2SO4 Ba(OH)2 Na2SO4.
- .在20℃时一刚性容器内部有一不漏气且可左右滑动的活塞将容器分隔成左、右室两室。左室充入N2,右室充入H 2和O 2的混



