3.1 原子间的相互作用 知识点题库
下列说法中,正确的是:( )
A . 相邻的原子之间的相互作用叫做化学键
B . 金属和非金属元素的相互化合,都能形成离子键
C . 第三周期主族元素中原子半径最小的是氯原子,离子半径最小的是铝离子
D . 甲元素原子半径比乙元素原子半径大,则甲的离子半径一定比乙的离子半径大。
下列各组物质中,化学键类型完全相同的是( )
A . SiO2和H2O
B . SO2和Na2O2
C . NaCl和HCl
D . AlCl3和KCl
固体A的化学式为NH5 , 它的所有原子的最外层都符合相应稀有气体原子的最外层电子结构,则下列有关说法中,不正确的是( )
A . 1mol NH5中含有5NA个N﹣H键(NA表示阿伏加德罗常数)
B . NH5中既有共价键又有离子键,它属于离子化合物
C . NH5的电子式为: 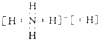 D . 它与H2O反应的化学方程式为:NH5+H2O═NH3•H2O+H2↑
D . 它与H2O反应的化学方程式为:NH5+H2O═NH3•H2O+H2↑
下列有关化学键的叙述,正确的是( )
A . 离子化合物中一定含有离子键
B . 单质分子中一定不存在化学键
C . 含有非极性键的分子一定是单质分子
D . 含有共价键的化合物一定是共价化合物
共价键、金属键、离子键和分子间作用力都是构成物质的粒子间的不同作用,含有以上所说的两种作用的晶体是( )
A . SiO2晶体
B . CCl4晶体
C . MgCl2晶体
D . Al2O3晶体
下表是元素周期表的一部分,针对表中的①~⑨九种元素,填写下列空白:
|
族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
|
二 |
① |
② |
③ |
|||||
|
三 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|||
|
四 |
⑨ |
-
(1) 在这些元素中,化学性质最不活泼的是(填具体元素符号,下同)。
-
(2) 在最高价氧化物的水化物中,酸性最强的化合物的化学式是,碱性最强的化合物的电子式是,其含有的化学键类型
-
(3) 最高价氧化物是两性氧化物的元素是;写出它的氧化物与盐酸反应的离子方程式
-
(4) 写出元素③的氢化物的电子式
-
(5) 写出④的单质与水反应的离子方程式
某金属有机多孔材料(MOFA)在常温常压下对CO2有超强的吸附能力,并能高效催化CO2与环氧乙烷衍生物的反应,其工作原理如图。下列说法不正确的是( )
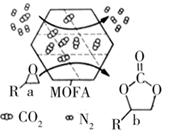
A . 该材料的吸附作用具有选择性
B . 该方法的广泛使用有助于减少CO2的排放
C . 在生成化合物b的过程中,有极性共价键形成
D . 其工作原理只涉及化学变化
下列有关说法错误的是( )
A . 一定条件下石墨转化为金刚石反应吸热说明石墨比金刚石稳定
B . 化学反应必然伴随发生能量变化
C . 化学键是一种作用力
D . 不同元素组成的多原子分子中的化学键一定是极性键
丙烷的一溴代反应产物有两种:  和
和 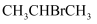 ,部分反应过程的能量变化如图所示(
,部分反应过程的能量变化如图所示( 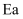 表示活化能)。下列叙述错误的是( )
表示活化能)。下列叙述错误的是( )
 和
和 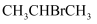 ,部分反应过程的能量变化如图所示(
,部分反应过程的能量变化如图所示( 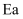 表示活化能)。下列叙述错误的是( )
表示活化能)。下列叙述错误的是( ) 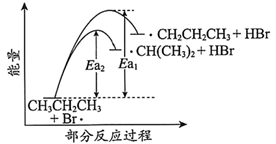
A . 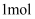 丙烷中有
丙烷中有 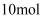 共价键
B .
共价键
B .  与
与 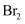 的反应涉及极性键和非极性键的断裂
C .
的反应涉及极性键和非极性键的断裂
C .  D . 比较
D . 比较 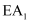 和
和  推测生成速率:
推测生成速率: 
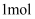 丙烷中有
丙烷中有 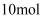 共价键
B .
共价键
B .  与
与 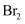 的反应涉及极性键和非极性键的断裂
C .
的反应涉及极性键和非极性键的断裂
C .  D . 比较
D . 比较 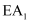 和
和  推测生成速率:
推测生成速率: 
下列说法中正确的是( )
A . 乙烯中 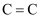 的键能是乙烷中
的键能是乙烷中 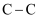 的键能的2倍
B . 氮气分子中含有1个
的键能的2倍
B . 氮气分子中含有1个 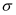 键和2个π键
C .
键和2个π键
C . 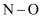 键的极性比
键的极性比 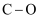 键的极性大
D .
键的极性大
D .  中4个
中4个 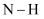 键的键能不相同
键的键能不相同
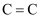 的键能是乙烷中
的键能是乙烷中 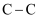 的键能的2倍
B . 氮气分子中含有1个
的键能的2倍
B . 氮气分子中含有1个 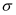 键和2个π键
C .
键和2个π键
C . 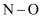 键的极性比
键的极性比 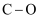 键的极性大
D .
键的极性大
D .  中4个
中4个 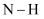 键的键能不相同
键的键能不相同
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。
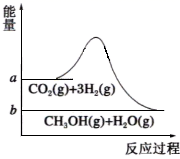
请回答下列问题:
-
(1) 观察图象可知上述反应过程中,断裂反应物中的化学键吸收的总能量(填“大于”“小于”或“等于”)形成生成物中的化学键释放的总能量。
-
(2) 甲醇的结构类似于乙醇,试写出甲醇的结构式:。甲醇分子中的化学键类型是(填“离子键“共价键”)。
-
(3) 科研人员开发出一种新型甲醇燃料电池。其电解质溶液是KOH溶液,在该电池的负极发生反应的物质是,发生的是(填"氧化"或"还原")反应。
-
(4) 欲使合成甲醇的化学反应速率加快,请写出两条措施:;
-
(1) 元素的第一电离能:AlSi(填“>”或“<”),按电负性由大到小的顺序排列N、O、F。
-
(2) 基态Mn2+的核外电子排布式为。
-
(3) 硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是。

-
(4) 硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:
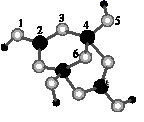
①在Xm-中,硼原子轨道的杂化类型有;配位键存在于原子之间(填原子的数字标号)。
②硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有(填序号)。
A.离子键 B.共价键 C.金属键 D.范德华力E.氢键
现有下列7种与生产生活相关的有机物,请回答下列问题:
①  ②
② 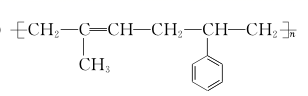 ③
③ 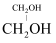 ④
④  ⑤
⑤ 
-
(1) 有机物是含碳的化合物,基态C原子中电子占据的最高能层符号是: ;
-
(2) 与①互为同系物的为 (填序号);
-
(3) ②的单体结构简式为: 、 ;
-
(4) ④中σ键和π键个数之比为 ;
-
(5) ⑤分子中O-C-H键角 (填“大于”“等于”或“小于”)甲醛分子内的O-C-H键角。
在下列各组物质中,化学键类型完全相同的是( )
A . NH4Cl和NaOH
B . H2O2和Na2O2
C . CO2和Ar
D . KCl和Na2O
我国的超级钢研究已居于世界领先地位,这种超级钢中含Mn10%、C0.47%、Al2%、V0.7%,其强度很大,在应用时能够实现钢板的轻薄化。回答下列问题:
-
(1) 基态Mn原子和V原子未成对电子数之比为。
-
(2) 下列状态的铝中,电离最外层一个电子所需能量最大的是___________。A . [Ne]3s2 B . [Ne]3s23p1 C . [Ne]3s24s1 D . [Ne]3s1
-
(3) NH3的VSEPR模型的名称是,写出一种和NH3互为等电子体的阳离子的化学式。分子中的大π键可用符号∏
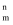 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为∏
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为∏  ),则平面分子
),则平面分子 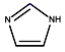 中的大π键应表示为。
中的大π键应表示为。
-
(4) 谷氨酸(HOOC-CH(NH2)-CH2-CH2-COOH)的钠盐-谷氨酸钠(C5H8NO4Na)是味精的主要成分,谷氨酸分子中C原子的杂化方式为 ,C原子与O原子所形成的化学键中σ键与π键的数目比n(σ)∶n(π)= ,π键的特征是两块电子云呈对称。
-
(5) Al2O3、N2、CO的沸点从高到低的顺序为。原因是 。
-
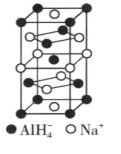
(6) 已知NaAlH4晶胞结构如图所示,它由两个正六面体叠加而成,Na+的配位数为。已知正六面体的棱长anm,NA为阿伏加德罗常数的值,则NaAlH4晶体的密度是 g• cm-3 (列出计算式)。
下列含有极性共价键的离子化合物化合物是( )
A . Na2O2
B . NaOH
C . Br2
D . NaCl
硫铁矿(主要成分FeS2)是接触法制硫酸的主要原料,接触法制硫酸的生产原理分三步。
I.4FeS2+11O2  2Fe2O3+8SO2;
2Fe2O3+8SO2;
II.2SO2+O2 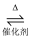 2SO3;
2SO3;
III.SO3+H2O=H2SO4。
回答下列问题:
-
(1) ①基态O原子的核外电子排布式为;基态Fe原子共有种运动状态不同的电子。
②Fe2+形成的配合物亚铁氰化钾(K4[Fe(CN)6])又称黄血盐,可用于检验Fe3+。写出两种与CN-互为等电子体的分子的化学式:;含有12molσ键的K4[Fe(CN)6]的物质的量为mol。
③已知Fe2+半径为61pm,Co2+半径为65pm,则在隔绝空气条件下分别加热FeCO3和CoCO3 , FeCO3受热分解温度(填“低于”或“高于”)CoCO3。
-
(2) ①H2SO4的酸性强于H2SO3的酸性的原因是。
②SO2中S原子的杂化方式为;SO3的立体构型为。第一电离能:SO(填“>”或“<”)。
-
(3) FeS2晶体的晶胞结构如图所示。
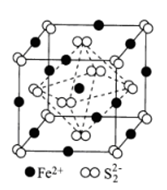
①FeS2晶体中距离Fe2+最近的Fe2+的数目为。
②FeS2晶体的晶胞参数为anm,密度为ρg·cm-3 , 阿伏加德罗常数的值为NA , 则FeS2的摩尔质量M=g·mol-1(用含a、ρ、NA的代数式表示)。
下列各组物质,化学键类型相同的是( )
A . HCl、NaCl
B . KI、CCl4
C . NaOH、H2O2
D . CO2、SO2
A、B、D、E、G为原子序数依次增大的五种短周期主族元素,非金属元素A最外层电子数与其周期数相同,B原子的最外层电子数是其所在周期数的2倍。B单质在D单质中充分燃烧能生成其最高价化合物 ,
, 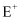 与
与 具有相同的电子层结构。A单质在G单质中燃烧,产物溶于水得到一种强酸。回答下列问题:
具有相同的电子层结构。A单质在G单质中燃烧,产物溶于水得到一种强酸。回答下列问题:
 ,
, 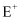 与
与 具有相同的电子层结构。A单质在G单质中燃烧,产物溶于水得到一种强酸。回答下列问题:
具有相同的电子层结构。A单质在G单质中燃烧,产物溶于水得到一种强酸。回答下列问题:
-
(1) G在元素周期表中的位置是,
 的电子式为;
的电子式为;
-
(2) D、E、G分别形成的简单离子的半径由大到小的顺序为(用离子符号表示);
-
(3) 由A、D、E三种元素组成的化合物含有的化学键类型为;
-
(4) 设计一个简单的实验证明G和B的非金属性强弱:(用化学方程式表示)。
下列关于化学键的说法中错误的是( )
A . 化学键分为离子键、共价键、氢键等
B . 相邻的阳离子和阴离子之间强烈的相互作用称为离子键
C . 干冰晶体中存在共价键和分子间作用力
D . 金刚石晶体中只存在共价键,不存在分子间作用力
最近更新
- 已知定义在区间[0,3]上的函数f(x)=kx2-2kx的最大值为3,那么实数k的取值范围为________.
- 一次晚会上一名演员身穿蓝色裤子和白色衬衫,当舞台上只有红光时,观众看到的是 色的裤子, 色的衬
- “Simon wants to know if the Class 3 students___hiking tomor
- When you wave to a friend, you are using body language.When
- 下图中表示转录过程的是
- 已知2tanα·sin α=3,的值是________.
- 唐朝诗人王维名句:“渭城朝雨浥轻尘,客舍青青柳色新。劝君更尽一杯酒,西出阳关无故人”。诗中 “君”前往的地区是 A.今陕
- The gentleman put on his dark glasses and hat, ______ goodby
- 2010年11月8日,国家国防科技工业局首次公布“嫦娥二号”卫星传回的月球虹湾区域局部影像图。影像图的传回,标志着“嫦娥
- 《次北固山下》描写时序交替中的景物,暗示时光流逝,蕴含自然哲理的诗句是:
- 已知命题(1) ,使成立;(2) ,使 成立;(3) ,,有成立; (4)若是的内角,则“” 的充要条件是“”.其中正
- 画出图中沿曲线ABCDE运动的物体在A、B、C、D、E各点的速度方向.【1】
- 已知f(x)=x+3x2+5x3+…+(2n-1)xn,试比较f()与3的大小.
- 根据下面提供的情境回答问题 上课铃声一停,语文老师走进教室,看见坐在第一排的罗小威,就停下脚步,微笑着说:“小威
- 硫代硫酸钠(Na2S2O3)俗称保险粉,可用于照相业作定影剂,也可用于纸浆漂白 作脱氯剂等。实验室可通过如下反应制取:2
- 十九大报告中提出,到本世纪中叶把我国建成和谐美丽强国……下列做法不利于绿色发展方式和生活方式的是
- 16.补写出下列句子中的空缺部分(5分) (1)在辛弃疾《永遇乐·京口北固亭怀古》中,表达了辛弃疾对时光流逝、美好不再的
- 关于两个三角洲的叙述,正确的是( ) A.甲图是珠江三角洲 B.乙图有京沪
- 阅读材料,完成下列各题。 材料一 “蓝蓝的天空,青青的湖水,绿绿的草原。”历史上图QZ10所示区域曾是一片水草丰美的地
- 标准的PCR过程一般分为变性、复性、延伸三大步,这三大步需要的温度依次是( ) A.95℃、55℃、72℃



