第4节 海水中的化学元素 知识点题库
已知:氧化性:IO3﹣>Fe3+>I2还原性:S2O32﹣>I﹣
反应式:3I2+6OH﹣═5I﹣+IO3﹣+3H2O,KI+I2⇌KI3
-
(1) 某学习小组对加碘盐进行了如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+).用适量蒸馏水溶解,并加稀硫酸酸化,将所得溶液分3份:第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显示淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入足量的KIO3固体后,滴加淀粉试剂,溶液不变色.
①该红色物质是 (用化学式表示);CCl4中显示紫红色的物质是 (用电子式表示).
②第二份试液中加入足量KI固体后,反应的离子方程式为
-
(2) KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失.写出潮湿环境中KI与氧气反应的化学方程式: .
将I2溶于KI溶液,在低温条件下,可制得KI3・H2O.该物质作为食盐加碘剂是否合适?
(填“是”或“否”),并说明理由:
-
(3) 为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失.下列物质中有可能作为稳定剂的是A . Na2S2O3 B . AlCl3 C . Na2CO3 D . NaNO2
-
(4) 对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂.请设计实验方案,检验该加碘盐中的Fe2+:
-
(1) 工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为.
-
(2) 漂白粉的主要成分是(填化学式),有效成分是(填化学式).
-
(3) 漂白粉溶于水后,受空气中的CO2作用,即产生漂白、杀菌作用,离子方程式为.
-
(1) 该消毒液可用NaOH溶液吸收Cl2制备,化学方程式为.
-
(2) 该消毒液的pH约为12,离子方程式为
-
(3) 向FeSO4溶液中滴入少量该溶液,溶液颜色变成棕黄色,反应的离子方程式为
-
(4) 该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险.每产生1mol Cl2(标准状况下),转移电子个数约为.
Cl2+H2O⇌HCl+HClO K=4.5×10﹣4
次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大).但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其它性能优越的消毒产品所替代.请回答:
-
(1) 氯碱工业生产氯气的化学方程式为.
-
(2) 84消毒液(主要成分为NaClO)与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为.
-
(3) 二氧化氯是一种高效、广谱、安全的杀菌、保鲜剂.我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为.
-
(4) 一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧化性强弱的微型装置(如图).
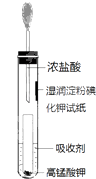
①下列溶液能吸收Cl2的是(填字母序号).
A.饱和食盐水 B.饱和Na2SO3溶液
C.饱和NaOH溶液 D.浓硫酸
②能说明Cl2的氧化性强于I2的实验现象是.
-
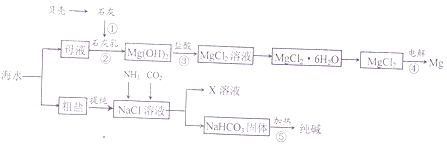
(1) 在上述反应①~⑤中,没有涉及的化学反应类型是 .A . 分解反应 B . 化合反应 C . 复分解反应 D . 置换反应
-
(2) 写出反应③的离子方程式.
-
(3) 粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:
①溶解;
②依次加入过量的BaCl2溶液、NaOH溶液、;
③过滤;
④;
⑤蒸发结晶.
其中加入过量氯化钡溶液的目的是.
-
(4) X溶液中的主要阳离子是Na+和.
-
(5) 检验纯碱样品中是否含NaCl应选用的试剂是.
离子 | Na+ | Mg2+ | Cl﹣ | SO42﹣ |
浓度/(g•L﹣1) | 63.7 | 28.8 | 144.6 | 46.4 |
再利用浓海水提镁的一段工艺流程如下图:
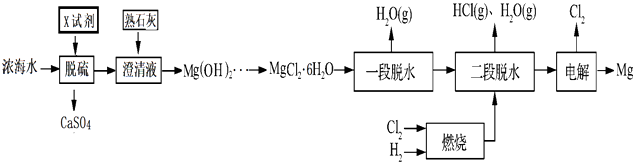
请回答下列问题
-
(1) 浓海水主要含有的四种离子中物质的量浓度最小的是.在上述流程中,可以循环使用的物质是.
-
(2) 在该工艺过程中,X试剂的化学式为.
-
(3) “一段脱水”目的是制备MgCl2•2H2O;“二段脱水”的目的是制备电解原料.若将MgCl2•6H2O直接加热脱水,则会生成Mg(OH)Cl.若电解原料中含有Mg(OH)Cl,电解时Mg(OH)Cl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率.生成MgO的化学方程式为.
-
(4) 若制得Mg(OH)2的过程中浓海水的利用率为80%,由Mg(OH)2至“二段脱水”制得电解原料的过程中镁元素的利用率为90%,则1m3浓海水可得“二段脱水”后的电解原料质量为g.
-
(5) 以LiCl﹣KCl共熔盐为电解质的Mg﹣V2O5电池是战术导弹的常用电源,该电池的总反应为:Mg+V2O5+2LiCl MgCl2+V2O4•Li2O 该电池的正极反应式为.
-
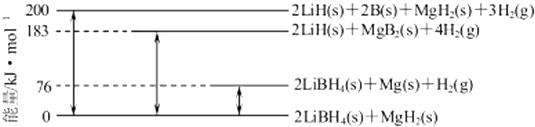
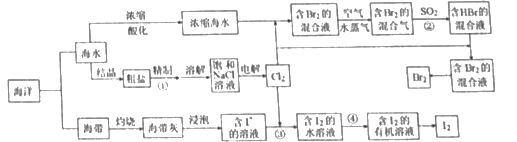
(6) Mg合金是重要的储氢材料.2LiBH4/MgH2体系放氢焓变示意图如下,则:
Mg(s)+2B(s) MgB2(s)△H=.
-
(1) 卤族元素在元素周期表中的位置是。
-
(2) ①中将粗盐精制的过程中,为除去其中的 Ca2+、 Mg2+、 SO42- , 所加以下四种试剂的先后顺序是(填序号)。
A 盐酸 B Na2CO3 溶液 C NaOH 溶液 D BaCl2 溶液
-
(3) ②中发生的化学方程式是。
-
(4) ③中发生的离子方程式是。
-
(5) ④的操作名称是。
(NaHCO3的制备)
反应原理:NH3+NaCl+CO2+H2O=NH4Cl+NaHCO3↓
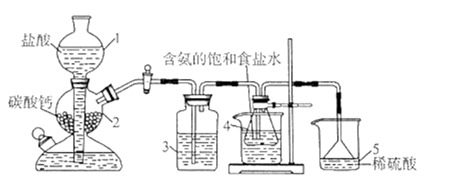
反应装置:
-
(1) 启普发生器中发生的离子反应方程式为,如果上述装置中导管被堵塞,启普发生器中观察到的现象是。
-
(2) 仪器3中盛装的试剂是;已知常温,NaCl的溶解度为35.9g,仪器4中含氨的饱和食盐水的配制方法是将20.0mL浓氨水与8.0gNaCl混合振荡过滤,试推测过滤除去的物质为。
-
(3) 观察仪器4中CO2流速的方法是,仪器5中试剂的作用是。
-
(4) 反应结束后,对仪器4进行冷却并趁冷过滤其中的悬浊液,“趁冷”的目的是。
-
(5) (Na2CO3的制备)
将(4)所得固体转移至蒸发皿中加热得到Na2CO3;请设计简单实验证明NaHCO3固体已分解完全。
-
(6) (NH4Cl的制备)
向(4)所得母液中加入两种物质并降温,NH4Cl会逐步结晶析出,所加物质的名称是,过滤NH4Cl晶体后的滤液可以再次循环使用。
-
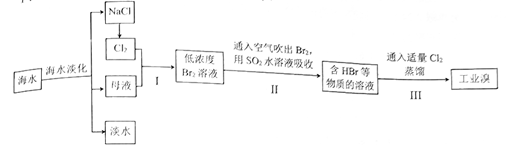
(1) Ⅰ.工业海水淡化及从海水中提取溴的过程如下:
请回答下列问题:
历史最久,技术和工艺也比较成然,但成本较高的海水淡化的方法是法。
-
(2) 从海水中可以得到食盐,为了除去粗盐中的Ca2+、Mg2+、
 ,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液。正确的操作顺序是______(填字母)。
A . ⑤④②③① B . ④①②⑤③ C . ②⑤④①③ D . ②④⑤①③
,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液。正确的操作顺序是______(填字母)。
A . ⑤④②③① B . ④①②⑤③ C . ②⑤④①③ D . ②④⑤①③ -
(3) 步骤Ⅰ中已获得Br2 , 步骤Ⅱ中又将Br2还原为Br- , 其目的为。
-
(4) 步骤Ⅱ用SO2水溶液吸收Br2 , 反应的离子方程式为。
-
(5) 从理论上考虑,下列物质的溶液也能与Br2反应的是______(填字母)。A . NaCl B . Na2CO3 C . Na2SO3 D . FeCl3
-
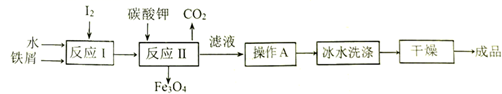
(6) Ⅱ.金属矿物冶炼得到的铁屑和海带中提取的碘可以用于生产KI,工艺流程如图所示:
请回答下列问题:
KI的溶解度随温度变化比较大,操作A包括、、过滤。
-
(7) 用冰水洗涤的目的是除去附着在KI表面的可溶性杂质,同时。
-
(8) 反应Ⅰ生成了铁与碘的化合物X,若X中铁元素与碘元素的质量比为21∶127,则X的化学式为。
-
(9) 写出反应Ⅱ的化学方程式。
-
(1) 某厂废水中含KCN,其浓度为650mg/L。现用氯氧化法处理,发生如下反应:KCN+2KOH+Cl2=KOCN+2KCl+H2O。投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平下列化学方程式:KOCN+KOH+Cl2—CO2+N2+KCl+H2O,。
-
(2) 若处理上述废水100L,使KCN完全转化为无毒物质,至少需要投放液氯多少克?
-
(3) 氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素,它们阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-。试写出:
①(CN)2与KOH溶液反应的化学方程式:。
②在NaBr和KSCN的混合溶液中滴加少量(CN)2 , 反应的离子方程。
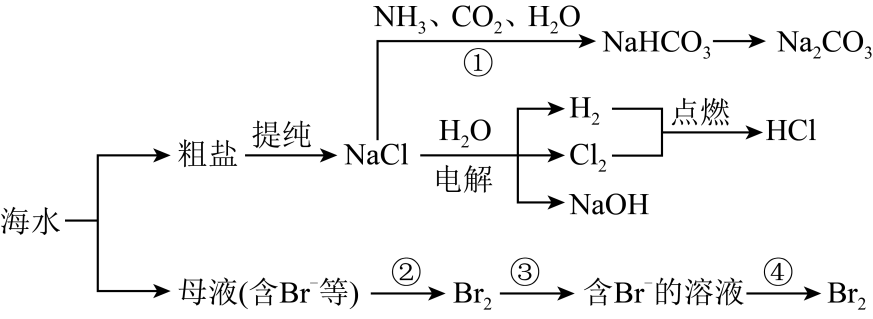
下列说法正确的是( )
 等)提纯所加试剂顺序为NaOH→Na2CO3→BaCl2→过滤→HCl
B . 过程①为了提高产率一般先通CO2再通NH3
C . 用澄清石灰水可以鉴别NaHCO3和Na2CO3溶液
D . 过程②③④可以达到富集溴的目的
等)提纯所加试剂顺序为NaOH→Na2CO3→BaCl2→过滤→HCl
B . 过程①为了提高产率一般先通CO2再通NH3
C . 用澄清石灰水可以鉴别NaHCO3和Na2CO3溶液
D . 过程②③④可以达到富集溴的目的
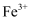 能与
能与 反应生成
反应生成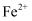 和
和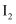 , 取10mL0.1mol/LKI溶液,滴加0.1mol/L
, 取10mL0.1mol/LKI溶液,滴加0.1mol/L 溶液3~4滴,充分反应后,继续加入2mL
溶液3~4滴,充分反应后,继续加入2mL 振荡,静置,下列有关该实验的说法正确的是( )
振荡,静置,下列有关该实验的说法正确的是( )
 层溶液呈紫红色
B . 取少量上层溶液,滴加
层溶液呈紫红色
B . 取少量上层溶液,滴加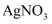 溶液,只有白色沉淀生成
C . 该实验中KI与
溶液,只有白色沉淀生成
C . 该实验中KI与 反应后(未加
反应后(未加 ),溶液中只存在
),溶液中只存在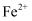 、
、 、
、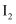 微粒
D . 取少量上层溶液,滴加KSCN溶液,若溶液显红色,则表明该反应存在化学反应限度
微粒
D . 取少量上层溶液,滴加KSCN溶液,若溶液显红色,则表明该反应存在化学反应限度
- A Brown University sleep researcher hassome advice for peopl
- 第三部分:阅读理解(共两节 第一节20小题,每小题2分,第二节5小题,每小题1分,满分45分) 阅读下列短文,从每题所给
- 他被誉为旧时代的最后一位诗人,同时又是新时代的最初一位诗人。他是 A.但丁 B.达·芬奇 C.
- 我们已经知道,铁在潮湿的空气里易生锈,设计一组实验(也可用图表示)来证明铁的生锈,既不是单纯水的作用也不单纯是空气中氧气
- 在FeCl3和BaCl2的酸性混合溶液中通入SO2气体,生成的白色沉淀是A BaSO4 B FeS
- 如图:直线y=x+3与坐标轴交于A、B两点,与过C、D的直线交于点E.已知OC:OD=2:1,CD= (1)求直线CD的
- 自《中华人民共和国村民委员会组织法》实施后,越来越多地区的农民群众直接投票选举村委会干部,实现了“自己的干部自己选,自己
- 在△ABC中,点M,N满足则x=________;y=________.
- “一个以议会形式粉饰门面,混杂着封建残余、已经受到资产阶级影响、按官僚制度组织起来、并以警察来保卫的、军事专制制度的国家
- 下列各句中,标点符号使用正确的一句是 () A.“小公民议事厅”是山东省青岛市
- Thisbook is said_____ into several foreign languages last ye
- 函数 的最小正周期为,则函数的 一个单调增区间是
- 请看下图,在这一购物流程中淘宝网购物流程图 A.货币执行了流通手段职能 B.货币充当了价值尺度职能 C.货币表现了
- 以下关于ATP和酶的叙述中正确的是 A.具有催化功能的酶都由氨基酸通过脱水缩合形成 B.ADP合成ATP时,能量储存在远
- 下图是表示某产业在世界上的迁移过程。回答 导致该产业迁移变
- 材料一:降水变率就是用以表示降水量变动程度的统计量,一般可分为绝对变率和相对变率。降水绝对变率是指某地实际降水量与同期多
- We are going tothe party ________next week. A.×
- 某中学生写作文时,用邻居的真实姓名,虚构邻居家重男轻女的情节,作文被某晚报选登,造成了较恶劣影响。该学生的行为主要侵犯了
- 对以下实验的实验现象描述,不正确的是 ( )A.铁丝在氧气中燃烧火星四射,生成黑色固体B.硫在空气中燃烧生成具有刺激性气
- 民族区域自制度是我国的基本政治制度。国务院公布的《全国年节及纪念日放假办法》第四条规定,少数民族习惯的节日,由各少数民族



