第4节 海水中的化学元素 知识点题库
下列说法中正确的是( )
A . 食品添加剂就是为增强食品的营养而加入的物质
B . 只有不法商贩才使用食品添加剂
C . 味精是食品添加剂,而碘盐中的“碘”不是添加剂
D . 在限量范围内使用食品添加剂不会对人体造成危害
三氯化氮分子中每个原子的最外层均达到8电子稳定结构,且氮与氯的共用电子对偏向氮原子.则下列关于三氯化氮的叙述正确的是( )
A . NCl3为非极性分子
B . NCl3跟水反应的产物为NH3和HClO
C . NCl3跟水反应生成NH4Cl、O2和Cl2
D . 在NCl3分子中N为+3价,跟水发生水解反应的产物是HNO2和HCl
在温度t1和t2下,卤素单质X2(g)和H2反应生成HX的化学平衡常数如下表,仅根据下表数据不能判断的是( )
化学方程式 | K(t1) | K(t2) |
F2+H2⇌2HF | 1.8×1036 | 1.9×1032 |
Cl2+H2⇌2HCl | 9.7×1012 | 4.2×1011 |
Br2+H2⇌2HBr | 5.6×107 | 9.3×106 |
I2+H2⇌2HI | 43 | 34 |
A . 已知t2>t1 , HX的生成反应为放热反应
B . 在相同条件下,X2平衡转化率:F2>Cl2
C . X2与H2反应的剧烈程度随着原子序数递增逐渐减弱
D . HX的稳定性:HBr>HI
用飞秒激光技术研究了氰化碘的分解反应:ICN→I+CN,发现该反应可在200飞秒内完成.已知(CN)2和卤素的性质相似.以下有关ICN的叙述正确的是( )
A . ICN不能和NaOH溶液作用
B . ICN是一种离子化合物
C . ICN可以和NaI作用生成单质碘
D . ICN空气中受热也能发生题中所述分解反应
碘是人体必须的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素.在实验室中,从海藻里提取碘的流程如图1和实验装置如图2:
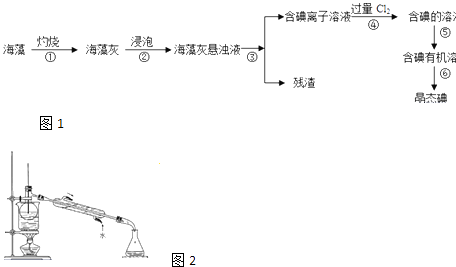
-
(1) 指出上述提取碘的过程中有关实验操作的名称:步骤③,步骤⑤.
-
(2) 写出步骤④对应反应的离子方程式:
-
(3) 提取碘的过程中,可供选择的有机试剂是 (填编号)A . 醋酸 B . 苯 C . 四氯化碳 D . 酒精
-
(4) 为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至⑤,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网、以及必要的夹持仪器和物品,尚缺少的玻璃仪器是.
-
(5) 从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏.指出如图实验装置中存在的错误之处:.
下列有关海水综合利用的说法正确的是( )
A . 电解熔融的氯化镁可制备镁单质和氯气
B . 从海水制食盐主要是通过化学变化完成
C . 电解氯化铝可以制得铝单质和氯气
D . 从海水中提取钠单质只发生物理变化
下列物质与用途对应关系不正确的是( )
选项 | A | B | C | D |
物质 | 单质碘 | 苯甲酸钠 | 聚乙烯 | 二氧化硅 |
用途 | 食盐添加剂 | 食品防腐剂 | 食品保鲜膜 | 光导纤维 |
A . A
B . B
C . C
D . D
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:

-
(1) 为了使MgSO4转化为Mg(OH)2 , 试剂①可以选用,要使MgSO4完全转化为沉淀,加入试剂的量应。
-
(2) 加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是。
-
(3) 试剂②选用;其反应的离子方程式为。
-
(4) 无水MgCl2在熔融状态下,通电后产生镁和氯气,该反应的化学方程式为。
海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
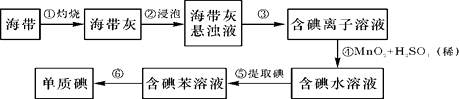
-
(1) 从上述步骤中可知,海带中含有的碘元素的主要存在形式是(填化学式)。
-
(2) 步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A烧杯 B表面皿 C坩埚 D酒精灯 E干燥器
-
(3) 步骤⑥是从含碘苯溶液中分离出单质碘和回收苯,还需经过蒸馏,指列实验装置中的不符合题意之处。
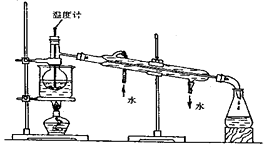
① ;② ;③ ;
进行上述蒸馏操作时,使用水浴的原因是 ;最后晶态碘在里聚集。
-
(4) 步骤④反应的离子方程式是。若用碘盐中的KIO3作氧化剂,在酸性溶液中氧化I— , 写出反应的离子方程式。
-
(5) 检验海带中是否含有碘元素,可以在步骤④后进行,检验时可用的试剂是。
-
(6) 步骤⑤中,某学生选择用苯来提取碘,其实验操作可分解为如下几步:
(A)把盛有溶液的分液漏斗放在铁架台的铁圈中;
(B)把50毫升碘水和15毫升苯加入分液漏斗中,并盖好玻璃塞;
(C)检验分液漏斗活塞和上口的玻璃塞是否漏液;
(D)倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
(E)旋开活塞,用烧杯接收溶液;
(F)将分液漏斗上口倒出上层溶液;
(G)将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔;
(H)静置,分层。
就此实验,完成下列填空:
正确操作步骤的顺序是→→→A→G→→E→F
下列有关物质性质与用途的叙述正确的是( )
A . 浓硫酸具有脱水性,可用作干燥剂
B . NH3极易溶于水,可用作制冷剂
C . 二氧化硫具有漂白性,与氯水混合使用漂白效果更好
D . ClO2具有氧化性,可用于自来水的杀菌消毒
许多国家十分重视海水资源的综合利用,不需要化学变化就能从海水中获得的物质是( )
A . 溴、碘
B . 钠、镁
C . 烧碱、氢气
D . 食盐、淡水
卤族元素包括氯、溴、碘等元素,其中溴和碘在陆地上含量极少,主要存在于海水中。
-
(1) 氯气有毒,一旦泄露会造成对空气的严重污染。工业上常用浓氨水检验氯气管是否漏气。(已知Cl2可将NH3氧化成N2)写出有关的化学方程式 。
-
(2) 亚氯酸钠(NaClO2)是一种漂白剂。已知NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+ 的物质的量 (填相同或不相同),解释其原因是。
-
(3) 从海水中提取溴,一般要经过浓缩、氧化和提取三个步骤。氧化时常用氯气做氧化剂,写出有关的离子方程式。
-
(4) 海带提碘时,由于碘的量较少,在灼烧、溶解之后得到的溶液用硝酸银溶液很难检验。设计一个检验浓液中是否含有碘离子的方法。
工业制备下列物质的方案中正确的是( )
A .  B .
B .  C .
C . 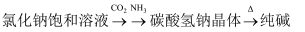 D .
D . 
 B .
B .  C .
C . 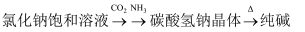 D .
D . 
氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的最初生成物是( )
A . HCl和HIO
B . HI和HClO
C . HClO3和HIO
D . HClO和HIO
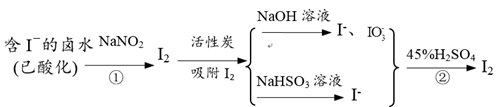
工业上可用NaNO2从含I-的卤水中提取单质碘。流程如下:
-
(1) 酸性条件下,含I-的卤水发生如下反应:
 +I-+_→NO ↑+I2 +_,补充完整方程式并配平:;当有0.75mol I-参与反应时,在标准状况下产生气体的体积是L。
+I-+_→NO ↑+I2 +_,补充完整方程式并配平:;当有0.75mol I-参与反应时,在标准状况下产生气体的体积是L。
-
(2) 上述反应为什么不选用常见的氧化剂氯气,而选择价格并不便宜的NaNO2 , 可能原因是。
-
(3) 从第②步反应后的溶液中提纯I2涉及到的方法可以是(选填编号)。
a.萃取 b.升华 c.纸层析 d.过滤
-
(4) 在富集碘元素过程中,还使用了NaHSO3溶液。该物质既能水解又能电离,设计实验验证其水解程度和电离程度的相对大小。
化学与科技、社会、生产密切相关,下列有关说法不正确的是( )
A . 从海水中可以提取镁、溴、铀和重水
B . 乙醇汽油的广泛使用不能减少汽车尾气中NOx的排放,目前,全球仍处于化石能源时期
C . 阿司匹林可用于治疗胃酸过多,碘酸钾可用作营养强化剂
D . 高炉炼铁时,增加炉子的高度,使CO和Fe2O3充分接触反应,不能减少尾气中CO的含量
实验室里可用如下图所示的装置制取氯酸钾、次氯酸钠,并验证氯水的性质。
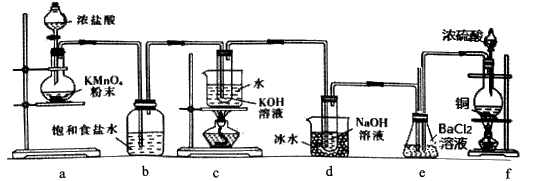
图中a为氯气发生装置,c的试管中盛有15mL30%的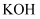 溶液,并置于热水浴中,d的试管中盛有15mL 8%的
溶液,并置于热水浴中,d的试管中盛有15mL 8%的 溶液,并置于冰水浴中,f为
溶液,并置于冰水浴中,f为 的发生装置。
的发生装置。
-
(1) 制取氯气时,在烧瓶中先加入一定量的
 固体,再通过(填写仪器名称)向烧瓶中加入适量的浓盐酸。
固体,再通过(填写仪器名称)向烧瓶中加入适量的浓盐酸。
-
(2) 装置b的作用是。
-
(3) f装置中反应的化学方程式为。
-
(4) 比较制取氯酸钾和次氯酸钠的条件,两者的差异是。
-
(5) 反应完毕经冷却后,c装置的试管中有大量晶体析出,图中符合该晶体溶解度随温度变化规律的曲线是(选填字母);从c装置的试管中分离该晶体的操作是(填写实验操作名称)。
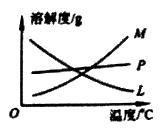
-
(6) 将d中余气与f中产生的气体通入e中,产生的现象为。
-
(7) 该实验有一处明显的缺点是。
海洋的化学资源有十分大的开发潜力。利用海水资源(主要含 、
、 , 少量的
, 少量的 、
、 、
、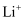 、
、 、
、 )制备碳酸锂的一种工艺如图所示:
)制备碳酸锂的一种工艺如图所示:
 、
、 , 少量的
, 少量的 、
、 、
、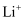 、
、 、
、 )制备碳酸锂的一种工艺如图所示:
)制备碳酸锂的一种工艺如图所示:
资料: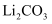 微溶于水,在冷水中溶解度较热水中大,不溶于乙醇。
微溶于水,在冷水中溶解度较热水中大,不溶于乙醇。
下列说法正确的是( )
A . 工序③和工序④顺序可互换
B . 工序⑤选择常温下进行,可降低碳酸锂在水中的溶解度,提高产率
C . 用乙醇洗涤粗产品可起到提高产率和快速干燥的效果
D . 滤渣1和滤渣2的主要成分分别是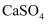 和
和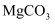
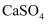 和
和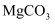
海水提溴的方法有多种,某提溴方法的部分工艺流程如下:
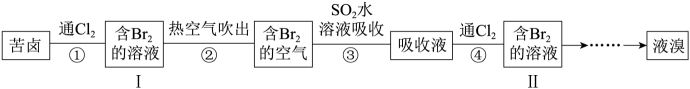
下列说法错误的是( )
A . 步骤③反应后的溶液酸性增强
B . 步骤②、③、④相当于“浓缩”环节
C . 步骤②利用了溴单质易挥发的性质
D . 用乙醇萃取Ⅱ溶液,可将水与Br2分离
海洋是巨大的化学资源宝库,如图是从海水中提取溴的流程图(部分)。据图回答下列问题。

-
(1) 写出一种工业上海水淡化的方法:。
-
(2) 过程1发生反应的离子方程式是。该反应可证明氧化性:

 (填“>”、“<”或者“=”),从原子结构角度解释原因。
(填“>”、“<”或者“=”),从原子结构角度解释原因。
-
(3) 过程2中发生反应生成两种强酸,写出该反应的化学方程式:。
-
(4) 上述过程2中将
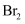 转化成
转化成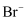 的目的是。
的目的是。
-
(5) 若过程2用
 溶液吸收溴,补全方程式:。
溶液吸收溴,补全方程式:。3
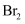 +_
+_ +_
+_ =_
=_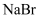 +_
+_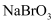 +_
+_
若反应中转移电子的物质的量为5mol,则被还原的溴单质的质量为:。
最近更新
- 世界市场形成的根本原因是() A.资本主义生产方式占据了统治地位 B.商品生产的发展和各国经济联系的加强 C.社会生产力
- 如图所示,拖拉机耕地时的速度往往很慢,这是为了 () A.保证挖土质量 B.获得较大的挖掘动力
- 在复数范围内解方程|z|2+(z+)i=(i为虚数单位).
- 某正态总体的概率密度函数是偶函数,而且该函数的最大值为,若总体落在区间(-∞,x)内的概率为0.001 3,则x的值是(
- “拿破仑执政期间,对外战争连绵不断,这些战争打击了欧洲各国旧的封建统治,传播了革命思想,但同时也掠夺了被占领国家的财富
- 根据句意及首字母提示完成单词 1. Doyou like to eat v_______ likecarrots and
- —__________isyou name? --My name is Mike. A. What
- 如图1,二次函数的图像过点A(-1,3),顶点B的横坐标为1. (1)求这个二次函数的表达式; (2)点P在该二次函数的
- 法律的显著特征是靠国家强制力保证实施。下列选项能体现这一特征的是 A.在今年爆发的甲型H1N1流感中,某人拒绝检查被拘留
- 互联网企业的金融化和金融企业的互联网化,近年来我国连续掀起了从“双11”到“双12”的几波电子商务大潮,创下了电子商务营
- 1688年“光荣革命”后统治英国的是( ) A.查理二世 B.威廉
- 读某城市内部和驻外联系路线图,回答问题。对图中路线网的叙述,不正确的是
- 已知A、B、C是圆上不同的三个点,且,存在实数λ,μ满足则实数λ,μ的关系满足
- .李冰主持修筑闻名世界的防洪灌溉工程是 A.灵渠 B.长城 C.都江堰 D.大运河
- (14分)如图所示为研究电子枪中电子在电场中运动的简化模型示意图。在Oxy平面的ABCD区域内,存在两个场强大小均为E的
- 在研究匀变速直线运动的实验中,如图所示为一次记录小车运动情况的纸带,图中A、B、C、D、E为相邻的记数点,相邻记数点的时
- 如果实数a,b满足a+b=6,ab=8,那么a2+b2= .
- 一列简谐横波沿绳传播,振幅为0.2 m,传播速度为1 m/s,频率为0.5 Hz.在t0时刻,质点a正好经过平衡位置,沿
- 填入下面一段文字中横线处的语句,与上下文衔接最恰当的一项是( ) 要激发深层的阅读动机,必须着力培养自己的阅读习
- 北京市为成功举办2008年奥运会,决定从2003年到2007年五年间更新市内现有的全部出租车,若每年更新的车辆数比前一年



