第4节 海水中的化学元素 知识点题库
①烧碱 ②纯碱 ③金属钠 ④氯气 ⑤盐酸.
①NH3 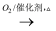 NO
NO 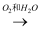 HNO3
HNO3
②浓HCl  Cl2
Cl2 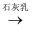 漂白粉
漂白粉
③MgCl2(aq)  无水MgCl2
无水MgCl2  Mg
Mg
④饱和NaCl(aq) 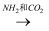 NaHCO3
NaHCO3  Na2CO3
Na2CO3
⑤铝土矿 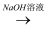 NaAlO2溶液
NaAlO2溶液 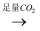 Al(OH)3
Al(OH)3  Al2O3
Al2O3  Al.
Al.
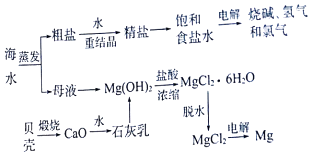
试回答下列问题:
-
(1) 实验室里将粗盐制成精盐的过程中,过滤的操作需用到玻璃棒,玻璃棒的作用是:,还需要的玻璃仪器有:.
-
(2) 粗盐中含有Ca2+、Mg2+、SO42﹣等杂质,精制后可得NaCl饱和溶液,精制时通常在溶液中:①加入过量的BaCl2溶液,②过量的NaOH溶液,③过量的Na2CO3溶液,则添加试剂顺序为(填写序号),最后在滤液加入盐酸至溶液呈中性.请写出加入盐酸后可能发生反应的离子方程式:.
-
(3) 海水提取食盐后的母液中有K+、Na+、Mg2+等阳离子.从离子反应的角度考虑,在母液里加入石灰乳发生反应的离子方程式:.
-
(4) 电解无水氯化镁制取镁的化学方程式为.将镁蒸气冷却后即为固体镁,镁蒸气需在Ar气氛围中冷却,理由:.
漂白粉的主要成分是:(填化学式)有效成分是:(填化学式)
它的漂白原理是(用化学方程式表示).
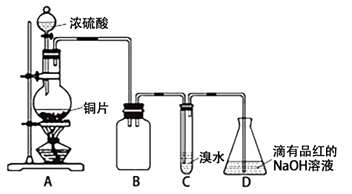
请回答下列问题:
-
(1) 装置B的作用是。
-
(2) 设计装置C的目的是验证SO2的性,装置C中发生反应的离子方程式是。装置D中NaOH全部转化为NaHSO3的标志是。
-
(3) 向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.HSO3-与ClO-恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量

甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HClO)
-
(4) 请设计简单实验证明:室温下HSO3-的电离平衡常数Ka与水解平衡常数Kb的相对大小:。
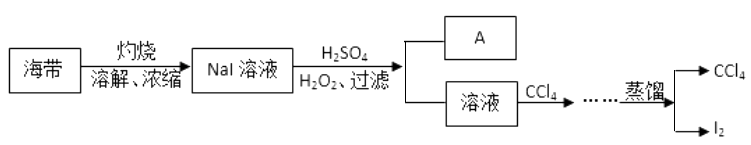
已知:常温下,碘在水中的溶解度为0.034g;碘的沸点为184℃;CCl4的沸点为77℃。
请回答:
-
(1) A物质是
-
(2) 写出在酸化下用H2O2氧化NaI的化学反应方程式
-
(3) 流程中省略部分的操作是
-
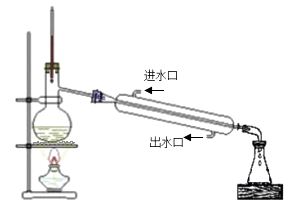
(4) 蒸馏装置中错误的是
(写三条)
-
(5) 蒸馏出的CCl4液体中常会带淡紫色,可能的原因是
-
(1) 海水晒盐可获得粗盐,在实验室中粗盐经过溶解、、可制得精盐。(填具体操作名称)
-
(2) 镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的,其主要步骤如下:
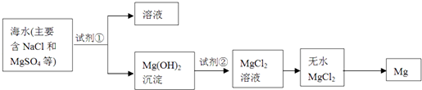
①为了使MgSO4转化为Mg(OH)2 , 试剂①可以选用。
②试从节约能源、提高金属镁的纯度分析,以下适宜的冶镁方法是。
A.Mg(OH)
 MgO
MgO  Mg B.Mg(OH)
Mg B.Mg(OH)  MgO
MgO  Mg
MgC.Mg(OH)2
 MgCl2
MgCl2 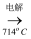 Mg D.Mg(OH)2
Mg D.Mg(OH)2  MgCl2
MgCl2 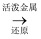 Mg
Mg -
(3) 溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作。工业以浓缩海水为原料提取溴的部分过程如下:
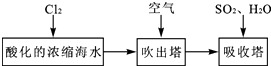
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
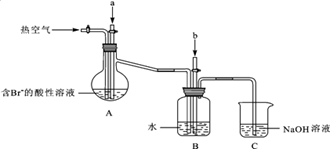
①A装置中通入a气体的目的是(用离子方程式表示);
②A装置中通入a气体一段时间后,停止通入,改通热空气.通入热空气的目的是;
③反应过程中,B装置中有SO42﹣生成,检验SO42﹣的方法是;
④C装置的作用是。
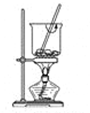 B . 过滤含碘离子溶液
B . 过滤含碘离子溶液 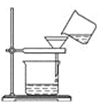 C . 放出碘的苯溶液
C . 放出碘的苯溶液 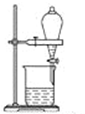 D . 分离碘并回收苯
D . 分离碘并回收苯 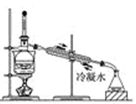
 Mg+Cl2↑
D . Mg(OH)2
Mg+Cl2↑
D . Mg(OH)2  MgO+H2O
MgO+H2O
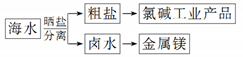
①通过氯碱工业可生产的产品有NaOH、NaClO、盐酸等
②除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸
③可将MgCl2·6H2O晶体在空气中直接加热脱水得到较纯净的无水MgCl2
④电解MgCl2溶液可制取金属镁
-
(1) 粽子由糯米等制作而成,糯米中的淀粉是否水解完全,可用来检验。
-
(2) 与甲烷互为同系物,且含有10个碳原子的有机物分子式为。
-
(3) 海洋资源的利用具有广阔前景。
①海水淡化的方法有(填一种)。
②下图是从海水中提取镁的简单流程:
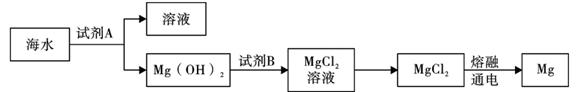
工业上常用于沉淀Mg2+的试剂A的俗名是,Mg(OH)2转化为MgCl2的离子方程式是。
-
(4) 如图所示是某同学设计的几种装置,其中能构成原电池的是(填序号)。
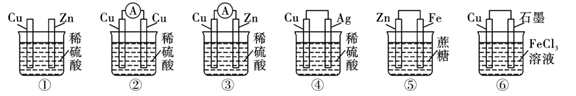
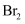 等物质
C . 利用太阳能电解海水可获取氢能源
D . 煤经过气化、液化可转化为清洁燃料
等物质
C . 利用太阳能电解海水可获取氢能源
D . 煤经过气化、液化可转化为清洁燃料
选项 | 实验操作 | 现象 | 结论 |
A | 向 |
|
|
B | 向含有 | 产生白色沉淀 |
|
C | 将稀盐酸滴入硅酸钠溶液中,充分振荡 | 产生白色沉淀 | 非金属性: |
D | 向某食盐溶液中滴加淀粉溶液 | 溶液不变色 | 该食盐不是加碘盐 |
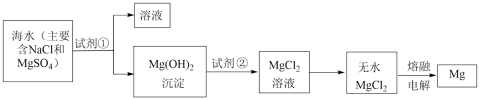
下列说法错误的是( )
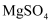 转化为
转化为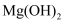 , 工业上试剂①主要选用
, 工业上试剂①主要选用 C . 加入试剂①后,可用过滤得到
C . 加入试剂①后,可用过滤得到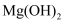 沉淀
D . 镁与铝等金属按一定比例制成的合金,由于其密度小、强度大,可用于制造飞机
沉淀
D . 镁与铝等金属按一定比例制成的合金,由于其密度小、强度大,可用于制造飞机
- Mother _____him to give up smoking, but he wouldn’t listen.
- 如图所示绘出了轮胎与地面间的动摩擦因数分别为μ1和μ2时,紧急刹车时的刹车痕(即刹车距离s)与刹车前车速V的关系曲线,则
- (08广安)广安地区的七、八月份属高温天气,又正值农村冬季蔬菜栽种季节,当菜苗栽上后, 很容易因蒸发过快而失水干枯,不
- ......
- 下列词语中加点字的注音,全部正确的一组是( ) A.挑衅(xìn) 褊小(biǎn)
- 下列各项实验应采取的交配方法分别是 ①鉴别一只白兔是否为纯合子②鉴别一对相对性状的显性和隐性 ③不断提高小麦抗病品种的纯
- 下列有关蒙古与清朝关系的表述,不正确的是
- 如图,是⊙O的直径,是⊙O上的两点,若,则的度数为( )A.B.C.D.
- 20世纪60、70年代韩国、新加坡和西亚产油国在经济发展上都( )A.面临国土小,人口密度大的问题 B.注重吸
- 我的妈妈从来不笑(15分) 女儿的学校发来一张通知,说邀请妈妈们参加座谈会,听听孩子们怎样评价自己的妈妈,这倒是一个新鲜
- We don’t have enough money .We,_______, can’t afford to buy
- 工业上利用液态空气中氧气、氮气和氩气的沸点不同,使其在不同的温度下气化,从而将各种气体分离出来(如图所示)。在蒸发液态空
- 表3为果蝇3个不同的突变品系与野生型 正交与反交的结果,试分析回答下列问题: (1)①组的正交与反交结果相
- 生物既能适应环境,又能影响环境。下列各项能说明生物影响环境的是( ) A.夏天大雨过后,蚯蚓常常会爬出地面
- 下列说法正确的是 A.需要加热才能发生的反应一定是吸热反应 B.吸热反应不加热的条件一定不能发生 C.放热反应在常温下一
- 阅读下面的文字,完成题。 【甲】说到门,我们便会兴起这样的印象:门是森严的、拒绝的,摒弃的,无情的东西。我们如果去访问一
- “猫被创造出来是为了吃老鼠,老鼠被创造出来是为了给猫吃,而整个自然界被创造出来是为了证明造物主的智慧。”这里所讲的“联系
- 现代商场中一般都安装自动扶梯.某商场有一台倾角为30°的自动扶梯,该扶梯在电压为380 V的电动机带动下以0.4 m/s
- When I study English, I like to put my dictionary _______ my
- 下列有关实验装置进行的相应实验,能达到实验目的的是( )A.用图1装置制取并收集干燥纯净的NH3 B.用图2所示装置可
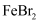 溶液中加入少量氯水,再加
溶液中加入少量氯水,再加 萃取
萃取 的还原性强于
的还原性强于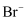 的
的 的
的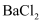 溶液中通入气体
溶液中通入气体