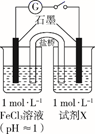
第3节 硫的转化 知识点题库
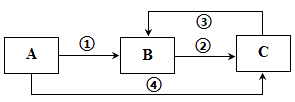
| 序号 | 实验事实 | 结论 |
| A | CO2的水溶液可以导电 | CO2是电解质 |
| B | Ca(ClO)2溶液中通入CO2产生白色沉淀 | 酸性:H2CO3>HClO |
| C | 向无色溶液中加入氯化钡溶液有白色沉淀生成,再加盐酸,沉淀不消失 | 原溶液中一定含有SO42- |
| D | 用铂丝蘸取某溶液在酒精灯火焰上灼烧直接观察火焰颜色,未见紫色 | 原溶液中不含K+ |
| 选项 | 实验目的 | 实验方案 |
| A | 比较镁、铝的金属性强弱 | 分别在MgCl2和AlCl3溶液中滴加氨水直至过量,观察现象 |
| B | 比较Cl2、Br2的氧化性强弱 | 将少量氯水滴入FeBr2溶液中,观察现象 |
| C | 证明SO2具有漂白性 | 将SO2通入酸性高锰酸钾溶液中,溶液褪色 |
| D | 证明电离常数Ka:HSO3->HCO3- | 测得同浓度的Na2CO3溶液的pH大于Na2SO3溶液 |
(甲同学的实验)
|
装置 |
编号 |
试剂X |
实验现象 |
|
| I | Na2SO3溶液(pH≈9) | 闭合开关后灵敏电流计指针发生偏转 |
| II | NaHSO3溶液(pH≈5) | 闭合开关后灵敏电流计指针未发生偏转 |
-
(1) 配制FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度。结合化学用语说明浓盐酸的作用:。
-
(2) 甲同学探究实验I的电极产物。
①取少量Na2SO3溶液电极附近的混合液,加入,产生白色沉淀,证明产生了
 。
。②该同学又设计实验探究另一电极的产物,其实验方案为。
-
(3) 实验I中负极的电极反应式为。
-
(4) (乙同学的实验)
乙同学进一步探究FeCl3溶液与NaHSO3溶液能否发生反应,设计、完成实验并记录如下:
装置
编号
反应时间
实验现象
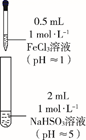
III
0~1 min
产生红色沉淀,有刺激性气味气体逸出
1~30 min
沉淀迅速溶解形成红色溶液,随后溶液逐渐变为橙色,之后几乎无色
30 min后
与空气接触部分的上层溶液又变为浅红色,随后逐渐变为浅橙色
乙同学认为刺激性气味气体的产生原因有两种可能,用离子方程式表示②的可能原因。
① Fe3++3
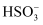
 Fe(OH)3 +3SO2;②。
Fe(OH)3 +3SO2;②。 -
(5) 查阅资料:溶液中Fe3+、
 、OH-三种微粒会形成红色配合物并存在如下转化:
、OH-三种微粒会形成红色配合物并存在如下转化: 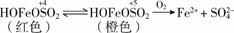
从反应速率和化学平衡两个角度解释1~30 min的实验现象:。
-
(6) 解释30 min后上层溶液又变为浅红色的可能原因:。
-
(7) (实验反思)
分别对比I和II、II和III,FeCl3能否与Na2SO3或NaHSO3发生氧化还原反应和有关(写出两条)。
 性质实验(夹持装置已省略)
性质实验(夹持装置已省略) 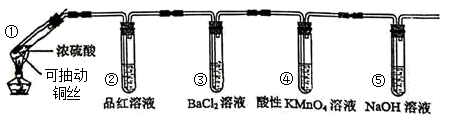
下列说法错误的是( )
 的漂白性
D . 试管⑤可以改为装有碱石灰的干燥管
的漂白性
D . 试管⑤可以改为装有碱石灰的干燥管
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | BaSO4难溶于酸 | 用盐酸和BaCl2溶液检验 |
| D | NH3能使酚酞溶液变红 | NH3可用于设计喷泉实验 |
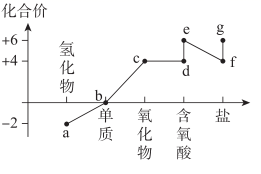
 减小
C . 盐g与盐f之间也可能发生反应
D . 铜与e的浓溶液共热产生的气体通入
减小
C . 盐g与盐f之间也可能发生反应
D . 铜与e的浓溶液共热产生的气体通入  溶液中,无明显现象
溶液中,无明显现象
-
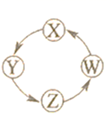
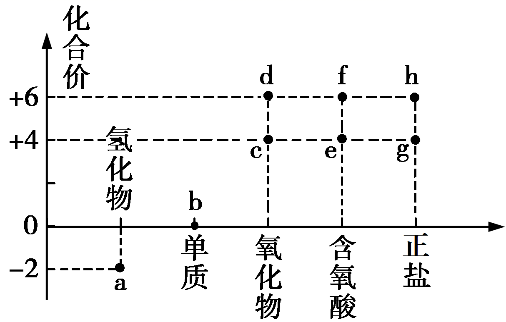
(1) 从X、Y、Z、W四种元素中选择合适的元素,组成与表中第一栏类别相同的物质,将其化学式填在表中相应的空格内。
类型
碱性氧化物
最高价的酸性氧化物
二元强酸
可溶性碱
弱酸的酸式盐
化学式
-
(2) 选用你在上表中所填的物质,按下列要求写出相应的化学方程式。
①某个化合反应:
②氧化物与足量的碱反应:
③酸式盐和足量的碱反应:
[提示:酸碱中和反应生成和水,酸跟碱反应时,若酸、碱电离产生的氢离子和氢氧根离子恰好完全反应,生成的为正盐(如NaCl、 Na2CO3);若酸中的氢离子部分被中和,生成的盐为酸式盐(如 NaHCO3)。一元酸没有酸式盐]
| 选项 | X | Y | Z | W | |
| A | S | SO2 | H2SO3 | Na2SO4 | |
| B | Na | Na2O2 | Na2CO3 | NaCl | |
| C | Cl2 | Ca(ClO)2 | HClO | HCl | |
| D | Fe | Fe2(SO4)3 | FeSO4 | Fe(OH)2 |
- 如图所示,用相同的轮滑不同的绕法提起相同的重物,绳重、摩擦忽略不计,在物体匀速上升的过程中() A. 甲图省力,
- 已知如下物质的溶度积常数: :;:; :。下列说法正确的是( ) A.同温度下,的溶解度大于的溶解度 B.将足量溶
- 下列说法正确的是。(填正确答案标号。选对1个得3分,选对2个得4分,选对3个得6分。每错选1个扣3分,最低得分为0分)
- 守着窗儿,独自怎生得黑? , 。(李清照《声声慢》)
- 已知甲、乙两种物质的溶解度(S甲、S乙)均随着温度的升高而增大。在10℃时20g水中最多能溶解5克甲;30℃时,乙物质的
- 已知正项数列{an}的前n项和为Sn,若{an}和{}都是等差数列,且公差相等,则a6=() A. B. C
- 已知角的顶点在原点,始边与平面直角坐标系x轴的正半轴重合,点在角的终边上,则=.
- 17.为了测量雪的密度,同学们找来器材进行了测量:① 用弹簧测力计测出空杯子重力为0.2N ;② 将杯子里装满水,用弹簧
- 电热毯、电饭锅是人们常用的电热式家用电器,它们一般具有加热和保温功能,其工作原理大致相同.图14-2①为某种电热式电器的
- He lived his whole life as a poor man. His art and talent we
- 下列关于空气的叙述,正确的是() A、空气的成分是比较固定的 B、城市空气污染严重是因为人口稠密使大气中的二氧化碳过浓
- 下列叙述正确的是( )A.固体氯化钠不导电,所以NaCl是非电解质B.铜丝能导电,所以铜是电解质C.氯化氢水溶液能
- 随着新航路的开辟,由美洲传到中国的是 ( )A.土豆(马铃薯)、玉米 B.烟叶、甘蔗 C.葡萄、
- 阅读下面这首诗,然后回答问题。 溪 居① 柳宗元 久为簪组②累,幸此南夷谪。 闲依农圃邻,偶似山林客。 晓耕翻露
- pH=12的氢氧化钠溶液稀释100倍后,pH=
- 为支持我国新能源汽车发展,中央财政对购买符合要求的新能源汽车实行补贴,一些试点省市的地方财政也同步进行补贴。在这一政策支
- 下列看法中,最能够体现矛盾的“统一”的是() A.积劳成疾 B.声东击西 C.量体裁衣 D.居安思危
- 构成金属晶体的微粒是A.原子 B.分子 C.金属阳离子 D.金属阳离子和
- 当条件满足时,20个腺苷和60个磷酸最多可以组成的ATP分子及其中所含的高能磷酸键有( )。 A. 20个,40
- 某元素最高正价氧化物对应的水化物的化学式是H2XO4,这种元素的气态氢化物的化学式为 A. HX B