第3节 硫的转化 知识点题库
下列物质间的转化,通过一步反应不能实现的是( )
A . CO2→Na2CO3
B . FeCl3→FeCl2
C . H2SiO3→Na2SiO3
D . S→SO3
下列说法正确的是( )
A . 将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中必有铁
B . CO2和SO2混合气体分别通入BaCl2溶液、Ba(NO3)2溶液中,最终都有沉淀生成
C . 钠、镁着火时,不可用泡沫灭火器灭火
D . 用加热分解的方法可将NH4Cl固体和Ca(OH)2固体的混合物分离
50ml浓H2SO4溶液(足量)中加入3.2g Cu,在加热条件下充分反应:
-
(1) 反应消耗的H2SO4的物质的量是,生成SO2的体积为(标准状况下) mL.
-
(2) 若题干中浓硫酸的物质的量浓度为a mol•L﹣1 , 投入足量的铜片加热,充分反应后,被还原的硫酸的物质的量n(H2SO4) 0.025a mol(填“等于”、“大于”或“小于”).
-
(3) 将题干中反应后的溶液稀释到500mL,取出50mL,并向取出液中加入足量的BaCl2溶液,得到沉淀19.81g,求原浓硫酸的物质的量浓度.
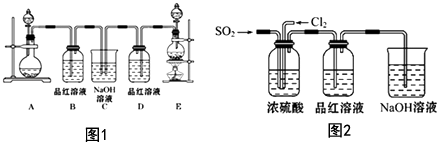
某中学化学实验小组为了证明和比较SO2与氯水的漂白性,设计了如下装置:
-
(1) 实验室常用装置E制备Cl2 , 写出该反应的离子方程式:.
-
(2) 反应开始后,发现B、D两个容器中的品红溶液都褪色,停止通气后,加热B、D两个容器,现象分别为B;D.
-
(3) 装置C的作用是.
-
(4) 该实验小组的甲、乙两位同学利用上述两套发生装置按下图装置继续进行实验:
通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅.
试根据该实验装置和两名同学的实验结果回答问题.
①试分析甲同学实验过程中,品红溶液不褪色的原因是(用离子方程式进行说明)
②你认为乙同学是怎样做到让品红溶液变得越来越浅的?.
具有漂白性和还原性的无色气体是( )
A . Cl2
B . NO2
C . NH3
D . SO2
对于下列事实的解释错误的是( )
A . 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B . 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C . 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应
D . 铝箔在空气中受热可以融化,由于氧化膜的存在,融化的铝并不滴落
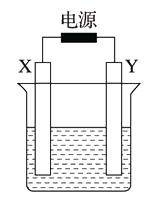
如图,X和Y均为石墨电极。
-
(1) 若电解液为滴有酚酞的饱和食盐水,电解反应的离子方程式为;电解过程中(填“阴”或“阳”)极附近会出现红色。
-
(2) 若电解液为500 mL含A溶质的某蓝色溶液,电解一段时间,观察到X电极表面有红色的固态物质生成,Y电极有无色气体生成。溶液中原有溶质完全电解后,停止电解,取出X电极,洗涤、干燥、称量,电极质量增加1.6 g。
①电解后溶液的pH为;要使电解后溶液恢复到电解前的状态,需加入一定量的(填加入物质的化学式)。(假设电解前后溶液的体积不变)
②Y电极产生气体的体积为L。
③请你推测原溶液中所含的酸根离子可能是;并设计实验验证你的推测,写出实验的操作步骤、现象和结论: 。
下列五种有色溶液与SO2作用均能褪色,其实质相同的是( )
①品红溶液;②酸性KMnO4溶液;③溴水;④滴有酚酞的NaOH溶液;⑤含I2的淀粉溶液
A . ①④
B . ①②③
C . ②③⑤
D . ③④
下列说法中错误的是( )
A . 二氧化硫能漂白某些物质,说明它具有氧化性
B . 二氧化硫的水溶液中滴加氯化钡无现象,再加入0.5mL3%的过氧化氢后产生沉淀
C . 将足量二氧化硫通入酸性高锰酸钾溶液中,溶液褪色,不能说明二氧化硫具有漂白性
D . 二氧化硫漂白过的草帽过一段时间后变黄
下列说法正确的是( )
A . 钠在空气中燃烧只生成白色固体
B . 钠在氯气中燃烧呈现苍白色火焰
C . SO2使紫色石蕊试液先变红后褪色
D . 铜在氯气中燃烧生成棕黄色烟
下列说法不正确的是( )
A . 瑞典化学家贝采利乌斯最早提出了有机化学的概念
B . 晶体硅可用于制造半导体材料
C . “光化学烟雾网”、“硝酸酸雨”的形成都与氮氧化物有关
D . 氢氧化铝和苏打都可以用于治疗胃酸过多
下列说法正确的是( )
A . 亚硝酸钠溶液具有防腐作用,可用来浸泡新鲜瓜果
B . 我国古代就已采用加热胆矾或绿矾的方法制取硫酸
C . 红宝石是含有少量金属氧化物的刚玉,主要成分为二氧化硅
D . Na3AlF6溶液中滴加1mol/L氨水至过量会产生白色沉淀
单质到盐的转化关系可表示为:
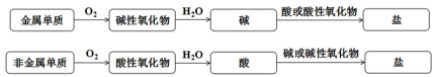
下述转化关系错误的是( )
A . Na  Na2O
Na2O  NaOH
NaOH  CH3COONa
B . Mg
CH3COONa
B . Mg  MgO
MgO  MgCl2
MgCl2 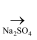 MgSO4
C . C
MgSO4
C . C  CO2
CO2  H2CO3
H2CO3 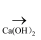 CaCO3
D . S
CaCO3
D . S  SO2
SO2  H2SO3
H2SO3  Na2SO3
Na2SO3
 Na2O
Na2O  NaOH
NaOH  CH3COONa
B . Mg
CH3COONa
B . Mg  MgO
MgO  MgCl2
MgCl2 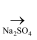 MgSO4
C . C
MgSO4
C . C  CO2
CO2  H2CO3
H2CO3 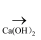 CaCO3
D . S
CaCO3
D . S  SO2
SO2  H2SO3
H2SO3  Na2SO3
Na2SO3
某兴趣小组设计如图所示装置制取SO2 , 研究其性质。
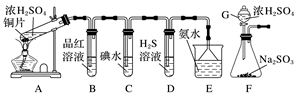
-
(1) 仪器G的名称是。
-
(2) 装置B、C、D分别用于检验SO2的漂白性、还原性和氧化性。则装置C中反应的离子方程式,证明SO2具有氧化性的实验现象是。
-
(3) 为了实现绿色环保的目标,某同学设计装置F来代替装置A。与装置A相比,装置F的优点是(写出两点)。
-
(4) 若选用装置F制取O2可选用的试剂是。
利用表中药品及图示装置不能制取的气体是( )
| 选项 | 制备气体 | ① | ② | |
| A | NH3 | 浓氨水 | 碱石灰 | |
| B | Cl2 | 浓盐酸 | 二氧化锰 | |
| C | NO2 | 浓硝酸 | 铜粉 | |
| D | SO2 | 浓硫酸 | 亚硫酸钠 |
A . A
B . B
C . C
D . D
下列说法错误的是( )
A . “爆竹声中一岁除”,爆竹中的火药含有硫黄
B . 浓硫酸可用铁制容器装运
C . 液氨可用作制冷剂
D . “雷雨发庄稼”,该过程没有硝酸生成
下列物质之间的转化都能一步实现的是( )
A . H2S→S→SO3→H2SO4
B . Si→SiO2→H2SiO3→Na2SiO3
C . FeS2→SO2→Na2SO3→Na2SO4
D . N2→NH3→NO2→HNO3→NO2
下列解释事实的方程式正确的是( )
A . CO2通入过量的NaOH溶液中:CO2+OH-=  B . SO2的催化氧化反应:2SO2+O2
B . SO2的催化氧化反应:2SO2+O2 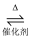 2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
 B . SO2的催化氧化反应:2SO2+O2
B . SO2的催化氧化反应:2SO2+O2 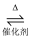 2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
甲、乙、丙、丁均为中学常见的纯净物,其中甲、乙、丙均含同一种元素,它们之间存在转化关系: 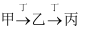 (其他产物及反应条件已略去)。回答下列问题:
(其他产物及反应条件已略去)。回答下列问题:
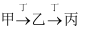 (其他产物及反应条件已略去)。回答下列问题:
(其他产物及反应条件已略去)。回答下列问题:
-
(1) 若甲为具有臭鸡蛋气味的有毒气体,乙为淡黄色固体单质;甲和丙反应可生成乙和另一种无色无味的液体,则甲的化学式为,写出甲和丙反应的化学方程式:。
-
(2) 若甲、乙、丙均为化合物,其中甲为有刺激性气味的气体,水溶液呈碱性;丙为红棕色气体。
①实验室检验气体甲的方法为(简述操作、现象及结论)。
②在催化剂的作用下,气体甲可还原乙和丙生成两种无污染的物质。同温、同压下将体积分别为
 、
、  、
、  的甲、乙、丙三种气体混合,在催化剂的作用下充分反应恰好生成两种无污染的物质,则
的甲、乙、丙三种气体混合,在催化剂的作用下充分反应恰好生成两种无污染的物质,则  、
、  、
、  应满足的关系是(用
应满足的关系是(用  、
、  、
、  表示)。
表示)。 -
(3) 若甲为短周期元素组成的一元强碱,丁为无色无味的气体。
①某实验小组设计用澄清石灰水来鉴别乙和丙,该实验(填“能”或“不能”)成功,其原因为。
②写出甲和丙反应的离子方程式:。
化学与生产、生活密切相关。下列说法正确的是( )
A . 含氟牙膏可用于预防龋齿
B .  有毒,不能作为食品添加剂
C . 过滤后的地沟油可用于加工食品
D . 75%酒精、明矾均可用于消毒杀菌
有毒,不能作为食品添加剂
C . 过滤后的地沟油可用于加工食品
D . 75%酒精、明矾均可用于消毒杀菌
 有毒,不能作为食品添加剂
C . 过滤后的地沟油可用于加工食品
D . 75%酒精、明矾均可用于消毒杀菌
有毒,不能作为食品添加剂
C . 过滤后的地沟油可用于加工食品
D . 75%酒精、明矾均可用于消毒杀菌
最近更新
- 下图为钠硫高能电池的结构示意图,M为Na2O和Al2O3的混合物,电池反应为2Na+xSNa2Sx该电池的工作温度为32
- AB是电场中的一条电场线,若将一负电荷从A点处自由释放,负电荷沿电场线从A到B运动过程中的速度时间图像如图所示,则A、B
- “红色旅游”作为一种新型主题旅游形式,近年来在神州大地逐渐兴起。下列湖南旅游景区以“红色旅游”为主要特色的是(
- 沼气是一种能源,它的主要成分是CH4。0.5mol CH4完全燃烧生成CO2和液态H2O时,放出445KJ热量,则下列热
- 用右图所示的装置进行实验,验证质量守恒定律。 (1)试剂a可以是________(写出一种即可)。 (2)证明质量守恒定
- 下列杂交组合中,后代只有一种表现型的是 A.Aabb×aabb B.AABb×aabb C.AaBb×Aa
- 用红色荧光染料标记人细胞膜上的蛋白质,用绿色荧光染料标记鼠细胞膜上的蛋白质。把人和鼠的两细胞融合。融合后的细胞一半发红色
- 对某种植物进行测交实验,后代有四种表现型,其数量分别是49、52、50、51,这株植物的基因型不可能是 A
- 下列关于细胞核的结构与功能的叙述不正确的是() A.多利羊的产生说明了动物细胞具有全能性 B.除了高等植物成熟的筛管细胞
- 到2009年12月11日,我国加入WTO已经8年。8年来,中国平均关税水平大幅降 低,服务领域的开放程度接近发达国家水平
- 若函数y=+3的图象恒过定点P,则P点坐标为________.
- Get Your Degree at Home! Have you ever wondered what a degre
- 于某与马某结婚时签订书面协议约定婚后所得财产各自所有。马某婚后即辞去工作在家侍养公婆、照顾孩子。于某长期在外地工作,后与
- A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平。D是一种日常生活中常用的调味品。A、B、C、D在一定
- 1.In (在制定计划时),they went to the library to refer to
- 顶点在原点,坐标轴为对称轴的抛物线,过点(-2,3),则它的方程是A.x2=-y或y2=x
- 现有4个人去参加某娱乐活动,该活动有甲、乙两个游戏可供参加者选择.为增加趣味性,约定:每个人通过掷一枚质地均匀的骰子决定
- 电影《建党伟业》中有这样一句经典台词:“什么是政治?政治就是把敌人的人搞得少少的,把自己的人搞得多多的!&r
- 用显微镜观察水中的花粉,追踪某一个花粉颗粒,每隔10 s记下它的位置,得到了a、b、c、d、e、f、g等点,再用直线依次
- 下表是某营养级昆虫摄食植物后能量流动情况,下列说法错误的是() 项目 昆虫摄食量 昆虫粪便量 昆虫呼吸消耗量 昆虫储存在