第二单元 铁、铜的获取及应用 知识点题库
①按Br2、Fe3+、I2的顺序氧化性逐渐减弱
②原溶液中Br﹣一定被氧化
③通入氯气后原溶液中的Fe2+一定被氧化
④不能确定通入氯气后的溶液中是否还存在Fe2+
⑤若取少量所得溶液,加入CCl4后静置,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中Fe2+、Br﹣均被完全氧化.
项目 | 熔点/℃ | 密度/ (g•cm﹣3) | 硬度(金刚 石为10) | 导电性 (银为100) |
某合金 | 2 500 | 3.00 | 7.4 | 2.3 |
铁 | 1 535 | 7.86 | 4.5 | 17 |
从性能看,该合金不适合制( )
-
(1) Fe2+离子在水溶液中呈现的颜色是 ;Fe(OH)2转化为红褐色沉淀的化学方程式为
-
(2) 有人认为白色沉淀迅速变为灰绿色的原因是Fe(OH)2凝胶吸附了溶液中过量的Fe2+
离子.为探究该观点的正确性,设计如下两个实验:
①向盛有NaOH溶液的试管中加入少量FeSO4溶液,若该观点正确,应观察到的现象是
②已知胶体粒子的吸附能力随温度升高而下降.向盛装FeSO4溶液的试管中滴加少量NaOH溶液,析出白色沉淀,沉淀迅速变为灰绿色,将此试管小心加热,若观察到 ,则说明上述解释成立.
①金属钠在纯氧中燃烧
②Fe2(SO4)3溶液中滴入NaOH溶液
③FeCl3溶液中滴入KSCN溶液
④无水硫酸铜放入医用酒精中.
⑴将固体混合物溶于水,搅拌后得无色透明溶液
⑵往此溶液中滴加硝酸钡溶液,有白色沉淀生成
⑶过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解.
(填化学式)试判断,固体混合物中肯定有,肯定没有,可能有,对可能有的物质可采用滤液中滴加溶液的方法来检验.
| | | | |
| A.苴却砚 | B.钛零件 | C.国胜茶 | D.油底肉 |
①在人类对金属材料的使用过程中,性质活泼的金属单质最早被人们冶炼和使用
②纯铁比生铁抗腐蚀性更强
③单质铝在空气中比较耐腐蚀,所以铝是不活泼金属
④向紫色石蕊试液中加入过量的Na2O2粉末,振荡,溶液变为蓝色并有气泡产生
⑤青铜、不锈钢、硬铝都是合金
⑥可通过焰色反应区分钾元素和钠元素
⑦将FeCl3溶液滴入KI-淀粉溶液中,溶液变蓝色
⑧铝粉和氧化镁粉末混合,高温能发生铝热反应
 和氨水的混合液浸取废铜矿渣中的单质铜,得到
和氨水的混合液浸取废铜矿渣中的单质铜,得到  。某小组同学欲通过实验探究其原理。
。某小组同学欲通过实验探究其原理。 (查阅资料)i.  呈深蓝色,
呈深蓝色, 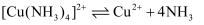 ;受热易分解,放出氨气。
;受热易分解,放出氨气。
ii. 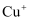 在水溶液中不稳定,
在水溶液中不稳定, 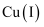 在溶液中只能以
在溶液中只能以 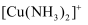 等络合离子的形式稳定存在;
等络合离子的形式稳定存在; 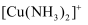 无色,易被氧气氧化为
无色,易被氧气氧化为  。
。
-
(1) (实验1)制备
 。
。 向盛有
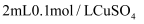 溶液的试管中滴加
溶液的试管中滴加 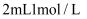 氨水,观察到溶液中立即出现浅蓝色沉淀;随后沉淀逐渐溶解,得到深蓝色溶液。经分离得到
氨水,观察到溶液中立即出现浅蓝色沉淀;随后沉淀逐渐溶解,得到深蓝色溶液。经分离得到  晶体。
晶体。资料表明,向
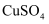 溶液中滴加氨水,可能会生成浅蓝色
溶液中滴加氨水,可能会生成浅蓝色 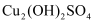 沉淀。
沉淀。①该小组同学取实验1中浅蓝色沉淀,洗涤后,(补全实验操作和现象),证明沉淀中含有
 。
。②补全实验1中生成
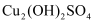 沉淀的离子方程式:
沉淀的离子方程式: +
+ 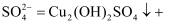
-
(2) 甲同学设计实验证明深蓝色溶液中含
 :加热深蓝色溶液并检验逸出气体为氨气。你认为此方案(填“可行”或“不可行”),理由是。
:加热深蓝色溶液并检验逸出气体为氨气。你认为此方案(填“可行”或“不可行”),理由是。
-
(3) (实验2)探究用
 和氨水的混合液浸取单质铜得到
和氨水的混合液浸取单质铜得到  的原理。
的原理。 编号
实验装置及部分操作
烧杯中溶液
实验现象
2-1
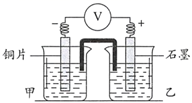
实验开始,先读取电压表示数,后迅速将其换成电流表,继续实验, 10 min内记录甲烧杯中现象
甲:
乙:
电压表指针迅速偏转至0.1V;甲中溶液无明显变化
2-2
甲:
乙:
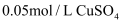
电压表指针迅速偏转至0.3V;甲中溶液无明显变化
2-3
甲:
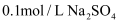 与
与 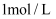 氨水等体积混合
氨水等体积混合乙:溶液A
电压表指针迅速偏转至0.35V;甲中溶液无明显变化
2-4
甲:
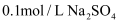 与
与 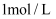 氨水等体积混合
氨水等体积混合乙:
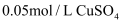
电压表指针迅速编转至0.65V;几分钟后,甲烧杯溶液逐渐由无色变蓝色
已知:其他条件相同时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,检测到的电压越大
溶液A为。
-
(4) 对比实验2-1和2-2,可以得到结论是。
-
(5) 实验2-4中,甲烧杯中溶液由无色变为蓝色的原因是。
-
(6) 依据上述实验,分析用
 和氨水的混合液浸取单质铜的原理:。
和氨水的混合液浸取单质铜的原理:。
 、
、 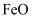 ,杂质为
,杂质为  和
和  等)为原料制备氢氧化氧铁(
等)为原料制备氢氧化氧铁( 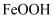 )的流程如下:
)的流程如下: 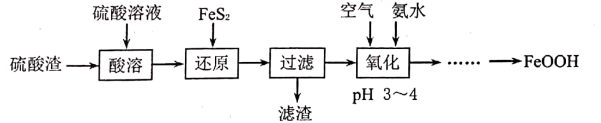
下列说法错误的是( )
 B . “还原”时可以用铁粉代替
B . “还原”时可以用铁粉代替  C . “氧化”的目的是将二价铁氧化成三价铁
D . “……”一系列操作为蒸发浓缩、冷却结晶
C . “氧化”的目的是将二价铁氧化成三价铁
D . “……”一系列操作为蒸发浓缩、冷却结晶
-
(1) I.铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂等。
向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2+(不考虑空间构型),[Cu(OH)4]2+结构可用示意图表示为。
-
(2) 胆矾CuSO4•5H2O可写为[Cu(H2O)4]SO4•H2O,其结构示意如图:则关于 [Cu(H2O)4]SO4的下列说法中错误的是________
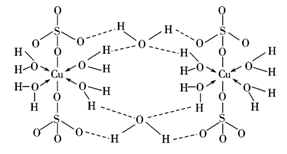 A . 此配合物中心离子的配位数为4 B . 配体为H2O,配位原子是氧原子 C . 此配合物中Cu2+提供孤对电子 D . 向此配合物溶液中加入BaCl2溶液,将出现白色沉淀
A . 此配合物中心离子的配位数为4 B . 配体为H2O,配位原子是氧原子 C . 此配合物中Cu2+提供孤对电子 D . 向此配合物溶液中加入BaCl2溶液,将出现白色沉淀 -
(3) II.经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1:3的个数比配合,还可以其他个数比配合。
若所得的Fe3+和SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合,所得离子显红色,该离子的离子符号是。
-
(4) 若所得的Fe3+和SCN-以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示。
| | | | |
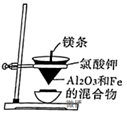
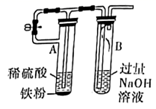
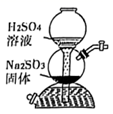
| A.铝热反应 | B.制备 | C.制备 | D.测定 |
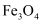 与
与  转化为
转化为 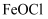 ,周围环境的
,周围环境的  增大
B .
增大
B . 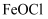 可自发转变为
可自发转变为 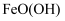 ,说明
,说明 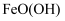 的溶解度小于
的溶解度小于 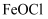 C . 检验
C . 检验 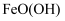 中是否含有
中是否含有 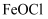 ,可选用的试剂是稀硫酸和
,可选用的试剂是稀硫酸和  溶液
D .
溶液
D . 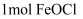 完全转化为
完全转化为 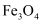 时转移
时转移 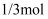 电子
电子
 FeCl2
FeCl2  Fe(OH)2
B . S
Fe(OH)2
B . S  SO3
SO3 H2SO4
C . NH4Cl (s)
H2SO4
C . NH4Cl (s)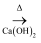 NH3
NH3 Mg(OH)2
D . Al2O3
Mg(OH)2
D . Al2O3 Al(OH)3
Al(OH)3 NaAlO2
NaAlO2
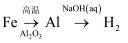 B .
B .  C .
C . 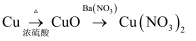 D .
D . 
- 下列说法中错误的是() A.在豆浆中加入少量石膏,能使豆浆结为豆腐 B.误服可溶性重金属盐,立即服用大量牛奶或蛋清或豆浆
- I will never know ________whether I was encouraging or disco
- 下列过程中,涉及肽键数量变化的是 A.洋葱根尖细胞染色体的复制 B.用纤维素酶处理植物细胞 C.小肠上皮细胞
- 下列对秦朝历史的评价,不正确的是 A.秦朝是我国历史上第一个统一的多民族的封建国家 B.秦朝在全国第一次推行郡县制度 C
- 下列反应中,硝酸既表现氧化性,又表现酸性的是() A.使石蕊试液变红 B.与铜反应放出NO气体,生成Cu(NO3)2 C
- 对图中由Q1点到Q2点运动的描述中,理解正确的是
- 设点P(x,y)(xy≠0)是曲线上的点,下列关系正确的是 ( ) A. B. C.
- (a2-+)÷a2b2;
- As a young boy my family was very poor. Iwould often help do
- 下列实验方案中合理的是()。 A.除去氢氧化钠中少量的碳酸钠——加稀盐酸 B.清洗铁制品表面的铁锈——用水洗涤 C.鉴别
- 有学者认为:“八国联军惊醒了中国这头“沉睡的巨人”,……让中国人向世界看齐,不自觉的参与世界近代化进程”。对作者的观点理
- 下列变化属于化学变化的是( ) A.煤焦油分馏 B.裂解C.
- 目前,发达国家和发展中国家都在全球寻求资源的最佳配置,这使全球生产体系出现混合型多层次分工的结构。棉花及其制品跨国生产与
- 上海市浦东新区2009届高三上学期期末质量抽测(政治18) “幸福感”已成为一项重要内容,列入每年进行的和谐社会指标体系
- 如图所示,一轻质弹簧竖立于地面上,质量为m的小球,自弹簧正上方h高处由静止释放,则从小球接触弹簧到将弹簧压缩至最短(弹簧
- 某农作物因缺钾而生长不良,应给它施用的化肥是 A.K2SO4 B.(NH4)2SO4
- 新民主主义革命时期,中国领导人 民推翻三座大山,人民因而选择并拥戴中国的领导。在中国的领导下,结束了国家四分五裂、积贫积
- 已知在中,,分别是角所对的边. (1)求;w.w.w.k.s.5.u.c.o.m (2)若,,求的面积
- 2015年4月5日,欧洲核子研究中心宣布,欧洲大型强子对撞机正式开启第二阶段运行,将探索希格斯玻色子机制、暗物质、反物质
- Over the weekend , a single image of a boy reading to an ora





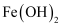 沉淀
沉淀 气体
气体 溶液的浓度
溶液的浓度


