第二单元 铁、铜的获取及应用 知识点题库
下列物质不属于合金的是( )
A . 硬铝
B . 水银
C . 不锈钢
D . 黄铜
中学化学中很多“规律”都有其使用范围,据有关“规律”下列结论合理的是( )
A . 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO
B . 金属钠可以通过电解熔融NaCl制得,推出金属铝可以通过电解熔融AlCl3制得
C . 金属钠在纯氧中燃烧生成Na2O2 , 推出金属锂在纯氧中燃烧生成Li2O2
D . CaCO3与稀硝酸反应生成CO2 , 推出CaSO3也能与稀硝酸反应生成SO2
出土的铜器文物表面有一层绿色的铜锈,铜锈的主要成分是( )
A . 碱式碳酸铜
B . 碳酸铜
C . 氢氧化铜
D . 氧化铜
有下列四个变化:①KClO3→KCl,②SiO2→H2SiO3 , ③Fe(OH)2→Fe(OH)3④Na→Na2O2 , 其中不能通过一步反应实现的是( )
A . 只有②
B . ②④
C . ③④
D . ①②
合金具有优良的物理、化学或机械性能,因而应用广泛.下列物质属于合金的是( )
A . 钢铁
B . 水银
C . 水晶
D . 金刚石
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A . NaClO(aq)  HClO(aq)
HClO(aq)  HCl(aq)
B . H2SiO3
HCl(aq)
B . H2SiO3  SiO2
SiO2  SiCl4
C . Al
SiCl4
C . Al  Al(OH)3
Al(OH)3  Al2O3
D . Fe2O3
Al2O3
D . Fe2O3  Fe(OH)3
Fe(OH)3  Fe2(SO4)3(aq)
Fe2(SO4)3(aq)
 HClO(aq)
HClO(aq)  HCl(aq)
B . H2SiO3
HCl(aq)
B . H2SiO3  SiO2
SiO2  SiCl4
C . Al
SiCl4
C . Al  Al(OH)3
Al(OH)3  Al2O3
D . Fe2O3
Al2O3
D . Fe2O3  Fe(OH)3
Fe(OH)3  Fe2(SO4)3(aq)
Fe2(SO4)3(aq)
治疗缺铁性贫血的常见方法是服用补铁药物,常采用更易被吸收的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水,但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中二价铁元素,设计并实施了如下实验:
![]()
试回答下列问题:
-
(1) 试剂1是,试剂2是。
-
(2) 该同学预测加入试剂2后,溶液应依然为浅绿色,但这与实际现象不符,请用离子方程式解释实际现象的合理性:,。
-
(3) 用离子反应方程式解释加入新制氯水后溶液变血红色的原因:。
-
(4) 补铁药物的说明书中通常会有“与VC同服可增加本品吸收”的内容,向淡红色溶液中加入VC , 片刻后溶液红色褪去,试从氧化还原角度解释补铁药物与VC同服的优点:。
将20g两种金属的混合物投入足量的稀硫酸中,反应完全后得到标准状况下H2 11.2L,则该混合物的组成可能是( )
A . Na和Fe
B . Mg和Cu
C . Al和Mg
D . Zn和Fe
某化学小组的同学取一定量的Al和Fe2O3的混合物进行铝热反应,并探究熔落物的成分。请回答下列问题:
-
(1) Ⅰ.引发铝热反应的实验操作是
-
(2) 做铝热反应时,内层纸漏斗底部剪一小孔用水润湿的目的是
-
(3) 反应的化学方程式为
-
(4) Ⅱ.已知:Al、Fe的熔、沸点数据如下:
物质
Al
Fe
熔点(℃)
660
1 535
沸点(℃)
2 467
2 750
某同学猜测,铝热反应所得到的熔落物是铁铝合金。理由:该反应放热能使铁熔化,而铝的熔点比铁低,所以铁和铝能形成合金。你认为他的解释是否合理?(填“合理”或“不合理”)。设计一个简单的实验方案,证明上述所得的熔落物中含有金属铝:
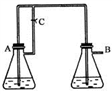
Fe(OH)2由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用图装置使用Fe,H2SO4(稀),NaOH溶液可在还原性气氛中制取Fe(OH)2白色沉淀,且较长时间内不变色,其中C为弹簧夹。(提示:还原性气氛如氢气环境)
-
(1) 则锥形瓶A中应加入的药品为。
-
(2) 锥形瓶B中应加入的药品为。
-
(3) 容器A中的反应开始后,请简单写出完成制备Fe(OH)2的后续操作步骤。。
-
(4) 若在反应开始之前先关闭弹簧夹C,则实验现象为:;请写出此时B瓶中发生的化学反应的离子方程式:。
下列描述中,不符合生产实际的是( )
A . 电解熔融的氧化铝制取金属铝
B . 在镀件上电镀锌,用锌作阳极
C . 电解法精炼粗铜,用纯铜作阳极
D . 电解饱和食盐水制烧碱,阳极室产生氯气
-
(1) 取少量Fe2O3粉末(红棕色)加入适量盐酸,发生反应的化学方程式:,反应后得到的溶液呈色。
-
(2) 用上述溶液分别做如下实验:取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为,此反应属于(填反应类型)。
-
(3) 在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈色,即制得Fe(OH)3胶体。
-
(4) 取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到烧杯中的液体产生丁达尔效应。这个实验可以用来区别。
-
(5) 用Fe(OH)3胶体进行下列实验:
①将其装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,这说明,这种现象称为。
②向其中加入饱和(NH4)2SO4溶液发生的现象是,原因是。
③提纯此分散系常用的方法是。
下列金属中,通常采用热还原法冶炼的是( )
A . Na
B . Al
C . Fe
D . Ag
在给定条件下,下列选项中所示的物质间转化均能实现的是( )
A . SiO2  H2SiO3
H2SiO3  Na2SiO3
B . S
Na2SiO3
B . S  SO2
SO2 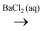 BaSO3
C . CuSO4
BaSO3
C . CuSO4  Cu(OH)2
Cu(OH)2 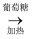 Cu2O
D . 饱和NaCl溶液
Cu2O
D . 饱和NaCl溶液  NaHCO3
NaHCO3  Na2CO3
Na2CO3
 H2SiO3
H2SiO3  Na2SiO3
B . S
Na2SiO3
B . S  SO2
SO2 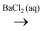 BaSO3
C . CuSO4
BaSO3
C . CuSO4  Cu(OH)2
Cu(OH)2 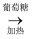 Cu2O
D . 饱和NaCl溶液
Cu2O
D . 饱和NaCl溶液  NaHCO3
NaHCO3  Na2CO3
Na2CO3
下列实验设计不能达到实验目的的是( )
| 实验目的 | 实验设计 | |
| A | 检验溶液中 | 取少量待测液,滴加 |
| B | 净化实验室制备的 | 气体依次通过盛有饱和 |
| C | 测定 | 将待测液滴在湿润的pH试纸上,与标准比色卡对照 |
| D | 工业酒精制备无水乙醇 | 工业酒精中加生石灰,蒸馏 |
A . A
B . B
C . C
D . D
由下列实验及现象不能推出相应结论的是( )
| 实验 | 现象 | 结论 | |
| A. | 向2mL0.1mol/LFeCl3的溶液中加足量铁粉,振荡,加1滴KSCN溶液 | 黄色逐渐消失,加KSCN溶液颜色不变 | 还原性:Fe>Fe2+ |
| B. | 将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 | CO2具有氧化性 |
| C. | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3显碱性 |
| D. | 将SO2通入酸性KMnO4溶液 | 紫色溶液褪色 | SO2具有还原性 |
A . A
B . B
C . C
D . D
聚合氯化铝铁[AlFe(OH)nCl6-n]m用于生活给水及工业给水的净化处理。以工业废料(Fe、Al、FeO、Fe2O3、Al2O3)为原料生产该产品的流程如下,下列说法错误的是( )
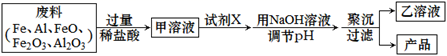
A . 产品中铁元素的化合价为+3
B . 甲溶液中一定存在的阳离子有H+、Al3+、Fe2+、Fe3+
C . 试剂X可以用H2O2 , 目的是将Fe2+氧化为Fe3+
D . 乙溶液呈酸性
元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系,下列说法正确的是( )
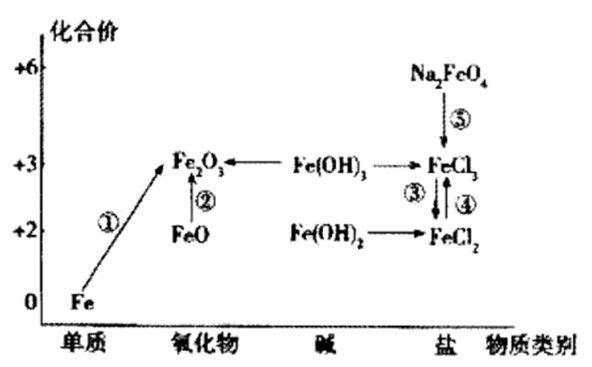
A . 铁与水蒸气在高温条件下反应可实现转化①
B . FeO是一种黑色粉末,不稳定,在空气中受热,迅速发生转化②生成红棕色粉末
C . 由图可预测:高铁酸钠(Na2FeO4)具有强氧化性,可用于消毒
D . 加入铁粉可实现转化③,加入碘水可实现转化④
某兴趣小组用油性笔在一小块覆铜板上写上“化学”,然后浸入盛有 溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干(如图)。对反应后的溶液进行分析,溶液中
溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干(如图)。对反应后的溶液进行分析,溶液中 与
与 之比为2∶3。下列说法不正确的是( )
之比为2∶3。下列说法不正确的是( )
 溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干(如图)。对反应后的溶液进行分析,溶液中
溶液的小烧杯中,过一段时间后,取出覆铜板,用水洗净并晾干(如图)。对反应后的溶液进行分析,溶液中 与
与 之比为2∶3。下列说法不正确的是( )
之比为2∶3。下列说法不正确的是( )

A . 反应后的溶液中: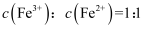 B . 反应的离子方程式为:
B . 反应的离子方程式为: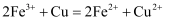 C . 反应后的溶液中:
C . 反应后的溶液中: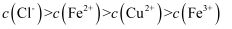 D . 反应后的溶液再生为
D . 反应后的溶液再生为 :加入足量铁粉,过滤,滤液中通入足量
:加入足量铁粉,过滤,滤液中通入足量
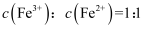 B . 反应的离子方程式为:
B . 反应的离子方程式为: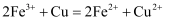 C . 反应后的溶液中:
C . 反应后的溶液中: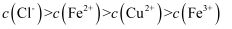 D . 反应后的溶液再生为
D . 反应后的溶液再生为 :加入足量铁粉,过滤,滤液中通入足量
:加入足量铁粉,过滤,滤液中通入足量
下列物质可由单质直接化合生成的是( )
A . 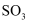 B .
B .  C .
C . 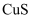 D .
D . 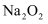
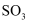 B .
B .  C .
C . 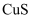 D .
D . 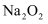
最近更新
- 已知向量{a,b,c}是空间的一个基底.求证:向量a+b,a-b,c能构成空间的一个基底.
- 赞泰州(3分) 泰州是一个新兴的城市,经过多年发展,地区特色日渐展现,旅游事业也越来越红火,许多外地游客纷纷慕名而来。要
- A、B两物体的质量之比mAmB=21,它们以相同的初速度v0在水平面上做匀减速直线运动,直到停止,其速度图象如图所示。那
- 通过一段时间的化学学习,你已经掌握了实验室制取气体的有关知识,请结合下列装置图,回答问题:(1)写出图中标有字母的仪器名
- 中国人以实现国家现代化为己任。中国最早提出实现国家工业化是在( ) A.中共七届二中全会
- 在容量瓶的使用方法中,下列操作正确的是( ) A、用容量瓶前必须对其进行干燥 B、用浓硫酸试样配制稀硫酸时,用
- 列提供了科技发展的四则信息,其中肯定错误的是()A.低温技术已有重大突破,1933年低温已达0.25K,1995年通过一
- 已知,则的展开式中常数项等于 .
- 2014年5月,中国与肯尼亚正式签署蒙内铁路项目合作协议。该铁路将由中国公司承建,中国的资金、技术、标准、装备制造和管理
- 已知日地距平比=(实际日地距离-日地平均距离)÷日地平均距离,它反映日地距离的变化情况。图示意日地距平比随时间的变化规律
- 下列估测的数据,最符合实际情况的是( ) A.某同学的体重约为500N B.教室里课桌高度约为1.6m
- Asthe saying goes,the moon________ always be full . A.ca
- 针对空气、水、土壤污染的严峻形势,中国的环境与资源保护,既要在全面治理污染的框架下通盘考虑,进行总体设计,又要突出重点、
- 把下列句子填在后面的横线上,组成语意连贯的一段话。(只填句子的序号)(4分)①被誉为“封建社会的百科全书”。②既带有浓郁
- 作文 请以“心灵深处的”为题,写一篇记叙文。 要求:(1)把题目补充完整,可填写“秘密”、“回忆”、“烦恼”、“快乐”、
- 给出两个命题:命题甲:关于x的不等式x2+(a-1)x+a2>0的解集为R;命题乙:函数f(x)=x3+9ax在区间[1
- 下列各句中,没有语病的一句是( ) A.可持续发展能力不断增强,生态环境得到改善,资源利用效率显著提高,促进了自然
- 计算的值.
- Go ________ the bridge,then you can get to the park.A.to
- 为测定某赤铁矿石中氧化铁的质量分数,小龙和他的同学用跑题的一氧化碳与10g赤铁矿石样品充分反应(杂质不参与反应),并将生
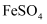 是否被氧化
是否被氧化 溶液,观察溶液颜色变化
溶液,观察溶液颜色变化
 溶液、浓
溶液、浓  的洗气瓶
的洗气瓶 溶液的pH
溶液的pH


