第二单元 铁、铜的获取及应用 知识点题库
①金属元素的原子只有还原性,离子只有氧化性
②金属元素在化合物中一般显正价
③金属性越强的元素相应的离子氧化性越弱
④金属元素的原子最外层电子数都少于4.
研究铜及其化合物的性质对科研、生产生活有重要的意义.
(1)铜可采用如下方法制备
①火法炼铜:Cu2S+O2 2Cu+SO2
2Cu+SO2
②湿法炼铜:CuSO4+Fe═FeSO4+Cu
上述两种方法中,铜元素均被 (填“氧化”或“还原”)成铜单质,若用①法每制得32gCu,转移电子的物质的量是 .
(2)在潮湿的空气中铜可以发生电化学腐蚀,生成铜绿,铜绿的化学式为 发生腐蚀的正极反应式为 ,由铜和锌组成的黄铜合金不易生锈,其防腐蚀的方法是 .
(3)①Li﹣﹣CuO电池总反应为:2Li+CuO═Li2O+Cu.电解质溶液为高氯酸锂有机溶液,电池的正极反应式为 .
②Cu2O是一种半导体材料,可在碱性溶液中用电解法制取,电解总反应式为:
2Cu+H2O Cu2O+H2↑,阳极反应式为 ;Cu2O投入稀硫酸中,得到蓝色溶液和红色沉淀,写出该反应的离子方程式 .
Cu2O+H2↑,阳极反应式为 ;Cu2O投入稀硫酸中,得到蓝色溶液和红色沉淀,写出该反应的离子方程式 .
(4)为了回收粗铜精炼后阳极泥中的Ag和Au,某实验小组查阅了有关资料如下表:
编号 | 常温下反应 | 化学平衡常数 |
反应甲 | Au+6HNO3⇌Au(NO3)3+3NO2↑+3H2O | <10﹣5 |
反应乙 | Au3++4Cl﹣⇌[AuCl4]﹣ | >105 |
从资料中可知,常温下金很难与硝酸反应,但却可溶于王水(浓硝酸与浓盐酸体积比为l:3的混合物).请你运用化学平衡移动原理,简要说明金能溶于王水的原因 .
(1)在试管I中加的试剂是
A.铁屑、稀H2SO4B.NaOH溶液
(2)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是 ,再关闭止水夹.
(3)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是 .

-
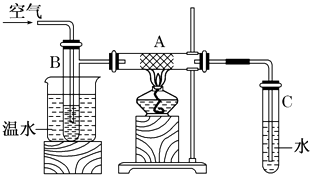
(1) 撤去A处酒精灯后铜丝仍然能保持红热的原因是;
-
(2) 反应后将试管C中的液体冷却,取出少量,加入到新制的Cu(OH)2悬浊液中,加热到沸腾可观察到现象是,写出反应的化学方程式.
①NH3 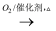 NO
NO 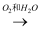 HNO3
HNO3
②浓HCl  Cl2
Cl2 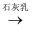 漂白粉
漂白粉
③MgCl2(aq)  无水MgCl2
无水MgCl2  Mg
Mg
④饱和NaCl(aq) 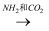 NaHCO3
NaHCO3  Na2CO3
Na2CO3
⑤铝土矿 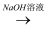 NaAlO2溶液
NaAlO2溶液 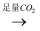 Al(OH)3
Al(OH)3  Al2O3
Al2O3  Al.
Al.
-
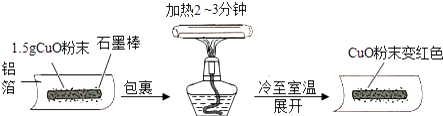
(1) 【猜想】把氧化铜还原成铜的物质是:Ⅰ石墨;Ⅱ.
-
(2) 【实验】用天平称量1.5g氧化铜粉末,直接用铝箔纸包裹.按上述操作步骤实验,黑色粉末,那么猜想Ⅱ不成立.
-
(3) 【实验】石墨棒能使氧化铜还原成铜,该反应的化学方程式为
-
(4) 【改进】把石墨棒换成铝粉重复上述操作,又获成功.那么称取等量的铝粉并进行同样的操作,其目的是.改进后的实验证明,金属铝与铜活动顺序是,该反应的化学方程式为
-
(5) 【拓展】如果使用复印机的“碳粉”代替石墨棒还原氧化铜,效果更好.联想在空气中灼烧的铁丝不能燃烧,而铁粉能燃烧,其原因是.
 2Fe+Al2O3
B . 2Ag2O
2Fe+Al2O3
B . 2Ag2O  4Ag+O2↑
C . Fe2O3+3CO
4Ag+O2↑
C . Fe2O3+3CO  2Fe +3CO2
D . 2MgO(熔融)
2Fe +3CO2
D . 2MgO(熔融)  2Mg+O2↑
2Mg+O2↑
-
(1) I.现有下列10种物质①熔融的氢氧化钠 ②蔗糖 ③纯净的盐酸 ④金属钠 ⑤硫酸 ⑥二氧化硫 ⑦硫粉 ⑧石膏(CaSO4·2 H2O) ⑨酒精溶液 ⑩液氨
属于电解质的有。
-
(2) 属于非电解质的有。
-
(3) 上述状态下能导电的有。
-
(4) 上述状态下的电解质不能导电的有。
-
(5) II.Fe(OH)2长时间露置于空气中发生变化的化学方程式为:。
偏铝酸钠溶液中通入足量二氧化碳反应的离子方程式为:。
-
(6) III.高纯度单晶硅可以按下列方法制备:
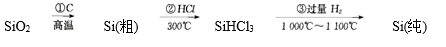
写出步骤①的化学方程式。
步骤②的产物经过冷凝后得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃),提纯SiHCl3主要操作的名称是。
-
(1) 无机非金属材料与我们的生活联系密切。我国具有独立知识产权的电脑芯片“龙芯一号”填补了我国计算机史上空白,“龙芯一号”材料的化学式为;传统的无机非金属材料在日常生活中有着广泛的运用。玻璃和水泥的生产中均用到的原料的名称是,其中碳酸钠在玻璃熔炉中反应的化学方程式为。
-
(2) 金属材料的应用更是广泛。工业常用30%FeCl3溶液腐蚀绝缘板上铜箔,制造印刷电路板。腐蚀废液中含有Fe3+、Fe2+、Cu2+离子。当向腐蚀液中加入足量的Fe粉,一定不存在的离子是;用实验判定腐蚀液中含有Fe2+离子。
 和
和 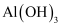 B .
B .  和NaCl
C .
和NaCl
C .  和
和 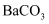 D .
D . 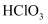 和
和 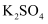
-
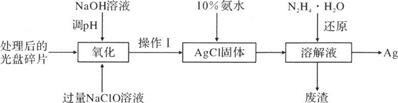
(1) NaClO溶液在受热或酸性条件下易分解,“氧化”阶段需在80℃条件下进行,适宜的加热方式为 。
-
(2) NaClO溶液与Ag反应的产物为AgCl、NaOH和O2 , 该反应的化学方程式为。有人提出以HNO3代替NaClO氧化Ag,从反应产物的角度分析,其缺点是。
-
(3) 操作Ⅰ的名称为。化学上常用10%的氨水溶解AgCl固体,AgCl与NH3·H2O按1:2反应可生成Cl-和一种阳离子的溶液(填阳离子的化学式)。实际反应中,即使氨水过量也不能将AgCl固体全部溶解,可能的原因是。
-
(4) 常温时N2H4·H2O(水合肼)在碱性条件下能还原(3)中生成的阳离子,自身转化为无害气体N2 , 理论上消耗0.1 mol的水合肼可提取到 g的单质Ag。
-
(5) 废旧电池中Ag2O能将有毒气体甲醛(HCHO)氧化成CO2 , 科学家据此原理将上述过程设计为原电池回收电极材料Ag并有效去除毒气甲醛。则此电池的正极反应式为 ,负极的产物有。
已知:①K2FeO4为紫色固体,微溶于KOH溶液;
②  具有强氧化性,在酸性或中性溶液中能快速产生O2 , 在碱性溶液中较稳定。
具有强氧化性,在酸性或中性溶液中能快速产生O2 , 在碱性溶液中较稳定。
-
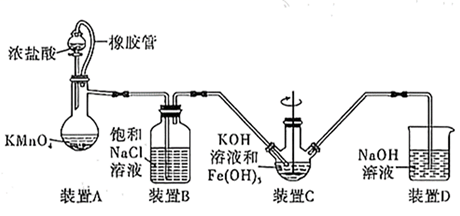
(1) 制备K2FeO4(夹持装置咯)
①如图所示,A为氯气发生装置,装置A中盛放KMnO4的仪器名称是。
②装置C中的KOH溶液需过量,目的是。
③C中得到紫色固体和溶液,则C中Cl2与Fe(OH)3发生反应生成K2FeO4的离子方程式为 ,此外Cl2还与过量的KOH反应。
-
(2) 探究K2FeO4的性质
甲同学取装置C中紫色溶液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2。该现象不能证明“酸性条件下
 氧化性强于Cl2”,其理由是:。
氧化性强于Cl2”,其理由是:。 -
(3) 测定K2FeO4的产率
若在制备装置C中加入Fe(OH)3的质量为10.7g,充分反应后经过滤、洗涤、干燥得K2FeO4固体10.3g,则K2FeO4的产率为(保留3位有效数值)。
①Cu 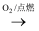 CuO
CuO  Cu(NO3)2
Cu(NO3)2
②Si 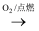 SiO2
SiO2  H2SiO3
H2SiO3
③Al2O3  Na[Al(OH)4]
Na[Al(OH)4] 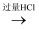 AlCl3
AlCl3
④Fe 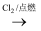 FeCl3
FeCl3 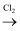 FeCl3
FeCl3
 B .
B .  ↑
C .
↑
C .  D .
D .  ↑
↑
- __________your compositions carefully and some spelling mist
- 阅读《晒月亮》,回答问题。晒 月 亮 池 莉常熟有一座山,叫做虞山。虞山有一座寺,叫做兴福寺。兴福寺有一把年
- (8分)完成下列填空: (1)鲸鱼、蘑菇、杨树、珊瑚虫等有很多的差别,但都属于生物,因为它们具有生物的共同特征:_
- 在一个固定体积的密闭容器中,加入2 mol A和1 mol B,发生反应:2A(g)+B(g)3C(g)+D(g)达到平
- 影响图中海南岛铁路线分布的主要自然因素是 A.河流 B.地形 C.气候
- 下列各句中加点的熟语使用恰当的一句是( )A.为了解决建筑公司拖欠民工工资问题,赵记者跑东跑西,找民工调查,找有关部
- 关于经纬度的变化规律正确说法是( ) A.以0°经线为界,东经和西经的度数分别向西、向东愈来愈大 B.以180°经
- 如果某日某时刻120°E与晨昏线的一部分重合,则该日可能是( ) A.秋分日 B.夏至日
- (06年山西卷)下列各句中,没有语病的一句是 A.青藏铁路纵贯青海、西藏两省区,跨越青藏高原,是连接西藏与内地的一条
- Read the sentencecarefully and you’ll see you’ve____a verb i
- 以下是某高校应届毕业生张欣同学写给某公司的求职信,从语言使用得体的要求看,存在五处不当,请按要求予以修改。 尊敬的领导:
- 随着世界经济的发展,二氧化碳的排放量不断增加。目前,碳排放已成为全球普遍关注的问题。图是21世纪初某年世界部分国家碳排放
- (1)根据下列离子方程式,写出相应的化学方程式: ①Ca2++CO===CaCO3↓__________________
- 近年来,我们党和国家在少数民族和民族地区实施了延边开放战略、“八七”扶贫攻坚计划、西部大开发战略等。这 ①表明我国坚持和
- 20世纪初,有学者认为,“张三李四是同时人。张三记了古典来做古文;李四又记了古典,去读张三做的古文。我想:古典是古人的时
- 下列光学器材中,可以成倒立、放大实像的是A.照相机 B.幻灯机 C.放大镜 D.平面镜
- 在化学反应前后,肯定不变的是 A.物质的种类 B.原子的种类 C.分子的种类D.物质的状态
- 运动物体在一段时间t内发生位移的大小取决于下列的哪一个物理量?A.物体的平均速度B.物体的初速度C.物体的末速度 D.物
- 已知向量 ,若∥, 则=_____________.
- 材料一:为加快转型发展,某市委市政府组织考察了天津、唐山,对比“天津速度”、“唐山效率”,发现情况如下: 【情况一



