第二单元 铁、铜的获取及应用 知识点题库
向Fe2O3和铁粉组成的混合物中,加入量的稀H2SO4 , 各物质恰好完全反应,测得溶液中不含Fe3+ , 且Fe2+与H2的物质的量之比为4:1,那么在反应中,Fe2O3、Fe、H2SO4的物质的量之比为( )
A . 1:1:1
B . 1:2:4
C . 1:2:3
D . 2:3:5
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
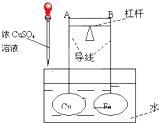
A . 杠杆为导体和绝缘体时,均为A端高,B端低
B . 杠杆为导体和绝缘体时,均为A端低,B端高
C . 当杠杆为绝缘体时,A端低,B端高;为导体时,A端高,B端低
D . 当杠杆为绝缘体时,A端高,B端低;为导体时,A端低,B端高
下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是( )
A . CuCl2
B . FeCl2
C . FeCl3
D . AlCl3
下列有关说法正确的是( )
A . 氮氧化合物、PM 2.5颗粒、CO2都会导致酸雨
B . 氯水和二氧化硫混合使用能增强漂白效果
C . 硫酸铜溶液可用于泳池消毒是利用了Cu2+能使蛋白质盐析
D . 轮船上挂锌锭防止铁腐蚀属于牺牲阳极的阴极保护法
5.76g部分氧化的Fe、Cu合金样品(氧化产物为Fe2O3、CuO),经如下处理,下列说法正确的是( )

A . V=224
B . 样品中Fe的质量为2.14 g
C . 未氧化前Fe元素的质量分数约为41.2%
D . 样品中CuO的质量为3.52 g
下列有关化学物质的俗称错误的是( )
A . 碳酸钠的俗称是纯碱
B . 四氧化三铁的俗称是磁性氧化铁
C . 氧化铁的俗称是铁红
D . 碳酸氢钠的俗称是苏打
某强酸性溶液X中可能含有Fe2+、Fe3+、Al3+、Ba2+、NH4+、CO32-、NO3-、SO42-、SiO32-中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。实验过程中有一种气体为红棕色。
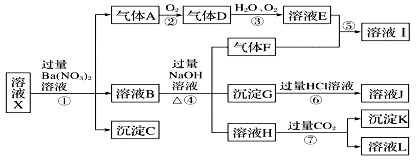
根据以上信息,回答下列问题:
-
(1) 由强酸性条件即可判断X溶液中肯定不存在的离子有。
-
(2) 溶液X中关于硝酸根离子的判断,正确的是(填编号,下同)。
a.一定含有
b.一定不含有
c.可能含有
-
(3) 气体F的电子式为,化合物I中含有的化学键类型有。
-
(4) 转化①的离子方程式为。
转化⑦的离子方程式为。
-
(5) 对不能确定是否存在的离子,可以另取X溶液,加入下列溶液中的一种,根据现象即可判断,该试剂最好是。
①NaOH溶液 ②KSCN溶液 ③氯水和KSCN的混合溶液 ④pH试纸 ⑤KMnO4溶液
下列铁的化合物中,含Fe元素的质量分数最小的是( )
A . FeO
B . Fe2O3
C . Fe3O4
D . FeS2
铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
-
(1) 向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是nm。
-
(2) 电子工业需要用30 %的FeCl3溶液腐蚀敷在绝缘板上的铜片制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式。某同学对FeCl3腐蚀铜后所得溶液的组成进行测定:取少量待测溶液,滴入KSCN溶液呈红色,则溶液中所含金属阳离子有。
-
(3) 若要验证该溶液中含有Fe2+ , 正确的实验方法是________(用字母代号填)。
A . 向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe2+。 B . 向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+。 C . 向试管中加入试液,先滴入KSCN溶液,无现象,再滴加氯水,若显血红色,证明原溶液中含有Fe2+ -
(4) 欲从废液中回收铜,并重新获得FeCl3溶液设计实验方案如下:
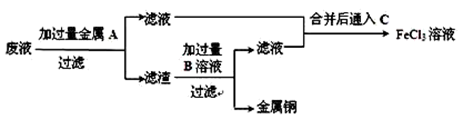
①写出上述实验中有关物质的化学式:A:;B:。
②写出通入 C的化学方程式
下列金属单质,不能在特定条件下和水反应的是( )
A . 镁
B . 钠
C . 铁
D . 银
FeCl2具有独有的脱色能力,适用于印染、造纸行业的污水处理。FeCl3在加热条件下遇水剧烈水解。FeCl3和FeCl2均不溶于C6H5Cl、C6H4Cl2、苯。回答下列问题:
-
(1) 由FeCl3∙6H2O制得干燥FeCl2的过程如下:
i.向盛有FeCl3∙6H2O的容器中加入过量SOCl2(液体,易水解),加热,获得无水FeCl3。
ii.将无水FeCl3置于反应管中,通入一段时间的氢气后加热,生成FeCl2。
①FeCl3∙6H2O中加入SOCl2获得无水FeCl3的化学方程式为。(已知该反应为非氧化还原反应)
② ii中通入一段时间的氢气后再加热的目的是。
-
(2) 利用反应2FeCl3 + C6H5Cl
 2FeCl2+ C6H4Cl2 +HCl↑,制取无水FeCl2。在三颈烧瓶中加入无水氯化铁和过量的氯苯,控制反应温度在一定范围内加热3 h,冷却、分离、提纯得到粗产品,实验装置如图。(加热装置略去)
2FeCl2+ C6H4Cl2 +HCl↑,制取无水FeCl2。在三颈烧瓶中加入无水氯化铁和过量的氯苯,控制反应温度在一定范围内加热3 h,冷却、分离、提纯得到粗产品,实验装置如图。(加热装置略去) 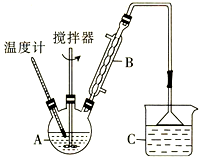
①仪器B的名称是 。反应前需向A中通入N2的目的是。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经、、干燥后,得到FeCl2粗产品。
③该装置存在的不足之处是。
-
(3) FeCl2的纯度测定。
①取a g样品配制成100 mL溶液;③用移液管移取所配溶液5.00mL,放入500 mL锥形瓶内并加水200mL;③往上述锥形瓶中加入硫酸锰溶液20.00 mL,用0.1 mol∙L-1酸性KMnO4标准溶液滴定,终点时消耗酸性KMnO4标准溶液V mL。滴定至终点的判断依据是。若所配溶液中ω(FeCl2)=kV(V为消耗的酸性高锰酸钾标准溶液的毫升数)g·L-1 , k=。
化学与生活、生产、科技密切相关。下列说法错误的是( )
A . 地下钢铁管道用导线连接锌块可以减缓管道的腐蚀
B . 中国天眼传输信息用的光纤材料是硅
C . 研发新能源汽车,减少化石燃料的使用,与“绿水青山就是金山银山”的绿色发展理念一致
D . 港珠澳大桥用到的合金材料,具有强度大、密度小、耐腐蚀等性能
现有下列8种物质:①AgCl ②Al ③液态醋酸 ④SO2 ⑤Ba(OH)
2固体 ⑥NaHCO3固体⑦稀硝酸 ⑧熔融FeCl3
-
(1) 上述状态下可导电的是(填序号,下同);属于电解质的是。
-
(2) 上述8种物质中,有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为:。
-
(3) 写出用⑧的饱和溶液制备Fe(OH) 3胶体的离子方程式:。
由一种阳离子与两种酸根阴离子组成的盐称为混盐,CaOCl2是一种常见的混盐。下列说法错误的是( )
A . CaOCl2有较强的氧化性
B . 该混盐可能具有漂白性
C . 由氯气和石灰乳为原料,每生成1mol CaOCl2 , 转移的电子为2mol
D . CaOCl2的溶液中加入足量浓硫酸,可有黄绿色的气体产生
能源是人类可持续发展面临的重要问题,某科学家设计的UT-3热化学循环如下图所示:
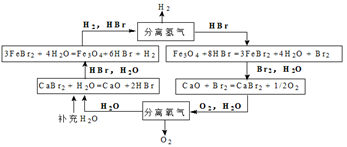
该过程最终制得的能源气体是( )
A . H2
B . O2
C . HBr
D . Br2
某废催化剂含SiO2、ZnS、CuS及少量的Fe3O4。某实验小组以废催化剂为原料,进行回收利用。设计实验流程如图:
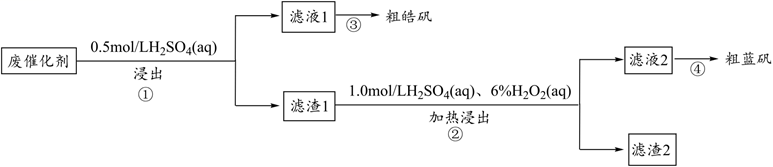 已知:CuS既不溶于稀硫酸,也不与稀硫酸反应。下列说法正确的是( )
已知:CuS既不溶于稀硫酸,也不与稀硫酸反应。下列说法正确的是( )
A . 步骤①操作中,生成的气体可用碱液吸收
B . 滤液1中是否含有Fe2+ , 可以选用KSCN和新制的氯水检验
C . 滤渣1成分是SiO2和CuS,滤渣2成分一定是SiO2
D . 步骤④要滴加稀硫酸防止CuSO4水解
为了防止FeSO4被氧化而变质,实验室在配制FeSO4溶液时,常在溶液中加入少量的( )
A . 铜粉
B . 铁粉
C . 锌粉
D . H2SO4
化学与生活、生产息息相关,下列说法正确的是( )
A . 氧化铁可以用作外墙涂料
B . 二氧化硅可以用作干燥剂
C . 二氧化硫常常用作食品增白
D . 氢氧化铝常用作高温耐火材料
下列关于古籍中的记载说法错误的是( )
A . 《天工开物》中“凡石灰,经火焚炼为用”涉及的反应类型是分解反应
B . 制造“司母戊鼎”的青铜和举世轰动的“超级钢”均属于合金
C . 《肘后备急方》中“青蒿一握,以水二升渍,绞取汁,尽服之”该过程属于化学变化
D . 诗句“千锤万凿出深山,烈火焚烧若等闲”描述的变化属于化学变化
草酸亚铁晶体是生产感光材料的原料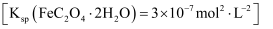 , 制备流程如下:
, 制备流程如下:
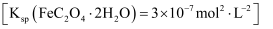 , 制备流程如下:
, 制备流程如下: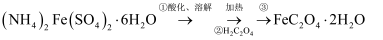
下列说法错误的是( )
A . 可用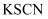 溶液检验
溶液检验 是否变质
B . 步骤①酸化的目的是抑制
是否变质
B . 步骤①酸化的目的是抑制 的水解
C . 步骤②反应为
的水解
C . 步骤②反应为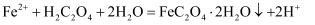 D . 步骤③为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
D . 步骤③为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
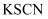 溶液检验
溶液检验 是否变质
B . 步骤①酸化的目的是抑制
是否变质
B . 步骤①酸化的目的是抑制 的水解
C . 步骤②反应为
的水解
C . 步骤②反应为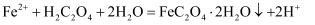 D . 步骤③为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
D . 步骤③为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
最近更新
- 下列关于“百花齐放,百家争鸣”方针的表述不正确的是 A.在艺术上“百花齐放”,在学术上“百家争鸣” B.学者在学术上有独
- 不等式组的解集在数轴上表示正确的是( )
- 图为某一时刻太阳高度等值线图,图中阴影部分为4月30日。读图完成题一飞机从M点沿最短距离飞往P点,其飞行方向是 (
- 在美国历史上被誉为“开国元勋”和黑奴解放者的两位总统是( )A.华盛顿、林肯B.杰佛逊、杜鲁门C.罗斯福、里根D.罗
- 增加:在缺词处加一个漏字符号(∧),并在其下面写出该加的词。 删除:把多余的词用斜线〔〕划掉。 修改:在错的词下划一横线
- 阅读下面的文言文,完成后面题。 王凌字彦云,太原祁人也。凌举孝廉,为发干长,稍迁至中山太守,所在有治,太祖辟为丞相掾属。
- 下列与《物种起源》中“物种变异、逐步进化”蕴涵的哲理一致的是 ①量变与质变的辩证关系 ②肯定与否定的辩证关系 ③物质与意
- 在△ABC中 ,B=120°,AC=7,AB=5,则△ABC的面积为________.
- Will you _______ finish your homework before eight this even
- 学习物质性质时,我们常对物质从不同的角度进行分类.现有某同学将氢气、一氧化碳、铁、红磷、水、二氧化碳共六种物质进行如下分
- 阅读下面的文字,完成小题。 丝绸之路的历史变迁与当代启示 古代丝绸之路,从时间上看,跨越2000多年,历经先秦、汉唐、宋
- 配制一定物质的量浓度的某溶液,下列情况会使配制结果偏低的是( ) A.未冷却即转移、定容
- —It’s necessary and important forthem students at school to
- 1931年初,苏联接受外国技术援助的项目已达124项,大部分是美、德两国提供的,同年,苏联向外国购买的机器设备约占世界设
- ,自缘身在最高层。(王安石《登飞来峰》)
- 已知则a,b的大小关系是(). A.a>b B.a=b
- 属于我国内海的是( ) A.渤海、黄海 B.渤海、琼州海峡 C.黄海、东海 D.东海、琼州海
- Here ______ three ______ of hisfamily. A. is;photoes
- 2.依次填入下列各句横线处的成语,最恰当的一组是( ) ①真正的长者并不是 ,他们常常通过一言一行,一颦
- 函数y=的定义域是( )A.(1,2] B.(1,2)C.(2,+∞)



