实验2-6 氢氧化铝的制备 知识点题库
在以上成分中,有一种属于两性物质,试分别写出该两性物质与盐酸、氢氧化钠溶液反应的化学方程式: .
取足量的形状、质量均相同的铝丝分别与等体积的6mol/L的盐酸、6mol/L氢氧化钠溶液反应,待反应停止后取出剩余的铝丝洗净、干燥、称量,剩余铝丝的质量关系是前者 后者(填“大于”或“小于”或“等于”);观察反应后的液体,发现铝与盐酸反应后所得的液体是黑色浑浊的,试管底部有少量黑色沉淀,对此现象,同学们进行了如下探究:
(1)提出猜想
同学们查找资料后获得如下信息:工业上用电解法冶炼铝所用的原料氧化铝是从铝土矿中提取的,所以得到的氧化铝中可能还含有微量的氧化铁和二氧化硅两种杂质,据此,同学们提出如下猜想:
猜想1:此黑色固体是铁单质,可能是电解得到的铝与杂质反应生成的,相应的化学反应方程式为 ;
猜想2:
猜想3:此黑色固体是铝单质,是铝与盐酸反应时因反应过快而变成粉末分散到溶液中;
猜想4:此黑色固体可能是上述若干种单质组成的混合物.
(2)设计实验方案并完成相关实验:
实验步骤 | 实验现象 | 结论 |
①将反应后所得的液体进行过滤、洗涤,分别取少量固体置于两支试管中 | _ | _ |
②向其中的一支试管中加入足量的稀盐酸,观察固体是否溶解. | 固体完全溶解 | 证明猜想 一定不正确. |
③向另一试管中加入足量的 溶液,观察固体是否溶解. | 固体完全溶解 | 猜想 一定不正确. |
得出结论:综合实验②③的现象,可推知猜想 是正确的. | ||
固体溶解在氢氧化钠溶液中的离子方程式为: .
 ,则与过量NH3•H2O也生成AlO
,则与过量NH3•H2O也生成AlO  B . Na2O2与CO2反应生成Na2CO3和O2 , 则与SO2反应可生成Na2SO3和O2
C . Fe与Cl2反应生成FeCl3 , 则与I2反应可生成FeI3
D . Al与Fe2O3能发生铝热反应,则与MnO2也能发生铝热反应
B . Na2O2与CO2反应生成Na2CO3和O2 , 则与SO2反应可生成Na2SO3和O2
C . Fe与Cl2反应生成FeCl3 , 则与I2反应可生成FeI3
D . Al与Fe2O3能发生铝热反应,则与MnO2也能发生铝热反应
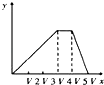 B .
B . 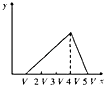 C .
C . 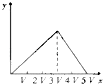 D .
D . 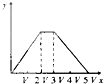
X | Y | Z | W | |
A | C | CO | CO2 | O2 |
B | Na | Na2O | Na2O2 | O2 |
C | AlCl3 | Al(OH)3 | NaAl(OH)4 | NaOH |
D | Fe | FeCl2 | FeCl3 | Cl2 |
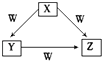
①加盐酸溶解 ②加NaOH溶液 ③过滤 ④加盐酸生成Al(OH)3
⑤通入过量CO2生成Al(OH)3 ⑥加过量氨水生成Al(OH)3 .
①AlCl3和氨水 ②Na2CO3与盐酸 ③AlCl3和NaOH溶液 ④Fe与氯气(点燃)
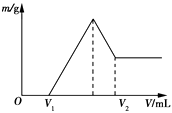
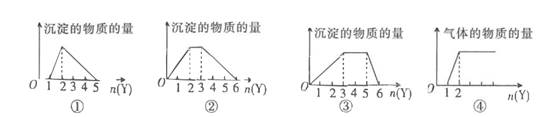
-
(1) 比较相同条件下微粒得到电子的能力Fe3+Cu2+(填“>” 、“<”或“=”)
-
(2) 已知Mg3N2遇水会剧烈反应生成白色沉淀和有刺激性气味的气体,写出Mg3N2与足量稀盐酸反应的化学方程式。
-
(3) 相同条件下冰的密度比水小,主要原因是 。
- 选出下列句中括号中的成语使用正确的一项是( ) A.学习一直第一的小明(激流勇退),成绩下降到了十五名。 B.我厂的制度
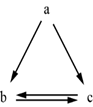
- 已知A、B可发生中和反应.在常温下D为液体,X是目前应用最广泛的金属,Y常 用作食品干燥剂.各物质间的转化关系如图所示
- 为和清华争夺优质生源,2009年11月8日,北大招办宣布试行自主招生“中学校长实名推荐制”。方案一经公布,便吸足了国内媒
- 。......
- 如图是一个反射弧的部分结构图,甲、乙表示连接在神经纤维上的电流表。当在A点以一定的电流刺激,甲、乙电流表的指针发生的变化
- 下列各项有两个错别字的是A.紧俏 羸弱 呕心沥血 哀声叹气 B.谄媚 诡奇 睥睨 冠冕堂煌C.慰
- 光线进人眼内,成像于眼球的哪一结构 A.角膜 B.晶状体 C.玻璃体 D.视网膜
- 函数y=ax(a>0且a≠1)在[1,2]上的最大值比最小值大,则a=______________.
- 下列各句中,没有语病的一句是(3分) A.市委下发了《关于开展向刘秉毅同志学习活动的决定》,号召全市广大党员干部向刘 秉
- 请分析回答下列有关生物技术实践方面的问题: Ⅰ.现有磨浆机、烧杯、滴管、量筒、玻璃棒、漏斗、纱布、苹果、试管、蒸馏水、质
- 党的“十六大”以来,我们党对社会和谐的认识不断深化,明确了构建社会主义和谐社会在中国特色社会主义事业总体布局中的地位。随
- 14.补写出下列句子中的空缺部分。 (1)桑之未落, 。
- 在△ABC和△A'B'C'中有①AB=A'B',②BC=B'C',③AC=A'C',④∠A=∠A', ⑤∠B=∠B',⑥
- 下列排列顺序正确的是
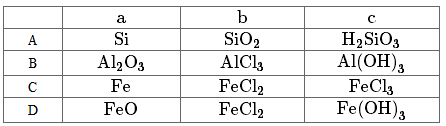
- 下列不是离子化合物的是() A. B. C. D.
- 图一是八月份某一晴天,一昼夜中棉花植株CO2的吸收和释放曲线;图二表示棉花叶肉细胞两种细胞器的四种生理活动状态。请分别指
- 人的心电图的出纸速度(纸带移动的速度)是2.5 cm/s,记录下的某人的心电图如图11-2-6所示。图纸上每格边长为5
- 我国古代某位君主亲身示范农耕以示重视农业技术推广的态度,使用右图所示工具最早的君主是 A.汉高祖
- 1989年,第七届全国人民代表大会第二次全体会议通过了《中华人民共和国行政诉讼法》。这是一部里程碑式的法律,标志着“民告
- 阅读《论语》中的一段文字,然后回答问题。 子之武城①,闻弦歌之声。夫子莞尔而笑,曰:“割鸡焉用牛刀?”子游对曰:“昔者偃



