实验2-6 氢氧化铝的制备 知识点题库
甲、乙两个探究性学习小组,拟在实验室中通过铝与足量的稀硫酸反应生成的氢气来测定铝的摩尔质量.
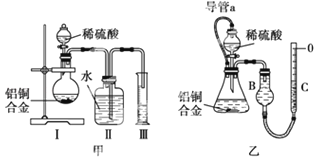
甲组同学拟设计如图甲所示的装置完成实验.
(1)实验前如何检验Ⅰ装置的气密性 .
(2)写出装置Ⅰ中发生反应的离子方程式: ;实验中使用铜铝合金的目的是 .
(3)乙组同学仔细分析了甲组同学的实验装置后认为:稀硫酸滴入烧瓶中,即使不生成氢气,也会将瓶内的空气排出,使所测氢气的体积偏大;实验结束后,连接广口瓶和量筒的导管中有少量水存在,使所测氢气的体积偏小.于是他们设计了如图乙所示的实验装置.装置中导管a的作用是① ;② .
(4)乙组同学在实验中准确测出4个数据,如下表:
实验前 | 实验后 | |
铝铜合金质量/g | m1 | m2 |
量液管(C)液面读数/mL | V1 | V2 |
如果实验条件下的气体的摩尔体积是24.5L•mol﹣1 , 利用上述数据写出铝的摩尔质量的表达式:M= g•mol﹣1 .
(5)若将铝铜合金溶解,下列试剂中最好选用 (填编号);理由是 .
a.浓硫酸 b.稀硫酸 c.稀硝酸 d.硫酸铁溶液.
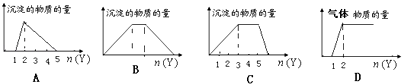
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3( )
-
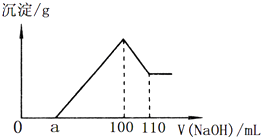
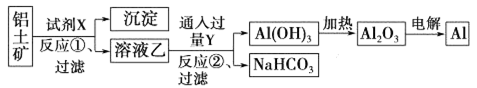
(1) 硫酸的物质的量浓度是多少?
-
(2) 若a=10,矿石样品中Fe2O3的质量是多少?
-
(3) 试计算a的取值范围.
-
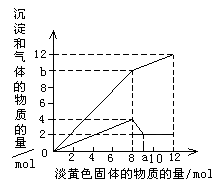
(1) 淡黄色固体是。
-
(2) 可知溶液中一定没有的离子是,理由是。
-
(3) 请解释为什么在投入8mol淡黄色固体后,产生气体的量在减少。
-
(4) 写出淡黄色固体加入的量为8mol到10mol之间发生的所有离子方程式。
-
(5) 所含离子的物质的量之比为。
下列叙述正确的是( )
| 选项 | 实验 | 解释或结论 |
| A | 向NaAlO2溶液中逐渐通入CO2气体,先出现白色胶状沉淀,继续通入CO2气体,白色胶状沉淀不溶解 | Al(OH)3是两性氢氧化物,不溶于碳酸溶液 |
| B | 在新制氯水中加入碳酸钙粉末,充分搅拌,氯水的漂白性增强 | 碳酸钙是催化剂 |
| C | 用蒸馏法能将溶解在CCl4中的碘分离出来 | 因为碘易升华,先分离出来 |
| D | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,则溶液变为黄色 | 氧化性:H2O2>Fe3+ |
-
(1) Ⅰ.钢(一种铁碳合金)是用量最大、用途最广的合金。其中,中碳钢中碳的含量范围为。超级钢的开发与应用已成为国际钢铁领域的研究热点,是钢铁领域的一次重大革命。我国的超级钢研究已居于世界领先地位,我国研制的这种超级钢中含(填元素符号)10%、C 0.47%、Al 2%、V 0.7%,这种超级钢强度很大,在应用时能够实现钢板的轻薄化。
-
(2) Ⅱ.FeSO4可作补血剂,用于治疗缺铁性贫血症。用FeSO4溶液制备Fe(OH)2的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的原因是为了防止Fe(OH)2被氧化,写出其被氧化的化学反应方程式。
-
(3) Ⅲ.高铁酸钾(K2FeO4)是一种新型、高效、无毒的多功能水处理剂。查阅资料已知:K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2 , 在碱性溶液中较稳定。
制备K2FeO4
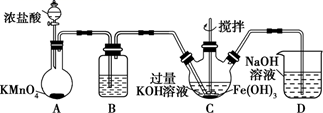
①在装置A中发生的化学反应中HCl显示出来的性质为。
②C为制备K2FeO4装置,写出次氯酸钾与氢氧化铁在碱性环境中反应的离子方程式:。
-
(4) 探究K2FeO4的性质。取C中浅紫红色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2 , 设计如下方案:取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。由方案中溶液变红可知a中含有Fe3+ , 该离子的产生不能判断一定是由K2FeO4被Cl-还原而形成的,原因是。
-
(5) 使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:□FeO
 +□H+=□O2↑+□Fe3++□_
+□H+=□O2↑+□Fe3++□_ ①完成并配平上述离子方程式(方框内填化学计量数,横线上写物质)。
②现取C中洗涤并干燥后样品的质量10 g,加入稀硫酸,收集到0.672 L气体(标准状况)。则样品中高铁酸钾的质量分数为。(计算结果保留到0.1%)
|
选项 |
性质 |
用途 |
|
A |
CCl4难溶于水,难于燃烧 |
CCl4常用作有机溶剂和灭火剂 |
|
B |
Al2O3既能与强酸反应,又能与强碱反应 |
Al2O3常用作耐高温材料 |
|
C |
SiO2透明,折射率合适,能够发生全反射 |
SiO2用作光导纤维材料 |
|
D |
Cl2具有漂白性 |
常用Cl2对自来水进行杀菌消毒 |
- 豆腐起源于我省淮南八公山。食用豆腐能获得人体所需要的多种氨基酸,其中含量最多的是亮氨酸(化学式:C6H13NO2)。下列
- 下列各组动物中,都用鳃呼吸的是() A.河蚌、鲨鱼、海马 B.鲸、蛇、乌鱼
- There is a new problem involved in the popularity of private
- A、B、C三质点同时同地沿一直线运动,其s-t图象如图1所示,则在0~t0这段时间内,下列说法中正确的是
- 根据下列实验装置图,回答下列问题.(1)写出标号仪器的名称:a ;b . (2)实验室用A制取氧气,试管内所装的药品
- 古人对某一历史时期的政治格局进行了描述:“溥(普)天之下,莫非王土,率土之滨,莫非王臣”,“礼乐征伐自天子出”,该政治格
- -- According to my grandma, it is a good idea to eat chicke
- 已知,一元二次方程x2﹣8x+15=0的两根分别是⊙O1和⊙O2的半径,当⊙O1和⊙O2相切时,O1O2的长度是() A
- 对溺水者先要清除他口鼻内的污物,再进行人工呼吸。这样可以A.保持呼吸道通畅
- 美国“遏制共产主义”的措施不包括 A.提出“杜鲁门主义”B.实施马歇尔计划 C.成立北大西洋公约组织 D.成
- 为贯彻落实党的十七大和总书记今年视察安徽时的重要指示精神,安徽省委、省政府决定设立合芜蚌自主创新综合配套改革试验区,积极
- 在DNA测序工作中,需要将某些限制性核酸内切酶的限制位点在DNA上定位,使其成为DNA分子中的物理参照点,这项工作叫做“
- 已知函数f(x)=(1-3m)x+10(m为常数),若数列{an}满足an=f(n)(n∈N*),且a1=2,则数列{a
- “稻花香里说丰年,听取蛙声一片”的景象已越来越少.下列各项中,不属于造成蛙类大量减少的主要原因的是( ) A.栖
- 24、某文艺团体为“希望工程”募捐组织了一场义演,共售出1000张票,筹 出票款6920元,且每张成人票8元,学生票
- When you go outing with your sisters you must see to ______
- 近期我国将采取渐进、微调、各省不同步的方式推开单独二胎政策,可能带来的影响有 ( ) A、缓解目前我国劳动力短缺状况
- 阅读下面的一段话,完成后面习题 苏州园林栽种和修剪树木也着眼在画意。高树与低树俯仰生姿。落叶树与常绿树相间,花时不
- 脍炙人口的唐诗深受人们喜爱,唐代诗人辈出。郭沫若:“世上疮痍,诗中圣哲;民间疾苦,笔底波澜。”他赞誉的是:A.李白B.杜
- 美国在20世纪90年代进入了新经济时代,其主要特征是 A.信息化和全球化



