实验2-6 氢氧化铝的制备 知识点题库
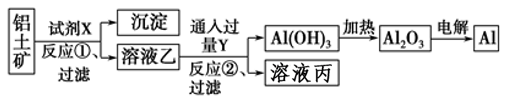
铝是一种重要的金属,在生产、生活中具有许多重要的用途.眉山市电解铝厂位于三苏故里修文乡,现已经形成年产33万吨电解铝,配套年产15万吨阳极碳块的规模.该厂用铝土矿为原料制备铝的工艺流程如下:
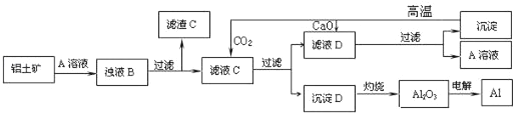
已知:①铝土矿的主要成分是 Al2O3 , 此外还含有少量CuO、Fe2O3 等杂质.②电解冶炼铝时用碳棒作阳极,用Na3AlF6作助熔剂,电解熔融的Al2O3 .
回答下列问题:
(1)写出铝土矿与 A 溶液反应的化学方程式 .
(2)滤渣 C的主要成分为 ;实验室过滤时使用的玻璃仪器有 .
(3)生成过程中,除CaO、H2O可以循环使用外,还可以循环使用的物质有 (填化学式).
(4)写出过量CO2通入滤液C生成D的离子方程式 .
(5)若生产54吨铝,放出平均摩尔质量为36g•mol﹣1的气体(经测定气体中不含O2),则消耗阳极 吨.
-
(1) 常作为潜水艇和呼吸面具中氧气的淡黄色固体是;
-
(2) 常用于焙制糕点,也可用作抗酸药的是;
-
(3) 属于两性氧化物的是;
-
(4) 属于红棕色固体是.
①Na2CO3溶液 ②NH4HCO3溶液 ③NaHCO3溶液 ④NaHSO4溶液 ⑤Al ⑥Al(OH)3 ⑦Al2O3 ⑧SiO2 .
A | B | C | D | |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
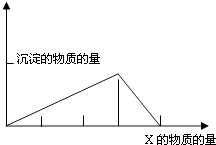
①NaAlO2(aq)  Al(OH)3
Al(OH)3  Al2O3(熔融)
Al2O3(熔融)  Al
Al  Fe
Fe
②S  SO3
SO3  H2SO4
H2SO4
③Cu2(OH)2CO3  CuCl2(aq)
CuCl2(aq)  Cu
Cu
④FeO3  FeCl3
FeCl3  无水FeCl3
无水FeCl3
⑤饱和NaCl(aq)  NaHCO3
NaHCO3  Na2CO3 .
Na2CO3 .
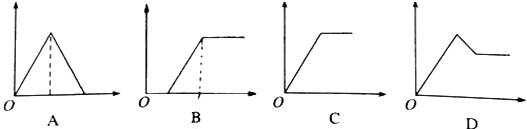
-
(1) 表示向饱和AlCl3溶液中滴加氨水至过量的是,离子方程式:.
-
(2) 表示向Na2CO3溶液中滴加盐酸溶液至过量的是,离子方式:.
-
(3) 表示向饱和石灰水中通入CO2至过量的是,离子方程式:.
-
(4) 表示向MgCl2 和AlCl3的混合溶液中滴加NaOH溶液至过量的是,离子方程式:.
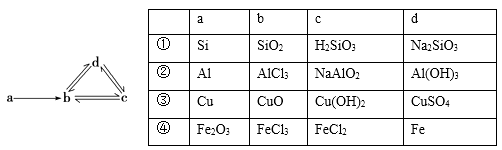
![]()
-
(1) 若 D 是金属,C 溶液在储存时应加入少量 D,其理由是(用必要的文字和离子方程式 表示)。
-
(2) 若 A、B、C 为含同一种金属元素的无机化合物,请写出 B 转化为 C 的所有可能的离 子力程式:。
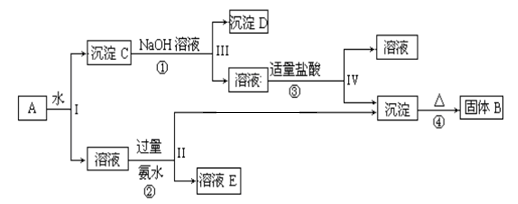
据此回答下列问题:
-
(1) I、II、III、IV四步操作采取的分离方法是。
-
(2) 根据上述框图反应关系,写出下列B、C、E所含物质的化学式
沉淀固体B;C;E
-
(3) 写出①、④四个反应方程式(是离子反应的写离子方程式)
① ④
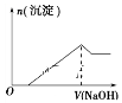 向MgCl2、AlCl3和盐酸的混合溶液中逐滴滴入NaOH溶液至过量
B .
向MgCl2、AlCl3和盐酸的混合溶液中逐滴滴入NaOH溶液至过量
B . 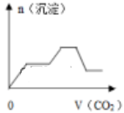 将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系
C .
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系
C . 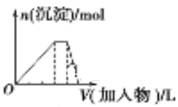 向NH4Al(SO4)2溶液中逐滴加入氢氧化钠溶液直至过量
D .
向NH4Al(SO4)2溶液中逐滴加入氢氧化钠溶液直至过量
D . 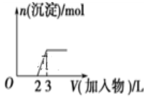 向烧碱溶液中滴加明矾溶液
向烧碱溶液中滴加明矾溶液
下列叙述正确的是( )
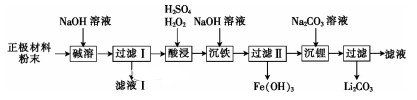
已知LiFePO4不溶于水和碱,能溶于强酸。
-
(1) “碱溶”时的离子方程式为。
-
(2) 向滤液Ⅰ中通入过量CO2会析出Al(OH)3沉淀,写出该反应的离子方程式:。
-
(3) “酸浸”时溶液中Fe2+发生反应的离子方程式为。
-
(4) 检验“沉铁”后所得溶液中是否存在Fe3+的方法是。
-
(5) 以Fe(OH)3为原料可以制取FeSO4晶体,还需的试剂有。
-
(6) “沉锂”时,检验Li+是否沉淀完全的方法是。
-
(1) 下列说法正确的是(填序号)。
① 配制氯化铁溶液,先将FeCl3固体溶于较浓盐酸,再用蒸馏水稀释到所需的浓度
② FeCl2只能通过置换反应生成,FeCl3只能通过化合反应生成
③ 利用氯水和KSCN溶液可以检验Fe3+中有无Fe2+
④ 加热蒸干Fe2(SO4)3溶液获得Fe2(SO4)3固体
⑤ 含a mol AlCl3的溶液和含1.5a mol NaOH的溶液,无论正滴和反滴,生成Al(OH) 3的质量相等
⑥ 由于金属铝性质稳定,所以Al在空气中能稳定存在
-
(2) 高铁酸钾(K2FeO4)是一种高效多功能水处理剂。其作用原理为。
-
(3) 以铝土矿(主要成分为Al2O3和Fe2O3、SiO2)为原料制备铝的一种工艺流程如下:

①滤渣主要成分为
②在实验室灼烧操作应选择的实验仪器为
③反应II中,加入NaHCO3一段时间才有沉淀生成,写出加入少量NaHCO3时发生反应的离子方程式。
-
(4) 已知25 ℃时Ksp[Cu(OH)2]=2.2×10−20 , Ksp[Fe(OH)3]=4.0×10−38 , Ksp[Al(OH)3]=1.1×10−33。
①在25 ℃下,向浓度均为0.1 mol·L−1的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成沉淀(填化学式)。
②溶液中某离子物质的量浓度低于1.0×10−5 mol·L−1时,可认为已沉淀完全。现向一定浓度的AlCl3和FeCl3的混合溶液中逐滴加入氨水,当Fe3+完全沉淀时,测定c(Al3+)=0.2 mol·L−1。此时所得沉淀中(填“还含有”或“不含有”)Al(OH)3。
 ,含
,含  和
和  等杂质)为原料制备铝的一种工艺流程如图所示:
等杂质)为原料制备铝的一种工艺流程如图所示: 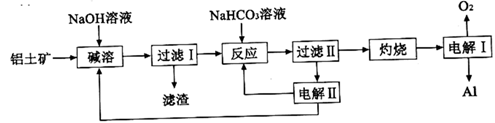
注:  在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。
-
(1) 铝土矿“碱溶”时,氧化铝转化为进入溶液,提高铝土矿浸取速率的措施有(任答两点)。
-
(2) 向“过滤Ⅰ”所得滤液中加入
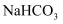 溶液,溶液的pH(填“增大”“减小”或“不变”),发生反应的离子方程式为。
溶液,溶液的pH(填“增大”“减小”或“不变”),发生反应的离子方程式为。
-
(3) “电解Ⅰ”是电解熔融的
 ,标准状况下每产生
,标准状况下每产生 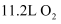 转移的电子数为。
转移的电子数为。
-
(4) “电解Ⅱ”是电解
 溶液,其原理如图所示,阳极的电极反应式为。
溶液,其原理如图所示,阳极的电极反应式为。 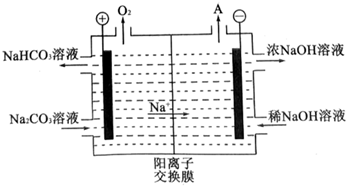
- 下列语句中,没有语病的一项是 A.一个人只要真正领略了苦难中的绝望,他就会明白,一切美化苦难的言辞是多么浮夸,一切炫耀苦
- 下列关于该图地区的叙述,不正确的是( )A.麦哲伦海峡将本地区分成南北两部分B.世界最大平原和最大高原都在本区C.印第
- 地理信息系统在城市环境管理工作中的应用领域有() ①城市环境规划与决策 ②城市路网规划③城市环境监测与评价 ④城市道
- 完形填空 I’m ____1_____ English. My name ____2_____ Lily.I’m a
- 读“大洋洲轮廓图”,回答问题。(16分)
- 下列说法正确的是() A.向久置的氯水中滴入紫色石蕊试液,溶液先变红后褪色 B.欲除去Cl2中的少量HCl气体,可将此混
- 将淀粉浆和淀粉酶的混合物放入玻璃纸袋中,扎好,浸入流动的温水中,相当长一段时间后,取袋中液体分别与碘水、新制Cu(OH)
- 16.名句名篇默写 (1)、尔来四万八千岁,不与秦塞通人烟。 西当太白有鸟道,_______。 地崩山摧壮士死, 然后天
- She__________ Robert for ten years. A. married B. marrie
- 下图中分别表示在发酵罐中培养酵母菌时,各环境因子对酵母菌繁殖速率的的影响,其中不正确的是( ) A. B.
- 如图,已知A、B两村庄的坐标分别为(2,2)、(7,4),一辆汽车在轴上行驶,从原点O出发. (1)汽车行驶到什么位置
- The small window in the wall could ______ some light into th
- 使人们意识到“人类也是生态平衡的一部分”,从而掀起了现代环保运动的作品是 A《百年孤独》 B《寂静的春天》 C《第二十
- 写出C4H9Cl的各种同分异构体并用系统命名法给其命名。
- 公信力是政府的影响力和号召力,反映着人民群众对政府的满意度和信任度。下列措施能有效提高某市政府公信力的是 ①市委召开党外
- 我国科学家经过艰苦努力,继完成人类基因组1%测序工作、水稻基因组“框架图和精密图”之后,又成功地率先完成了家蚕基因组“框
- Mr.Smith ___________ is smoking is looking for what helost y
- 17.补写出下列名篇名句中的空缺部分。(限选6个小题)(6分) (1)仰观宇宙之大, 。所以游目骋怀,足以
- 设NA为阿伏加德罗常数的值,下列关于0.2mol・L-1Ba(NO3)2溶液的说法不正确的是()。A.2L溶液中的阴、阳
- 等腰三角形周长为20cm,腰长为(cm),底边长为(cm),则与的函数关系式为 ,自变量的取值范



