实验2-6 氢氧化铝的制备 知识点题库
铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3 , 还含有FeO、SiO2)中.工业上用铝土矿制备铝的某种化合物的工艺流程如下:
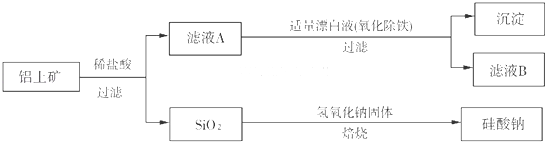
(l)滤液A所含溶质属于盐的是 .
(2)检验滤液B中是否还含有铁元素的方法为: (注明试剂、现象).
(3)将滤液B中的铝元素以沉淀形式析出,最佳试剂应选 (填代号).
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
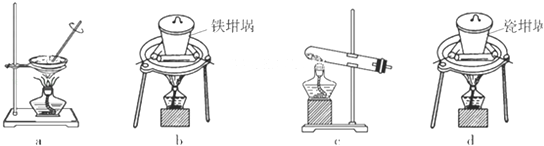
(4)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为 (填代号).
实验I:
(1)取形状、大小均相同的铝丝分别与等体积的、PH相同的盐酸、稀硫酸反应,随反应进行,盐酸中生成气体的速率明显比硫酸中生成气体的速率快,对此原因,你认为合理的猜测是下列的 (填写相应的字母);
a.盐酸的物质的量浓度大于硫酸的物质的量浓度
b.Cl﹣能促进此反应的进行
c.SO42﹣能抑制此反应的进行
d.硫酸使铝发生钝化
(2)为了探究反应速率不同的原因,请你根据所提供的药品,填写实验方案中的空白部分.
药品:氯化钠固体、硫酸钠固体、硫酸铜固体、氯化铜固体、6mol/L盐酸、3mol/L硫酸、18.4mol/L硫酸、5mol/L硝酸.
方案:取两支试管,分别加入形状、大小均相同的铝丝和等体积的 (填写相应的试剂,下同),再向其中的一支试管中加入适量的 固体,并振荡使固体溶解,观察实验现象.
实验探究:略.
实验II:
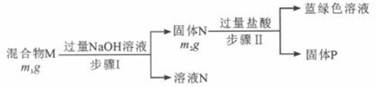
取足量的形状、质量均相同的铝丝分别与等体积的6mol/L的盐酸、6mol/L氢氧化钠溶液反应,待反应停止后取出剩余的铝丝洗净、干燥、称量,剩余铝丝的质量关系是前者 后者(填“大于”或“小于”或“等于”);观察反应后的液体,发现铝与盐酸反应后所得的液体是黑色浑浊的,试管底部有少量黑色沉淀,对此现象,同学们进行了如下探究:
(1)提出猜想
同学们查找资料后获得如下信息:工业上用电解法冶炼铝所用的原料氧化铝是从铝土矿中提取的,所以得到的氧化铝中可能还含有微量的氧化铁和二氧化硅两种杂质,据此,同学们提出如下猜想:
猜想1:此黑色固体是铁单质,可能是电解得到的铝与杂质反应生成的,相应的化学反应方程式为 ;
猜想2:此黑色固体是硅单质,是电解得到的铝与二氧化硅反应生成的.
猜想3:此黑色固体是铝单质,是铝与盐酸反应时因反应过快而变成粉末分散到溶液中;
猜想4:此黑色固体可能是上述若干种单质组成的混合物.
(2)设计实验方案并完成相关实验:
将反应后所得的液体进行过滤、洗涤,分别取少量固体置于两支试管中,完成下列实验:
1向其中的一支试管中加入足量的稀盐酸,观察固体是否溶解.实验时发现固体完全溶解,证明猜想 一定不正确(填“1”、“2”、“3”、“4”).
②向另一试管中加入足量的氢氧化钠溶液,观察固体是否溶解.实验时发现固体完全溶解,证明猜想 一定不正确(填“1”、“2”、“3”、“4”);
(3)得出结论
综合实验①②的现象,可推知猜想 (填“1”、“2”、“3”、“4”)是正确的,固体溶解在氢氧化钠溶液中的离子方程式为: .
①Na2CO3﹣制玻璃 ②SiO2﹣太阳能电池 ③AgI﹣人工降雨 ④NaCl﹣制纯碱⑤Al2O3﹣焊接钢轨 ⑥NaClO﹣消毒剂 ⑦Fe2O3﹣红色油漆或涂料 ⑧MgO﹣耐火材料.
①Ca(HCO3)2②Al(OH)3③NaAlO2④(NH4)2CO3⑤Al.
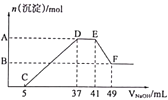
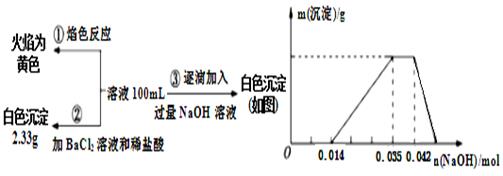
请回答下列问题:
-
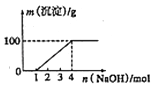
(1) 根据上述3组实验可以分析废水中一定不存在的阴离子是,一定存在的阳离子是。
-
(2) 写出实验③图像中沉淀开始减少至完全消失阶段发生反应的离子反应方程式:。
-
(3) 分析图像,在原溶液中c(NH4+)与c(Al3+)的比值为,所得沉淀的最大质量是g。
-
(4) 若通过实验确定原废水中c(Na+)=0.14 mol·L¯1,试判断原废水中NO3¯是否存在?(填“存在”“不存在”或“不确定”)。若存在,c(NO3¯)=mol·L¯1。(若不存在或不确定则此空不填)
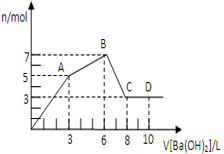
-
(1) 氢氧化钡溶液浓度为。
-
(2) 原混合溶液中SO42-和Cl-的物质的量之比为。
下列说法不正确的是( )
①Al ②Al2O3 ③ Al(OH)3 ④NaHCO3
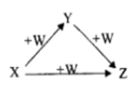
①Na、Na2O、Na2O2 ②AlCl3、Al(OH)3、 NaAlO2 ③ Fe、 FeCl2、FeCl3 ④NaOH、Na2CO3 、NaHCO3 ⑤C、CO、CO2
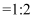 ,则下列说法正确的是( )
,则下列说法正确的是( ) ①甲烧杯中盐酸不足 ②乙烧杯中铝过量 ③甲烧杯中生成的气体体积为10.08L ④乙烧杯中 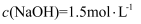
- ________ and short of breath, Andy and Ruby were the first t
- 下列词语中,只有一个错别字的一组是( ) A、防犯 蛛丝马迹 虚左以待 远见卓识 B、船
- 四边形ABCD的内角A与C互补,AB=BC=2,CD=3,DA=1. (1)求角和的长; (2)求四边形的面积.
- Peter is young, but he__ many foreign countries. A. has been
- 下列叙述正确的是 A.稀释浓硫酸时应将水沿烧杯内壁倒入浓硫酸中,并用玻璃棒不断搅拌 B.将100g溶质质量分数为98%的
- 穿越时空后,假如你生活在河姆渡聚落,你能体验到的是()。 A.成员之间的贫富差别大
- 在马拉松比赛的后半程,运动员大腿肌肉细胞进行呼吸作用所形成的产物有 ( ) A.CO2
- 下列说法不正确的是 A.卤代烃不是烃 B.石蜡油不是油脂 C.甘油不是油 D.环己烷不是饱和烃
- 文学作品阅读太湖碎锦 范烟桥 ①太湖,用文人的套语来形容,是“三万六千顷、七十二峰”。民间则说“八百里太湖跨三州”。不经
- 当导体两端电压一定时,通过导体的电流随导体电阻变化规律的图像如下图所示。请根据图像判断,当导体电阻为60 Ω时,通过该导
- 一位母亲记录了儿子3~9岁的身高的数据,她根据这些数据建立的身高y(cm)与年龄x的回归模型为 =7.19x+73.93
- (11分)把课本中的文字知识用图表、材料等多种方式呈现,是一项重要的历史学习技能。阅读下列三幅图片并回答问题。 (
- 若则 。
- 泉城济南,景色秀美;保护环境,人人有责。下列做法,与保护环境的倡导不相符的是①污水排入大明湖 ②随意丢弃方便袋 ③植树种
- 若=________.
- 对于甲型H1N1流感病毒,专家表示是可防、可控、可治的,不必过于惊慌。这是因为
- ......
- 设命题p:,命题q:若是的必要不充分条件,则实数的取值范围是_____________
- 如图所示,某实验小组进行以下实验:(1)上述实验进行对比的目的是 . (2)
- 关于不同射线的性质,下列说法中正确的是 [ ]A.α射线是原子核发生衰变时放射出的氦核,它的电离作用最弱B



