第三节 羧酸 酯 知识点题库
①乙酸丙酯 ②甲酸乙酯 ③乙酸甲酯 ④乙酸乙酯
物质 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) |
乙醇 | -117.0 | 78.0 | 0.79 |
乙酸 | 16.6 | 117.9 | 1.05 |
乙酸乙酯 | -83.6 | 77.5 | 0.90 |
某学生在实验室制取乙酸乙酯的主要步骤如下:
①配制2 mL浓硫酸、3 mL乙醇(含18O)和2 mL乙酸的混合溶液。
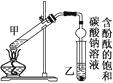
②按上图连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。
-
(1) 配制①中混合溶液的方法为;
反应中浓硫酸的作用是;
写出制取乙酸乙酯的化学方程式:。
-
(2) 上述实验中饱和碳酸钠溶液的作用是________(填字母)。A . 中和乙酸和乙醇 B . 中和乙酸并吸收乙醇 C . 减少乙酸乙酯的溶解 D . 加速酯的生成,提高其产率
-
(3) 步骤②中需要小火均匀加热,其主要理由是;
步骤③所观察到的现象是;
欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器有;分离时,乙酸乙酯应从仪器(填“下口放”或“上口倒”)出。
-
(4) 该同学反复实验,得出乙醇与乙酸的用量和得到的乙酸乙酯生成量如下表:
实验
乙醇(mL)
乙酸(mL)
乙酸
乙酯(mL)
①
2
2
1.33
②
3
2
1.57
③
4
2
x
④
5
2
1.76
⑤
2
3
1.55
表中数据x的范围是;实验①②⑤探究的是。
已知有机物A是具有水果味的液体,其分子式为C4H8O2 , 在一定条件下有下列转化关系:
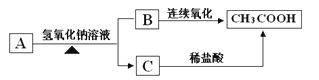
-
(1) 写出A的结构简式
-
(2) 由A与氢氧化钠溶液反应生成B和C属于 反应(填反应类型);
-
(3) 写出下列反应的化学方程式连续氧化中的第一步反应 ;C与盐酸反应 2
-
(4) A有多种同分异构体,写出符合下列条件的所有A的同分异构体的结构简式
①该有机物能与氢氧化钠反应 ②结构中只含一个甲基.
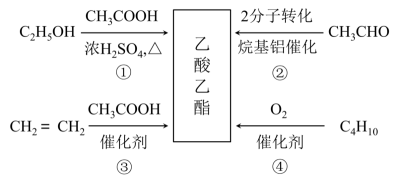
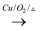 CH3CHO
CH3CHO 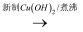 CH3COOH,请用上述表述方法表示
CH3COOH,请用上述表述方法表示 ①挥发性 ②酸性 ③比碳酸的酸性强 ④还原性 ⑤能发生酯化反应
下列各实验中,分别填出表现甲酸相应性质的编号:
-
(1) 在碳酸钠溶液中加入甲酸有气体放出,说明甲酸具有;
-
(2) 在甲酸钠晶体中加入浓磷酸,加热后放出能使湿润蓝色石蕊试纸变红的气体,说明甲酸具有;
-
(3) 与乙醇、浓硫酸混和后共热,能闻到一种香味,说明甲酸具有;
-
(4) 在甲酸溶液中加入氢氧化铜,能看到溶液变蓝色,说明甲酸具有;
-
(5) 在新制氢氧化铜中加入甲酸溶液,加热看到有红色沉淀生成,说明甲酸具有.
| 选项 | 性质 | 用途 |
| A | H2能在O2中燃烧并放出大量的热 | H2用作洁净燃料 |
| B | 硝酸能与苯发生取代反应 | 苯用作溶剂 |
| C | 葡萄糖能与新制Cu(OH)2悬浊液反应 | 葡萄糖可用作甜味剂 |
| D | 乙酸能与NaOH溶液反应 | 乙酸可用作调味剂 |
-
(1) 大米和小麦中的主要营养物质是 (选填“糖类”、“油脂”、“蛋白质”或“维生素”)。
-
(2) 乙酸可使紫色石蕊试液变色。
-
(3) 酒精的结构简式是;乙酸分子中官能团的名称是。
-
(4) 下列试剂中,能用于检验酒精中是否含有水的是(_____)。A . CuSO4 · 5H2O B . 无水硫酸铜 C . 浓硫酸 D . 金属钠
-
(5) 请写出乙醇与乙酸生成乙酸乙酯的化学反应方程式。
-
(6) 除去乙酸乙酯中残留的乙酸,有效的处理方法是(______)。A . 蒸馏 B . 水洗后分液 C . 用过量饱和碳酸钠溶液洗涤后分液 D . 用过量氯化钠溶液洗涤后分液
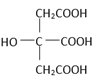 ,下列有关说法错误的是( )
,下列有关说法错误的是( )
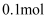 柠檬酸与足量的
柠檬酸与足量的 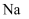 反应生成
反应生成 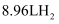 C . 柠檬酸可与乙醇发生酯化反应
D . 柠檬酸中所有碳原子不可能在同一平面上
C . 柠檬酸可与乙醇发生酯化反应
D . 柠檬酸中所有碳原子不可能在同一平面上
小明的知识储备:
①乙醇能和氯化钙形成CaCl2·6C2H5OH
②有关物质的沸点:
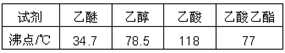
制备过程:
装置如图所示,A中放有浓硫酸,B中放有10mL无水乙醇和5mL冰醋酸,D中放有滴有酚酞的饱和碳酸钠溶液。迅速升温到170℃进行反应。
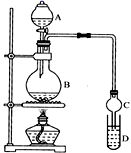
-
(1) 请补充出乙酸与乙醇发生酯化反应的化学方程式。
-
(2) 实验装置还缺少。
-
(3) 实验过程中滴加大约3mL浓硫酸,B的容积最合适的是___。(填字母)A . 25mL B . 50mL C . 250mL D . 500mL
-
(4) 小明在D中观察到了明显的的分层现象,其下层显色。
产品提纯:
①将D中混合物转入分液漏斗进行分液。②有机层用5mL饱和氯化钙溶液洗涤,最后用水洗涤。有机层倒入一干燥的烧瓶中,用无水硫酸镁干燥,得粗产物。③将粗产物蒸馏,收集馏分,得到纯净干燥的乙酸乙酯。
-
(5) 操作②的目的为洗去,操作③中,应收集℃馏分。
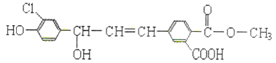
 )。下列说法正确的是( )
)。下列说法正确的是( )

-
(1) 试管甲中依次放入以下液体:①2 mL乙醇;②3 mL;③2 mL乙酸。为防止试管甲中的液体在实验时发生暴沸,在加热前还应加入。
-
(2) 试管乙中盛放的试剂是;反应结束后,分离试管乙中的液体混合物需要用到的分离操作为。
-
(3) 装置丙的名称为,其作用为。
-
(4) 若实验中使用的乙醇为C2H518OH,试管甲中发生反应的化学方程式为:。
-
(5) 已知苯甲酸乙酯的沸点为212℃,用上述装置能否在乙处收集到产品(填“能”或“不能”)。
下列说法正确的是。( )
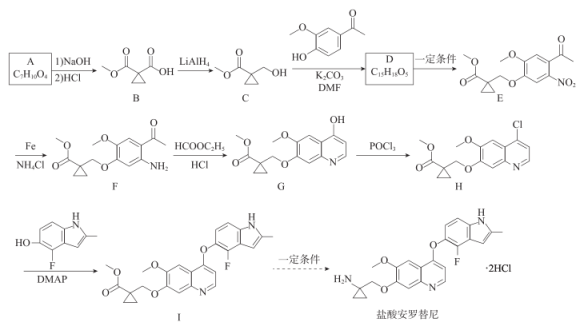
已知信息:
i.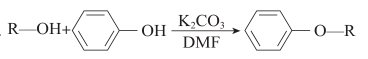
ii.羰基与烯醇存在互变异构: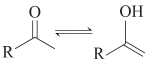
回答下列问题:
-
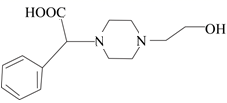
(1) A中官能团的名称为。
-
(2) B有多种同分异构体,其中能同时满足下列条件的化合物的结构简式为、。(不考虑立体异构)
①不存在环状结构;
②可发生水解反应、加聚反应,也能与新制氢氧化铜悬浊液反应生成砖红色沉淀;
③核磁共振氢谱有两组峰,峰面积之比为1:3。
-
(3) D的结构简式为,D→E的反应条件为。
-
(4) F→G的反应方程式为。
-
(5) H→I的反应类型为。
-
(6) 设计由苯甲酸甲酯制备甲酸苯甲酯的合成路线(无机试剂任选)。
- 如图6-2-21所示,平行板电容器经开关S与电池连接,S闭合一段时间后断开,a处固定一带电荷量很小的正电荷,φa表示a点
- 图甲为菜豆种子萌发的过程,图乙为肉眼看到的幼苗的幼根,请据图回答: (1)图甲处于①②阶段时,萌发所需的营养物质由种子的
- 2011年“世界水日”的主题是“未来之水”。下列关于水的说法中,不正确的是()。 A.硬水和软水可以用肥皂水鉴别 B.地
- The charity show was very successful with the help of all t
- (2015•鄂州)将下列句子组成语段,顺序排列正确的一项是() ①甲骨文是中国文化的活化石,它与古埃及象形文字、古巴比
- 如图,△ABC与△ADE都是直角三角形,∠B与∠AED都是直角,点E在AC上,∠D=30°,如果△ABC经过旋转后能与△
- 彭敦文认为:“五四运动的内涵,无论是政治方面的,还是思想方面的,都充满着多元性与矛盾性。”这里的“多元性”是指五四运动是
- 如图,椭圆x2+=1的左、右顶点分别为A、B,双曲线Γ以A、B为顶点,焦距 为2,点P是Γ上在第一象限内的动点,直线AP
- 某人能看懂文字和听懂别人的淡话,但不能用词语表达自己的思想,这表明他的大脑受到损伤,受伤的区域是( ) A.大脑皮
- 食品添加剂溴酸钾(KBrO3)会致癌,已被禁用,其中溴元素(Br)的化合价为() A.+1 B.+3 C.+5
- 下列物质中,富含蛋白质的是 A.土豆 B.鸡蛋 C.花生油
- 日本控制和垄断占领区的金融和内外贸易的目的是( ) A.攫取中国的资源财富
- 如图,点与点关于直线对称,则______.
- 操作:在△ABC中,AC=BC=2,∠C=90°,将一块等腰直角三角板的直角顶点放在斜边AB的中点P处,将三角板绕点P旋
- 钠及其化合物是中学化学学习和研究的重要内容. (1)如图是钠的原子结构示意图
- When the man came in, dressed in black, gun in hand, weall s
- 先化简,再求值:,其中.
- 下列词语中有错别字的一项是( ) A.缄默 一霎时 姗姗来迟 冥思遐想 B.羸弱 戈
- 长方形的长是(2m+3n)米,宽为(2m-3n)米,则该长方形的面积是
- 我国四大地理区域中水资源最丰富的区域是 A.北方地区 B.南方地区C.西北地区



