第三章 晶体结构与性质 知识点题库
含氮化合物种类繁多,卟吩(图A)连有取代基时即称为卟啉,卟啉的四个氮原子易与金属离子结合生成叶绿素(图B)等多种物质.请回答:

-
(1) 卟吩中N原子采用的轨道杂化方式是
-
(2) 下列有关叶绿素分子的说法正确的是 (填选项序号).A . 图1中1﹣5号C中有三个具有手性 B . 分子中存在配位键 C . 图1中1、2、3、4号C共面 D . N的第一电离能大于O
-
(3) 卟啉与Fe2+合即可形成血红素,Fe2+的电子排布式为
-
(4) 氰化氢(HCN)是一种含氮剧毒化合物,其分子中σ键与π键的个数比为.由分子结构推测,氰化氢(填“易”或“不易”)溶于水,原因是.氰化氢进人人体后产生的CN﹣能使人迅速中毒,请举出两种CN﹣的等电子体.
-
(5) N与B能够形成一种硬度接近金刚石的物质,其晶体结构如图2,若其晶胞边长为apm,则其密度为g.cm﹣3(只列算式).
-
(1) Cu基态原子的外围电子排布为,Cr基态原子的外围电子排布为,这样排布的理由是.
-
(2) NH3是一种很好的配体,原因是.
-
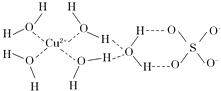
(3) 图中虚线表示的作用力为.
-
(4) 胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4•H2O晶体.在该晶体中,含有的原子团或分子有:[Cu(NH3)4]2+、NH3、SO42﹣、H2O,其中[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团或分子是,写出一种与此正四面体结构互为等电子体的分子的分子式.
-
(5) 金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4 , 呈正四面体构型.Ni(CO)4易溶于 (填标号).A . 水 B . 四氯化碳 C . 苯 D . 硫酸镍溶液.
-
(1) E属于区的元素,其基态原子的核外电子排布式为。
-
(2) 五种元素中,电负性最大的是(填元素符号)。
-
(3) B与其同周期相邻元素第一电离能由大到小的顺序为(用元素符号表示)。
-
(4) 下图是已经合成的最著名的“D-B”化合物的分子结构。“D-B”化合物在研磨或迅速加热时会剧烈分解并引起爆炸,生成非常稳定的两种单质分子(相对分子质量之比为7:64),发生反应的化学方程式为。
-
(5) A 元素的最高价含氧酸根离子( 只含A 和氧两种元素)的空间构型为,该酸根离子的中心原子的轨道杂化类型为,与该酸根离子互为等电子体的一种分子为(填化学式)。
-
(6) 已知G 与Cl元素的某种化合物的晶胞结构如图所示:
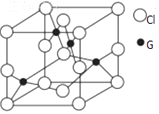 则该化合物的化学式是,若G 与Cl原子最近的距离为a cm,则该晶体的密度为g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数的数值为NA)。
则该化合物的化学式是,若G 与Cl原子最近的距离为a cm,则该晶体的密度为g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数的数值为NA)。
图1 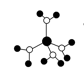 图2
图2 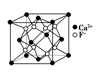 图3
图3  图4
图4 
-
(1) 碳化硅(SiC)是一种晶体,具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的。下列各种晶体:①晶体硅 ②硝酸钾 ③金刚石 ④碳化硅 ⑤干冰 ⑥冰,它们的熔点由高到低的顺序是(填序号)。
-
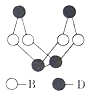
(2) 下列离子晶体的立体构型示意图,如下图所示。
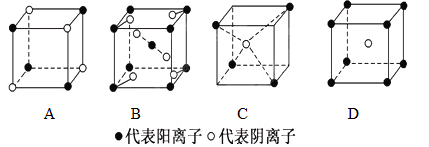
以M代表阳离子,以N代表阴离子,写出各离子晶体的组成表达式。
A.,B:,C:,D:。
-
(3) 已知FeS2晶体(黄铁矿的主要成分)具有A的立体结构。
①FeS2晶体中具有的化学键类型是。
②若晶体结构A中相邻的阴、阳离子间的距离为acm,且用NA代表阿伏加德罗常数,则FeS2晶体的密度是g·cm-3。
-
(1) 基态Cu原子价电子排布式为,基态 Fe2+核外有个未成对电子。
-
(2) C、N、O三种元素第一电离能由高到低的顺序为 。
-
(3) 铁可形成多种配合物,如[Fe(CN)6]4-、 Fe(CO)5等,1 mol
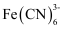 中含有σ键的数目为 (已知 CN-与N2是等电子体) ;Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4 , 据此可以判断Fe (CO)5晶体属于(填晶体类型)。
中含有σ键的数目为 (已知 CN-与N2是等电子体) ;Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4 , 据此可以判断Fe (CO)5晶体属于(填晶体类型)。
-
(4) 下列变化过程中,破坏的力的作用类型相同的是______(填标号)。A . 铝气化 B . AlCl3 溶于水 C . 加热使铜熔化 D . 熔融NaCl
-
(5) Fe能与N形成一种磁性材料,其晶胞结构如图所示。
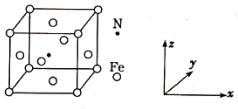
①该磁性材料的化学式为。
②Fe原子的坐标参数为(
 ,
,  ,0)(
,0)(  ,0,
,0,  )(0,
)(0,  ,
,  ),N原子的坐标参数为。
),N原子的坐标参数为。③已知该晶体的晶胞参数为a pm,列出其密度表达式为g/cm3(用含a的式子表示,只列式子,不作计算)。
-
(1) 钛的应用越来越受到人们的关注。
①第四周期元素中,基态原子的未成对电子数与钛相同的有(填元素符号)。
②钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是。
-
(2) 锰及其化合物的应用研究是前沿科学之一
①已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列(选填字母编号)。
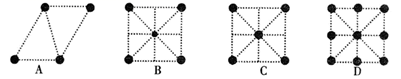
②三醋酸锰[(CH3COO)3Mn]是一种很好的有机反应氧化剂。三醋酸锰[(CH3COO)3Mn]中阳离子的价层电子排布式中电子的自旋状态(填“相同”或“相反”)。
③Mn2+能形成配离子为八面体的配合物MnClm·nNH3 , 在该配合物的配离子中,Mn2+位于八面体的中心。若含1 mol该配合物的溶液与足量AgNO3溶液作用可生成1mol AgCl沉淀,则该配离子化学式为。
-
(3) 比较Fe和Mn的第三电离能,I3(Fe)I3(Mn)(填“大于”或“小于”),原因是。
-
(4) 某钙钛型复合氧化物如图,以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有巨磁电阻效应。
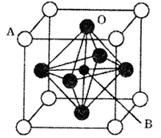
已知La为+3价,当被钙等+2价元素A替代时,可形成复合钙钛矿化合物LaxA1-xMnO3 , (x>0.9),此时一部分+3价锰转变为+4价,导致材料在某一温度附近有反铁磁-铁磁、铁磁-顺磁转变及金属-半导体的转变,则复合钙钛矿化合物中+3价锰与+4价锰的物质的量之比为(用含x的代数式表示)。
-
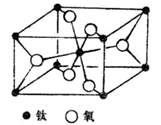
(5) 具有较高催化活性的材料金红石的晶胞结构如图所示。已知该晶体的密度为d g·cm-3 , Ti、O原子半径分别为a pm和b pm,阿伏加德罗常数的值为NA , 则金红石晶体的空间利用率为(列出计算式)。
-
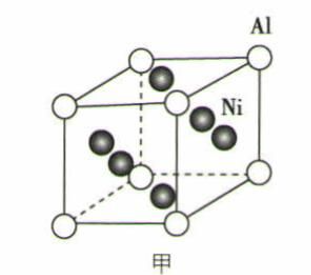
(1) Ni与Al形成的一种合金可用于铸造飞机发动机叶片,其晶胞结构如图甲所示,该合金的化学式为。
-
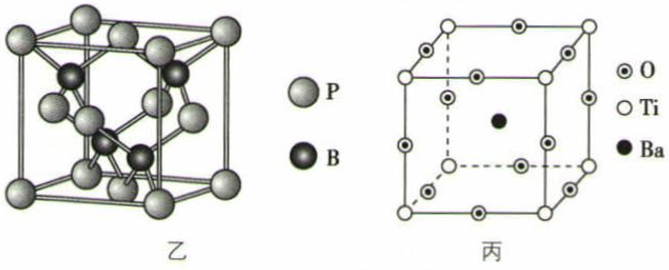
(2) ①磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。如图乙是磷化硼晶体的晶胞,B原子的杂化轨道类型是 。立方相氮化硼晶体的熔点要比磷化硼晶体的高,其原因是 。
②已知磷化硼的晶胞参数a =478 pm,请列式计算该晶体的密度ρ=g·cm-3(用含NA的代数式表示即可,不需要计算出结果)。晶胞中硼原子和磷原子最近的核间距d为pm。
-
(3) 自然界中有丰富的钛矿资源,如图丙表示的是钡钛矿晶体的晶胞结构,经X射线衍射分析,该晶胞为正方体,晶胞参数为apm。
写出钡钛矿晶体的化学式,其密度是g·cm-3(设阿伏加德罗常数的值为NA)。
 、
、  、
、  、
、  )等在光电子器件、太阳能电池以及生物探针等方面有广阔前景。回答下列问题:
)等在光电子器件、太阳能电池以及生物探针等方面有广阔前景。回答下列问题:
-
(1) 砷元素基态原子价层电子排布式为:
-
(2) 下列状态的锌,分别失去最外层一个电子所需能量最小的是___________。A .
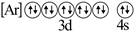 B .
B . 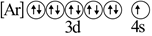 C .
C . 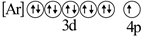 D .
D . 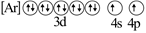
-
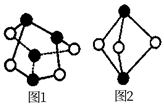
(3) 雄黄(
 )如图1和雌黄(
)如图1和雌黄(  )如图2是提取砷的主要矿物原料,二者在自然界中共生。图1中
)如图2是提取砷的主要矿物原料,二者在自然界中共生。图1中  原子轨道杂化类型为。图2中
原子轨道杂化类型为。图2中 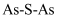 键角
键角 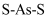 键角(填
键角(填 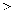 ,
, 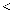 或
或  )。
)。 
-
(4)
 分子中
分子中  键数目有个,分子的空间构型为。分子中大
键数目有个,分子的空间构型为。分子中大 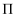 键可用符号
键可用符号 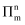 表示,其中m代表参与形成的大
表示,其中m代表参与形成的大 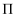 键原子数,n代表参与形成大
键原子数,n代表参与形成大 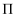 键电子数(如苯分子中的
键电子数(如苯分子中的 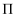 键可表示为
键可表示为  ,则
,则  中大
中大 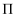 键应表示为。
键应表示为。
-
(5)
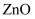 具有独特的电学及光学特性,是一种应用广泛的功能材料。
具有独特的电学及光学特性,是一种应用广泛的功能材料。 ①已知
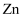 和O的电负性分别为1.65、3.5,
和O的电负性分别为1.65、3.5, 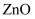 中化学键类型为,
中化学键类型为, 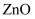 可以与
可以与  溶液溶解生成
溶液溶解生成 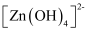 ,请从化学键角度解释能形成该离子的原因。
,请从化学键角度解释能形成该离子的原因。②一种
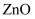 晶体的晶胞(立方体)如图3所示,
晶体的晶胞(立方体)如图3所示,  为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 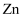 原子半径为
原子半径为 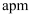 。图4是沿着立方格子对角面取得的截图,则
。图4是沿着立方格子对角面取得的截图,则 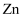 原子与O原子间最短距离x=
原子与O原子间最短距离x= 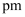 。晶体的密度为
。晶体的密度为 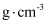 (列出计算式即可)。
(列出计算式即可)。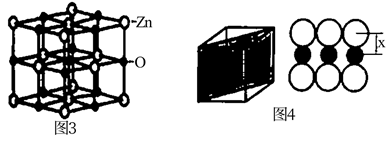
-
(1) 基态钛原子的价电子排布式为,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有种。
-
(2) Ti的四卤化物熔点如下表所示,TiF4熔点高于其它三种卤化物,自TiCl4至TiI4熔点依次升高,原因是。
化合物
TiF4
TiCl4
TiBr4
TiI4
熔点/℃
377
-24.12
38.3
155
-
(3) Ti(IV)的某配合物可用于催化环烯烃聚合,其结构如图所示:
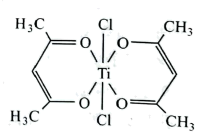
①配合物中H、C、O三种元素的电负性由大到小的排列顺序为。
②请在图中标出配位键(用“→”表示);
③配合物中非金属元素的含氧酸根的中心原子杂化轨道类型是sp2的是。
-
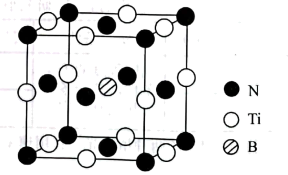
(4) 用B掺杂TiN后(晶胞结构中只是B原子部分代替钛原子),其晶胞结构如图所示,距离Ti最近的B有个,Ti与B的最近距离为nm;掺杂B后的晶体密度是TiN晶体的倍。(已知掺杂B后的晶体密度为ρg/cm3 , 阿伏加德罗常数的值为NA)
-
(1) 基态Ga原子的价电子排布式为。
-
(2) 晶体硅、碳化硅、金刚石三种晶体的熔点由高到低的顺序为。
-
(3) 氮化镓不存在于自然界中,只能通过人工合成来制备,反应为
 。
。①GaCl3熔点为77.9℃,其晶体类型为。GaF3的熔点为1000℃,则将GaF3熔化时,被破坏的作用力是。
②上述反应涉及的元素中,电负性最小的是(填元素符号,下同),第一电离能最大的是。
-
(1) 硫原子的价电子轨道表示式为。
-
(2) 硫化钠的熔点 (填“大于”“小于”或“等于”)硫化钾的熔点,原因是。
-
(3) 硫酸根和硫代硫酸根的结构如下图所示:
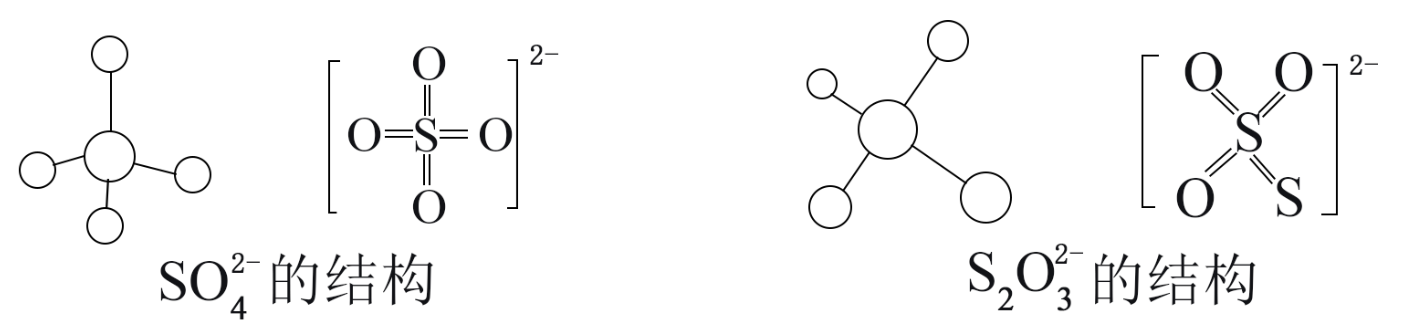
S2O
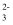 的空间构型为, 中心硫原子的杂化轨道类型为。
的空间构型为, 中心硫原子的杂化轨道类型为。 -
(4) 硫原子和氧原子可形成多种链式硫酸根离子,连二硫酸根离子、连三硫酸根离子如下图所示:
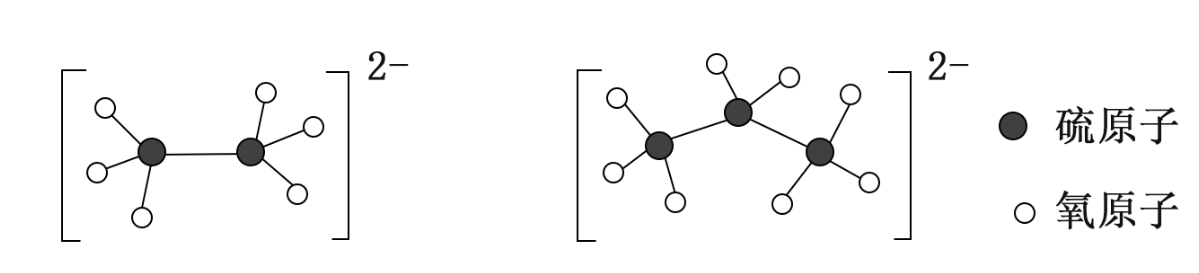
这类硫原子数可变的多硫氧合阴离子的化学式可用通式表示为(用n代表硫原子数)。
-
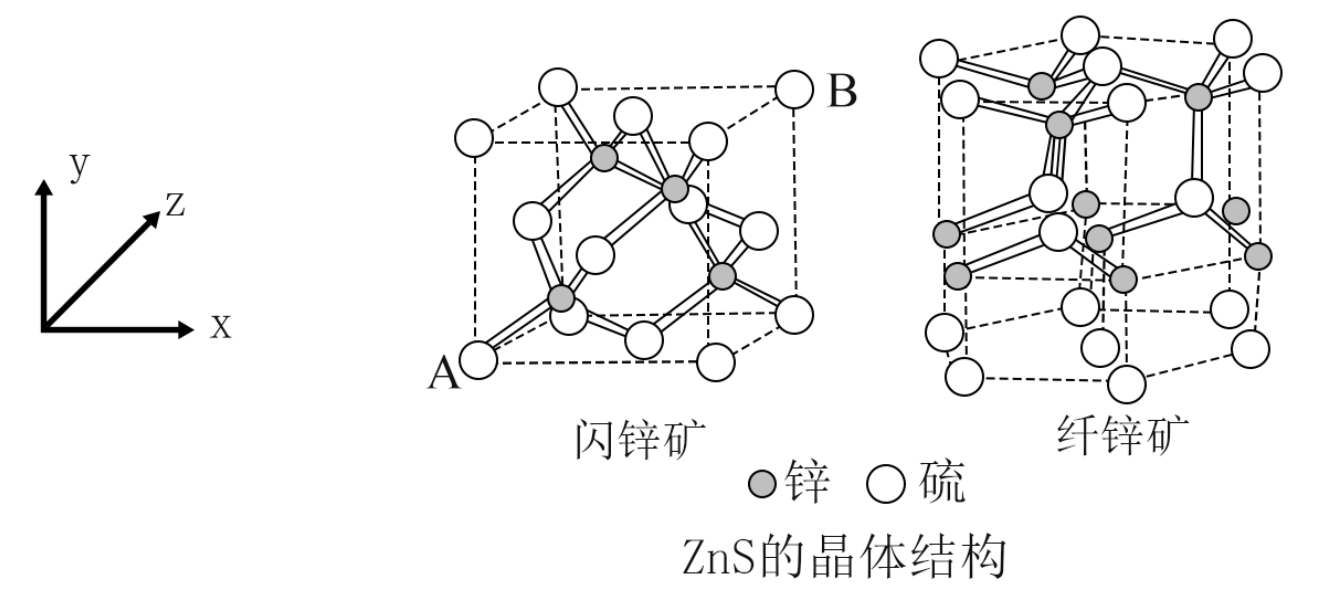
(5) 天然硫化锌以闪锌矿和纤锌矿存在,ZnS的晶体结构如下图所示,闪锌矿中Zn2+的配位数为,已知原子A、B的分数坐标为(0, 0, 0)和(1, 1, 1),原子C的分数坐标为。 纤锌矿晶体堆积模型为。
-
(6) 闪锌矿中,设晶胞边长为a, Zn2+和 S2-的离子半径分别为
 和
和 , 则Zn2+和S2-离子的空间占有率为% (列出计算表达式)。
, 则Zn2+和S2-离子的空间占有率为% (列出计算表达式)。
- 如图是某化学反应的微观模型,“○”“”分别表示不同元素的原子,下列各项中对图模型理解正确的是()A.该反应属于分解反应
- 已知四棱锥中平面,且,底面为直角分别是的中点. (1)求证:// 平面; (2)求截面与底面所成二面角的大小; (3)求
- 随着社会的发展,越来越多的人认识到了英语的重要性,但是有些人担心自己方言太重,英语口语不够标准,不能够很好地和外宾交流
- 有关生态系统的叙述中,正确的是() A.生态系统是由生产者、消费者和分解者组成 B.生态系统中越高级的消费者所获得的物质
- C Handshaking, though a European practice, is often seen
- 把下面几个句子组成语意连贯的一段话,排序正确的一组是 ①每一种话语体系,都代表了特定的视界。 ②我们说了上千年的古话,说
- 下列叙述正确的是 [ ] A.制糖
- 恩格斯说:“世界的真正统一性在于它的物质性。”下列能够充分说明这一论述的是 ①自然界是客观存在的物质世界 ②
- 花是由什么发育而成的( ) A.花芽 B.花柄 C.花轴 D.花梗
- 静止的实验火箭,总质量为M,当它以对地速度vo喷出质量为Δm的高温气体后,火箭的速度为 A. B.―C.
- 我国坚决取缔并关闭严重污染环境的小企业,这从一个方面表明我国政府在有效地行使() A.保护自然环境,维护国家安全的职能
- 3.下列句子中,没有语病且句意明确的一句是:(3分) ( ) A.10月17日下午,澳大利亚新南
- 2014年8月中旬,临沂市小麦政策性农业保险理赔工作结束,理赔面积12.6万亩,理赔金额1762万元,16万农户得到保险
- 阅读下列材料,问答问题: 材料一 中华人民共和国外交政策和原则是,为保障本国独立、自由和领土主权的完整,拥护国际的持久
- 如图所示的四种现象中,属于光的反射现象的是 ( )
- 图中能反映北美洲自西向东地势起伏的剖面图是( )
- 常温下,若1体积硫酸恰好与2体积pH=11的氢氧化钠溶液混合后pH=3(混合后体积变化不计)则二者物质的量浓度之比应为
- 如下图所示,用四种方式用轻绳将小球拴住,静止在倾角为θ的光滑斜面上,根据下面四个图的情况判断以下说法中正确的是 (
- Outstandingcharacters________history will be remembered_____
- MrsSmith cut herself while she thismorning.



