第三章 晶体结构与性质 知识点题库
下列叙述中不正确的是( )
A . 通过化合反应与置换反应均可以制得Fe3O4
B . 通过化合反应与复分解反应均可以制得Fe(OH)3、NaHCO3
C . 离子化合物的熔点不一定比共价化合物的熔点高
D . 向含有1mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总物质的量为3 mol
硒有两种同素异形体:灰硒和红硒.灰硒溶于三氯甲烷,红硒溶于二硫化碳,它们都不溶于水,则灰硒和红硒的晶体属于( )
A . 原子晶体
B . 分子晶体
C . 金属晶体
D . 以上均有可能
物质的性质决定了物质的用途,下面列出了金属的几种性质:①导热性、②导电性、③还原性、④延展性、⑤具有金属光泽.请在下面金属用途后的横线上填上金属主要性质对应的序号.(每空限选一个)
(1)用铝锭制成包装用的铝箔 ;
(2)用铝制成的高压铝锅 ;
(3)用铁粉回收照相业废液中的银 ;
(4)电信业中大量使用的铜丝、金属电缆
下列有关化学键与晶体结构说法正确的是( )
A . 两种元素组成的分子中一定只有极性键
B . 离子化合物的熔点一定比共价化合物的高
C . 非金属元素组成的化合物一定是共价化合物
D . 含有阴离子的化合物一定含有阳离子
四氯化硅结构和四氯化碳类似,对其性质判断①四氯化硅是分子晶体;②常温下为液态;③四氯化硅沸点较低;其中正确的是( )
A . 只有①
B . ①③
C . ②③
D . ①②③
MgO、Rb2O、CaO、BaO四种离子晶体熔点的高低顺序可能是( )
A . MgO>Rb2O>BaO>CaO
B . MgO>CaO>BaO>Rb2O
C . CaO>BaO>MgO>Rb2O
D . CaO>BaO>Rb2O>MgO
下列配合物的水溶液中加入硝酸银不能生成沉淀的是( )
A . [Co(NH3)4Cl2] Cl
B . [Co(NH3)3Cl3]
C . [Co(NH3)6] Cl3
D . [Cu(NH3)4]Cl2
如图是氯化铯晶体的晶胞(晶体中的最小重复单元),已知晶体中两个最近的Cs+离子核间距离为a cm,氯化铯的相对分子质量为M,NA为阿伏加德罗常数,则氯化铯晶体密度是( )
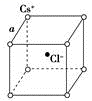
A .  g/cm3
B .
g/cm3
B .  g/cm3
C .
g/cm3
C .  g/cm3
D .
g/cm3
D .  g/cm3
g/cm3
 g/cm3
B .
g/cm3
B .  g/cm3
C .
g/cm3
C .  g/cm3
D .
g/cm3
D .  g/cm3
g/cm3
下列叙述正确的是( )
A . 氯化铯晶体中,每1个Cs+与其他8个Cs+等距离紧邻
B . 金刚石网状结构中,由共价键构成的碳原子环中,最小的环上有4个碳原子
C . 熔点由高到低的顺序是:金刚石>碳化硅>晶体硅
D . PCl3和了BCl3分子中所有原子的最外层都达到8电子稳定结构
W、M、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质在高空大气层中保护人类免遭太阳光中紫外线的强烈侵袭;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色的Z2O和黑色的ZO两种氧化物。
-
(1) Y3+基态电子排布式可表示为。
-
(2) MX3-的空间构型是(用文字描述)。H2X分子的VSEPR模型名称为。
-
(3) 含Z(H2X)42+的溶液中通入MH3 , 会生成Z(MH3)42+的原因。(从电负性角度解释)
-
(4) 1 mol WX2中含有的π键数目为。
-
(5) AlP因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2000℃ ,其晶胞结构如图所示。
①磷化铝的晶体类型为。
②A、B点的原子坐标如图所示,则C点的原子坐标为。
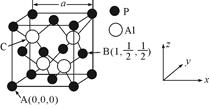
③磷化铝的晶胞参数a=546.35pm(1pm=10-12m),其密度为 g/cm3(列出计算式即可,用NA表示阿伏加德罗常数的数值)。
C、N、O、P、S、Cl、Cu、Zn八种元素的单质及化合物在现代工业生产中有着广泛的应用,请回答下列问题:
-
(1) 第一电离能:ZnCu(填“>”或“<”下同)电负性S Cl。
-
(2) 写出基态Cu原子的价电子排布式
-
(3) SO3的空间构型是 ,白磷P4分子呈正四面体结构,P原子位于正四面体的四个顶点,则P原子的杂化形式为。
-
(4) 与SCN—互为等电子体的微粒有(任写两种)。
-
(5) NH3、PH3、AsH3三者的沸点由高到低的顺序是,原因是。
-
(6) Cu与Cl形成的一种化合物的晶胞结构如图所示(黑点代表铜原子)。
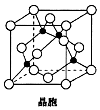
①该晶体的化学式为。
②已知该晶体中Cu原子和Cl氯原子之间的最短距离apm且恰好为体对角线的
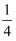 ,阿伏加德罗常数为NA , 则该晶体的密度为g/cm3(列出计算式即可)。
,阿伏加德罗常数为NA , 则该晶体的密度为g/cm3(列出计算式即可)。
下列不是离子化合物的是( )
A . HF
B . CaI2
C . KOH
D . NaNO3
下列有关说法正确的是( )
A . 7.8g苯含有0.6NA个σ键
B . 基态F原子核外有9种能量不同的电子
C . 第一电离能:Ga>Zn
D . 每个面心立方晶胞中八面体空隙与四面体空隙个数比为1:2
电能是一种无污染、可再生的二级能源。储电材料种类繁多。如图是两种储电材料,请阅读试题、观察图片,回答问题。
-
(1) Ⅰ.新型碳氮材料的储电能力应用前景广阔。其基本构成单元如图所示。
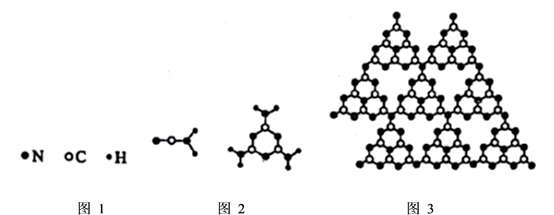
图1中化学键σ键与π键之比为;图2中碳原子的杂化方式为。
-
(2) 图3中,储电材料的分子式可以表示为。
-
(3) 碳元素与氮元素的电负性大小关系为。氮元素与氧元素的第一电离能大小关系为。
-
(4) 碳的最高价含氧酸根的空间构型是;硝酸的酸性强于亚硝酸的原因是。
-
(5) Ⅱ.传统锂电池的主要成分是 LiCoO2 其晶胞结构如图所示;因结构中存在笼状空隙, 可以与Ni 和Mn 发生位置替换, 形成储电性能更加优良的化合物LiNi
 Mn
Mn  Co
Co  O2。
O2。 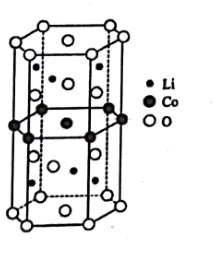
基态 Co 原子的价电子排布式为; 化合物 LiCoO2 中 O元素在晶胞中的位置,除了位于六棱柱的顶点外,其他具体位置是。
-
(6) 已知化合物中各原子半径依次为:Li=a,Ni=b,Mn=c,Co=d,O= e,晶胞的棱长为 m,底边边长为n ,该晶体的空间利用率的计算表达式为 (用含有 a、b、c、d、e、m、n 的式子表示 )。
据报道复旦大学修发贤教授课题组成功制备出砷化铌纳米带,并观测到其表面态具有百倍于金属铜薄膜和千倍于石墨烯的导电性。相关研究论文已在线发表于权威科学期刊《自然》。回答下列问题:
-
(1) 铌元素(Nb)为一种金属元素,其基态原子的核外电子排布式为[Kr]4d55s1。下列是Nb的不同微粒的核外电子排布式,其中失去最外层1个电子所需能量最小的是(填标号)。
a.[Kr]4d35s15p1b.[Kr]4d45s1c.Kr]4d2d.Kr]4d3
-
(2) 砷为第VA族元素,砷可以与某些有机基团形成有机化合物,如(ClCH=CH)2AsCl,其中As原子与2个C原子、1个Cl原子形成的VSEPR模型为。
-
(3) 英国曼彻斯特大学物理学家安德烈·盖姆和康斯坦丁诺沃肖洛夫用微机械剥离法成功从石墨中分离出石墨烯,因此共同获得2010年诺贝尔物理学奖;而石墨烯具有优异的光学、电学、力学特性在材料学、微纳加工、能源、生物医学和药物传递等方面具有重要的应用前景,被认为是一种未来革命性的材料。
已知“石墨烯”的平面结构如图所示,一定条件下石墨烯与H2发生加成反应生成石墨烷,石墨烷中碳原子杂化类型是,石墨烯导电的原因是。

-
(4) 石墨烯也可采用化学方法进行制备如采用六氯苯、六溴苯作为原料可制备石墨烯。下表给出了六氯苯、六溴苯、苯六酸俗名为蜜石酸的熔点和水溶性:
物质
六氯苯
六溴苯
苯六酸
熔点/℃
231
325
287
水溶性
不溶
不溶
易溶
六溴苯的熔点比六氯苯高的原因是,苯六酸与六溴苯、六氯苯的水溶性存在明显的差异本质原因是。
-
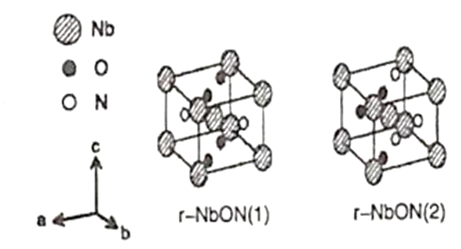
(5) 出于以更高效率利用太阳光等目的研制出金红石型铌氧氮化物(NbON),比以往的光学半导体更能够吸收长波长侧的光,作为光学半导体的新材料。该化合物的晶胞有如图所示的两种构型,若晶胞的边长为apm,该晶体的密度为g·cm-3。(NA是阿伏加德罗常数的值,相关原子量:Nb—93)
下列各组物质中,都含有共价键,却又都不属于共价化合物的一组是( )
A . 
 B .
B . 
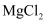 C .
C . 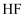
 D .
D . 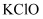


 B .
B . 
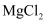 C .
C . 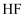
 D .
D . 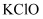

现有原子序数递增的X、Y、Z、W四种常见元素。其中X元素基态原子核外电子占据了三个能级,且每个能级上的电子数相等;Y原子的p轨道处于半充满状态,Z的单质是空气的主要成分之一;W在周期表中位于ds区,且与Z可形成化学式为W2Z或WZ的二元化合物。请回答下列问题:
-
(1) W元素原子核外电子运动状态有种,该元素基态离子W+的电子排布式为。
-
(2) 元素X、Y和Z的第一电离能由大到小顺序为(填元素符号)。
-
(3) Y2Z与XZ2具有相同的结构特征,其理由是。
-
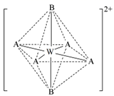
(4) X、Y和Z均可形成多种氢化物,写出一种X的氢化物分子结构中σ键和π键数目之比3∶2的结构式;A、B分别是Y、Z的最简单氢化合物,A的空间构型为,其中Y原子的杂化轨道类型为;W2+与A、B分子结合成配合离子[WA4B2]2+结构如下图,该配合离子加热时首先失去的组分是(填“A”或“B”)。
-
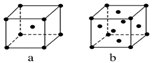
(5) 元素W的单质晶体在不同温度下可有两种堆积方式,晶胞分别如图a和b所示,假定不同温度下元素W原子半径不变,且相邻最近原子间距为原子半径之和,则其体心立方堆积与面心立方堆积的两种晶体密度之比为。
下列关于晶格能的说法中正确的是( )
A . 晶格能指形成1 mol离子键所放出的能量
B . 晶格能指破坏1 mol离子键所吸收的能量
C . 晶格能指1 mol离子化合物中的阴、阳离子由相互远离的气态离子结合成离子晶体时所放出的能量
D . 晶格能的大小与晶体的熔点、硬度都无关
下列叙述错误的是( )
A . 沸点的高低: Cl2>F2
B . 硬度的大小: Mg> Ca> K
C . 熔点的高低: Na> Mg> Al
D . 晶格能的大小: NaF> NaCl> NaBr > NaI
下列说法正确的是( )
A . 氢元素和其他元素可形成共价化合物,也可形成离子化合物
B . 离子化合物中只含离子键,共价化合物中只含共价键
C . 碘晶体升华、HCl气体溶于水都有共价键被破坏
D . NaCl晶体中,Na+和Cl-之间通过静电引力形成离子键
最近更新
- 蝗虫大发生时,可长途迁徙,所经之处农作物受到严重破坏。研究发现蝗虫种群数量的增长受多种因素的影响。当雨量充沛、气候潮湿时
- 阅读下面短文,根据短文内容,补全表格中所缺的信息。 Cars are very important in the lif
- 将2molS02和1molO2放入一个密闭容器中,在一定的条件下反应到达“平衡状态”,此时,下列所示容器内存在各物质的物
- 西瓜是同学们喜欢的水果,下列能发育成西瓜籽的结构是 A.子房壁 B.胚珠 C.花药
- 国务院常务会议决定,从2013年8月1日起,对月销售额不超过2万元的小微企业暂免征收增值税和营业税。据此回答下列各题。
- 右图中AO是一条与平面镜成60°的光线,请在图中画出反射光线并标出反射角度数.
- 钛号称“崛起的第三金属”,被广泛应用于军事、医学等领域。已知钛有48Ti、49 Ti、50Ti等同位素,下列关于金属钛
- 2009年我国外交工作以应对金融危机为主线,以多边峰会为重要平台,积极参与应对金融危机、气候变化等国际合作,各项外交工作
- “扬汤止沸”不如“釜底抽薪”,主要说明想问题、办事情 ( ) A.坚持全面的观点,分清主流与支
- 某有机物是药物生产的中间体,其结构简式如右图。下列有关叙述 不正确的是( ) A.该有机物与浓溴水可发生取代反应
- 写作岁月无痕,亲情似水。在你的家庭里,你一定感受到浓浓的亲情了吧!爸爸妈妈为你的成长时时担忧,爷爷奶奶为你的健康处处呵护
- (10分)2008年9月25日上午21时9分,“神州”七号载人飞船发射升空。火箭点火起飞,583秒后,飞船与火箭分离,准
- 如图,在△ABC中,∠ACB=90°,过B,C两点的⊙O交AC于点D,交AB于点E,连接EO并延长交⊙O于点F.连接BF
- 质量M=4kg的小车內有一跨过定滑轮的轻绳两端连接小物块m1和m2.如图示,m1=1kg,m2=2kg.m1和固定在小车
- ____with the size of the whole earth , the biggest ocean doe
- 科学家将哺乳动物或人的成熟红细胞放进蒸馏水中,造成红细胞破裂出现溶血现象,再将溶出细胞外的物质冲洗掉,剩下的结构在生物学
- 如图所示,C为两极板水平放置的空气平行板电容器,闭合开关S,当滑动变阻器R1、R2的滑动头处于各自的中点位置时,悬在电容
- 阅读下面这首唐诗,然后回答问题。(8分)军城早秋 严武[注]昨夜秋风入汉关,朔云边月满西山。更催飞将追骄虏,莫遣沙
- 封开县境内新发现了大型的“钼矿”,金属钼可用于制造火箭、导弹等耐高温材料。 如果钼铅矿(PbMoO4)中的铅元素为+2价
- --- What do youthink of the lecture of Li Yang's Crazy Engl



