第二章 分子结构与性质 知识点题库
下列有关物质结构的说法正确的是( )
A . 共价化合物中各原子最外层都一定满足8电子结构
B . BaO2晶体中阳离子与阴离子数目之比为1∶2
C . H2O是一种非常稳定的化合物,这是由于氢键所致
D . 在反应2Na2O2+2H2O = 4NaOH+O2↑,既有离子键、极性键和非极性键的断裂,又有离子键、极性键和非极性键的形成
下列各物质的中心原子采用sp3杂化的是( )
A . NH3
B . O3
C . CO2
D . BeCl2
“暖冰”是韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成的.某老师在课堂上做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成含有少量KSCN 的FeCl2溶液,则溶液呈血红色.则下列说法中不正确的是( )
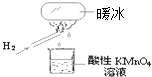
A . 在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰”
B . 水凝固形成20℃时的“暖冰”所发生的变化是化学变化
C . 该条件下H2燃烧生成了既具有氧化性又具有还原性的物质
D . 该条件下H2燃烧的产物中可能含有一定量的H2O2
下列化合物中,含有非极性共价键的离子化合物是( )
A . CaC2
B . N2H4
C . Na2S2
D . NH4NO3
四氯化硅结构和四氯化碳类似,对其性质判断①四氯化硅是分子晶体;②常温下为液态;③四氯化硅沸点较低;其中正确的是( )
A . 只有①
B . ①③
C . ②③
D . ①②③
若ABn的中心原子A上没有未用于形成共价键的孤电子对,运用价层电子对互斥理论,下列说法正确的是( )
A . 若n=2,则分子的空间构型为V形
B . 若n=3,则分子的空间构型为三角锥型
C . 若n=4,则分子的空间构型为正四面体型
D . 以上说法都不符合题意
金属及其化合物在科学研究和工业生产中具有重要的用途。
-
(1) 三氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:
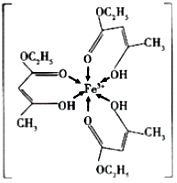
①此配合物中,铁离子价电子排布图为;
②此配离子中碳原子的杂化轨道类型为;
③此配离子中含有的化学键为。
A 离子键 B 金属键 C 极性键 D 非极性键 E 配位键 F 氢键 G σ键 H π键
-
(2) NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。NO2-离子的VSEPR模型名称为,K3[Co(NO2)6]是黄色沉淀,该物质中四种元素的电负性由大到小的顺序是。
-
(3) 研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2 , 其中适合作录音带磁粉原料的是。
-
(4) 锰的一种配合物的化学式为Mn(BH4)2(THF)3 , 写出两种与BH4-互为等电子体的微粒(请写一个分子和一个离子)。
-
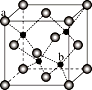
(5) ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶体的结构如图所示,a的配位数为,已知晶胞密度为ρ g/cm3 , 则晶包的棱长为nm(NA表示阿伏加德罗常数)。
X、Y、Z、W、Q为原子序数依次增大的前四周期元素,X核外未成对电子数有2个,与其他元素均能形成二元化合物;Y是地壳中含量最多的金属元素;Z是遗传物质的组成元素之一;W内层电子数是最外层电子数的9倍;Q基态原子价层电子排布中成对电子数和未成对电子数相同,且成对电子数为最外层电子数的2倍。据此回答下列问题:
-
(1) Q的基态原子的价层电子排布式为。
-
(2) X、Y、Z、W四种元素中,电负性最大的是(填元素符号,下同);同周期元素中,第一电高能介于Y 和Z之间的有。
-
(3) Y 和W的氯化物熔点高的是(填化学式),原因是;与Z的低价氯化物互为等电子体的离子是(填离子符号)。
-
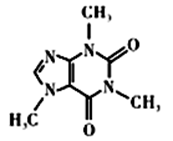
(4) 咖啡因对中枢神经有兴奋作用,其结构简式如图所示。常温下,咖啡因在水中的溶解度为2g,加适量水杨酸钠[C6H4(OH)(COONa)]可使其溶解度增大,其原因可能是,分子中氮原子的杂化类型有。
-
(5) 已知WX的密度为3.25 g/cm3 , 单元晶胞边长481pm,经计算可确定该单元晶胞中含有个WX,说明在形成晶体时,半径大的粒子先进行了方式的堆积,晶胞中距离W最近的X有个。
-
(1) 某实验小组尝试用燃烧法确定有机物M的分子式,所用装置如下:
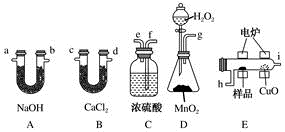
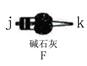
①产生的氧气按从左到右方向流动,所选装置各导管的连接顺序是(以上装置不能重复使用):g→fe→hi→ → →jk。
②F装置作用是。
③若准确称取有机物M(只含C、H、O三种元素中的两种或三种)3.24g,经充分燃烧后,A管质量增加9.24g,B管质量增加2.16 g,则该有机物的实验式为。
④已知在相同条件下该M蒸气相对氢气的密度为54,且能与Na反应但不与NaOH溶液反应,写出该物质在灼热的铜丝条件下与氧气的反应方程式 。
-
(2) 在常温下测得的某烃C8H10(不能与溴水反应)的核磁共振谱上,观察到两种类型的H原子给出的信号,其强度之比为2∶3,试确定该烃的结构简式为;该烃在光照下生成的一氯代物在核磁共振谱中产生的吸收峰强度比为。
含有  的
的 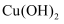 悬浊液可用于检验醛基,原理可用下列化学方程式表示:
悬浊液可用于检验醛基,原理可用下列化学方程式表示: 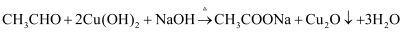
 的
的 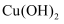 悬浊液可用于检验醛基,原理可用下列化学方程式表示:
悬浊液可用于检验醛基,原理可用下列化学方程式表示: 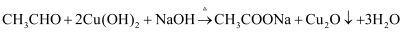
-
(1)
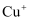 基态核外电子排布式为。
基态核外电子排布式为。
-
(2)
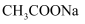 中碳原子轨道的杂化类型是。
中碳原子轨道的杂化类型是。
-
(3)
 分子中
分子中  键与
键与  键的数目比
键的数目比 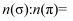 。
。
-
(4)
 广泛应用于太阳能电池领域,其晶胞为立方体(见下图),晶胞中
广泛应用于太阳能电池领域,其晶胞为立方体(见下图),晶胞中 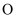 原子的配位数为。
原子的配位数为。 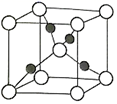
-
(5)
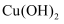 可溶于氨水生成
可溶于氨水生成  配离子。研究发现,
配离子。研究发现,  与
与  的空间构型相同,而
的空间构型相同,而  却难以与
却难以与  形成配离子,其原因是。
形成配离子,其原因是。
“阿比朵尔”(如图所示)是抗击新冠病毒潜在用药,关于“阿比朵尔”说法正确的是( )
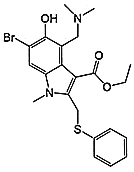
A . 不能使溴水褪色
B . 所有的原子可能在同一个平面上
C . 核磁共振氢谱共有11个峰
D . “阿比朵尔”属于芳香烃
磷酸盐几乎是所有食物的天然成分之一,作为重要的食品配料和功能添加剂被广泛用于食品加工中。在食品加工中使用的磷酸盐通常为钠盐、钙盐、钾盐以及作为营养强化剂的铁盐和锌盐。天然存在的磷酸盐是磷矿石[主要成分为Ca3(PO4)2 , 同时还有SiO2等],用硫酸跟磷矿石反应,能生成被植物吸收的Ca(H2PO4)2。
回答下列问题:
-
(1) 金属铁可导电、导热,具有金属光泽,有延展性,这些性质都可以用“理论”解释。
-
(2) SiO2硬而脆,其原因是。
-
(3) Ca、Fe、K、Zn的第一电离能由大到小的顺序为。
-
(4) O、Si、P、S四种元素形成的最简单氢化物的稳定性最强的是 (填化学式);P4难溶于水却易溶于CS2 , 其原因为。
-
(5) PO
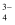 的空间构型为,酸性条件下,PO
的空间构型为,酸性条件下,PO 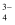 可与Fe3+形成H3[Fe(PO4)2]从而掩蔽溶液中的Fe3+ , 基态Fe3+核外M层有种空间运动状态不同的电子。
可与Fe3+形成H3[Fe(PO4)2]从而掩蔽溶液中的Fe3+ , 基态Fe3+核外M层有种空间运动状态不同的电子。
常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为0.01mol·L-1)的pH和原子半径、原子序数的关系如图所示。下列说法错误的是( )
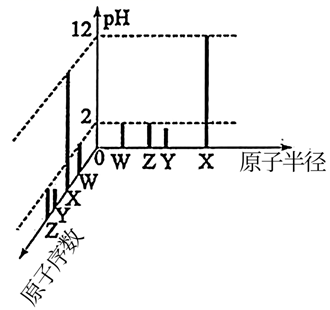
A . 第一电离能:W>Z>Y>X
B . 简单离子的半径:Y>Z>W>X
C . W的氢化物空间构型不一定是三角锥形
D . Z的单质具有强氧化性和漂白性
①PH3的分子空间结构为三角锥形,②BeCl2的分子空间结构为直线形,③CH4的分子空间结构为正四面体形,④CO2为直线形分子,⑤BF3的分子空间结构为平面正三角形,⑥NF3的分子空间结构为三角锥形。下面对分子极性的判断正确的是( )
A . ①⑥为极性分子,②③④⑤为非极性分子
B . 只有④为非极性分子,其余为极性分子
C . 只有②⑤是极性分子,其余为非极性分子
D . 只有①③是非极性分子,其余是极性分子
化合物M(NH4CuSO3)为难溶于水的白色固体,取少量M进行如下实验,下列推断正确的是( )
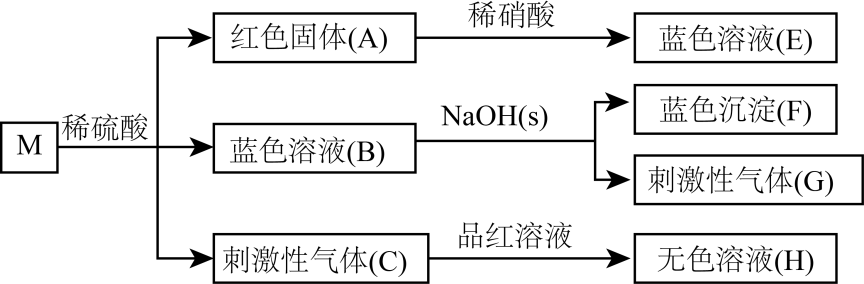
A . 化合物M中Cu的化合价为+2价
B . 红色固体(A)为氧化铜
C . G为含极性共价键的极性分子
D . 加热H无明显现象
我国科学家率先利用 作为客体分子进行组装,得到新型碳纳米管片段材料,合成效率优于石墨片层卷曲,此材料具有显著的光电效应。下列说法正确的是( )
作为客体分子进行组装,得到新型碳纳米管片段材料,合成效率优于石墨片层卷曲,此材料具有显著的光电效应。下列说法正确的是( )
 作为客体分子进行组装,得到新型碳纳米管片段材料,合成效率优于石墨片层卷曲,此材料具有显著的光电效应。下列说法正确的是( )
作为客体分子进行组装,得到新型碳纳米管片段材料,合成效率优于石墨片层卷曲,此材料具有显著的光电效应。下列说法正确的是( )
A .  中的碳原子为
中的碳原子为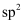 杂化
B . 由
杂化
B . 由 形成碳纳米管为物理变化
C . 石墨和
形成碳纳米管为物理变化
C . 石墨和 均为分子晶体
D . 碳纳米管导电的原因是形成了金属键
均为分子晶体
D . 碳纳米管导电的原因是形成了金属键
 中的碳原子为
中的碳原子为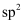 杂化
B . 由
杂化
B . 由 形成碳纳米管为物理变化
C . 石墨和
形成碳纳米管为物理变化
C . 石墨和 均为分子晶体
D . 碳纳米管导电的原因是形成了金属键
均为分子晶体
D . 碳纳米管导电的原因是形成了金属键
离子液体是在室温或接近室温时呈液态的盐类物质,应用广泛。1-乙基-3-甲基咪唑四氟硼酸盐离子液体结构如图所示,其环状结构中存在大π键,下列相关叙述错误的是( )

A . 该物质阳离子中至少10原子共平面
B . 该物质阴离子呈正四面体形
C . 该离子液体存在共价键、配位键、氢键
D . 该离子液体与水能够形成氢键
下列说法正确的是( )
A .  分子形状呈三角锥形,是非极性分子
B . 凡有规则外形的固体一定是晶体
C . 电负性越大的元素,第一电离能也越大
D .
分子形状呈三角锥形,是非极性分子
B . 凡有规则外形的固体一定是晶体
C . 电负性越大的元素,第一电离能也越大
D .  分子中σ键与π键的数目之比是1:1
分子中σ键与π键的数目之比是1:1
 分子形状呈三角锥形,是非极性分子
B . 凡有规则外形的固体一定是晶体
C . 电负性越大的元素,第一电离能也越大
D .
分子形状呈三角锥形,是非极性分子
B . 凡有规则外形的固体一定是晶体
C . 电负性越大的元素,第一电离能也越大
D .  分子中σ键与π键的数目之比是1:1
分子中σ键与π键的数目之比是1:1
铜是重要的金属,广泛应用于电气、机械制造、国防等领域,铜的化合物在科学研究和工农业生产中有许多用途。回答下列问题:
-
(1) 基态Cu原子价层电子排布式为。
-
(2)
 晶体中S原子的杂化方式为,
晶体中S原子的杂化方式为, 的立体构型为。
的立体构型为。
-
(3) 向
 溶液中加入过量氨水,可生成
溶液中加入过量氨水,可生成 , 其配体的电子式为;下列有关说法正确的是。
, 其配体的电子式为;下列有关说法正确的是。A.氨气极易溶于水,原因之一是
 分子和
分子和 分子之间形成氢键
分子之间形成氢键B.
 分子和
分子和 分子空间构型不同,氨分子的键角小于水分子的键角
分子空间构型不同,氨分子的键角小于水分子的键角C.
 所含有的化学键有离子键、极性共价键和配位键
所含有的化学键有离子键、极性共价键和配位键D.
 组成元素中电负性最大的是氮元素
组成元素中电负性最大的是氮元素 -
(4) 金铜合金的一种晶体结构为立方晶型,如图所示:
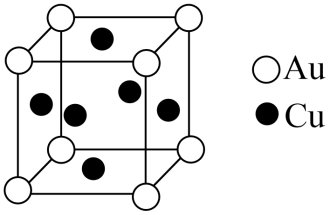
①该合金的化学式为。
②已知该合金的密度为
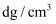 , 阿伏加德罗常数值为NA , 则该晶胞的棱长为cm。
, 阿伏加德罗常数值为NA , 则该晶胞的棱长为cm。 -
(5) 以情性电极电解足量的
 溶液。阳极上的电极反应式为:,若该电极产生气体的物质的量为0.01mol,则析出铜的质量为g。
溶液。阳极上的电极反应式为:,若该电极产生气体的物质的量为0.01mol,则析出铜的质量为g。
-
(1) I.解释下列问题:
H2O内的O-H、水分子间的范德华力和氢键,从强到弱依次为,H+可与H2O形成H3O+ , H3O+中O采用杂化,H3O+的空间构型为。H3O+中H-O-H键角比H2O中的,原因是。
-
(2) 用质谱仪检测气态乙酸时,谱图中出现质荷比(相对分子质量)为120的峰,原因是。
-
(3) 金属镓(Ga)位于元素周期表中第4周期IIIA族,其卤化物的熔点如下表:
GaF3
GaCl3
GaBr3
熔点/℃
>1000
77.75
122.3
GaF3熔点比GaCl3熔点高很多的原因是。
-
(4) 三价铬离子能形成多种配位化合物。
 中提供电子对形成配位键的原子是,中心离子的配位数为。
中提供电子对形成配位键的原子是,中心离子的配位数为。
-
(5) 基态Ti原子的核外电子排布式为。
-
(6) CaTiO3的晶胞如图(a)所示,金属离子与氧离子间的作用力为,Ca2+的配位数是。

-
(7) 一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I﹣和有机碱离子
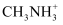 , 其晶胞如图(b)所示。其中Pb2+与图(a)中的空间位置相同,有机碱
, 其晶胞如图(b)所示。其中Pb2+与图(a)中的空间位置相同,有机碱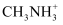 中,N原子的杂化轨道类型是;若晶胞参数为anm,则晶体密度为g·cm-3(列出计算式)。
中,N原子的杂化轨道类型是;若晶胞参数为anm,则晶体密度为g·cm-3(列出计算式)。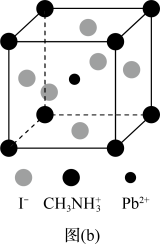
最近更新
- 面对北洋军阀的统治,几经挫折的国民党和都认识到,必须以武装的反革命。为此,国民党在1924年采取的重要措施是 A.与合作
- 春秋初期,楚国君主首先称王。随后,吴、越等国国君也相继称王。上述现象本质上反映了( ) A.专制制度动摇
- 能正确表示下列反应的离子反应方程式为() A.惰性电极电解MgCl2溶液:2Cl- +2 H2O2OH- +Cl2↑ +
- 按要求修改下面文章。 ①1985年,我在美国俄勒冈州波特兰市安家落户后不久,州政府指定我去帮助他们接待一个来自中国的大型
- 3.以下对生物实验的叙述正确的是 A.检测梨汁是否有葡萄糖,可加入适量斐林试剂后摇匀,并观察颜色变化 B.在探究细胞
- 英国资产阶级革命对英国的历史作用,最重要的是 A.建立了君主立宪制 B.为英国资本主义的发展开辟了广阔的道路 C
- 06(天津卷)44 在显像管的电子枪中,从炽热的金属丝不断放出的电子进入电压为U的加速电场,设其初速度为零,经加速后形成
- 过原点作曲线的切线,则切点坐标是______________,切线斜率是_________。
- If you come to the party,you a great time. A.would
- 定义在R上的函数, ( ) A、-3 B、3 C、6
- 化简的值是( ) A. B. C. D.
- 如果a g 某气体中含有分子数为b,则c g该气体在标准状况下的体积是 ( ) A. B
- 阅读下面的文字,完成后面题。 写作“是一场绝望的竞赛” 宣金学 门罗是第一位获得诺贝尔文学奖的加拿大人。她也是在该奖项设
- 在磁感应强度为2.0T的匀强磁场中,放一条与磁场方向垂直的长度为0.5m的通电导线,导线中的电流为4.0A.这段导线在与
- 柳宗元在《封建论》中说:“秦有天下,裂都会而为之群邑,废侯卫而为守宰。……此其所以为得也。”这句话指的是
- 如图,△ABC中,∠A=60°,P为AB上一点, Q为BC延长线上一点,且PA=CQ,连PQ交AC边于D, PD=DQ,
- 下列加点词语运用不正确的一项是( ) A.某同学面对老师说:“学生才疏学浅,老师过誉了。” B.静静的小山村在月光中若有
- 平行六面体的底面是菱形,且,试问:当的值为多少时,面?请予以证明.
- “一切合法的劳动收入和合法的非劳动收入,都应该得到保护。”这对于最广泛最充分地调动一切积极因素,发展社会主义市场经济有积
- 最能代表细胞膜基本化学成分的一组化学元素是( ) A、C.H.O.N



