第二章 分子结构与性质 知识点题库
下列物质所属晶体类型分类正确的是( )
A | B | C | D | |
原子晶体 | 石墨 | 生石灰 | 碳化硅 | 金刚石 |
分子晶体 | 冰 | 固态氨 | 氯化铯 | 干冰 |
离子晶体 | 氮化铝 | 食盐 | 明矾 | 芒硝 |
金属晶体 | 铜 | 汞 | 铝 | 铁 |
A . A
B . B
C . C
D . D
中科院国家纳米科学中心2013年11月22日宣布,该中心科研人员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了80多年的问题提供了直观证据.这不仅将人类对微观世界的认识向前推进了一大步,也为在分子、原子尺度上的研究提供了更精确的方法.下列说法中正确的是( )
①正是氢键的存在,冰能浮在水面上
②氢键是自然界中最重要、存在最广泛的化学键之一
③由于氢键的存在,沸点:HCl>HBr>HI>HF
④由于氢键的存在,使水与乙醇互溶
⑤由于氢键的存在,使水具有稳定的化学性质.
A . ②⑤
B . ③⑤
C . ②④
D . ①④
下列四种物质的结构图中,小黑球代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表价键,示例:如  ),下列说法正确的是( )
),下列说法正确的是( )
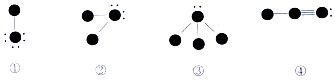
A . 四种物质中摩尔质量最大的是③
B . ①与③反应生成一种离子化合物
C . ④中含有非极性共价健
D . 该四种化合物涉及6种元素
根据条件回答下列问题
-
(1) 下列物质:①O2②三氯甲烷 ③CH3CH2CH2OH④O3⑤CHCl3⑥CH3OCH2CH3⑦
 C ⑧CH3CH(OH)CH3⑨
C ⑧CH3CH(OH)CH3⑨  C ⑩CH3OH.其中属于同系物的有(填序号,下同),互为同分异构体的有,互为同素异形体的有,属于同位素的有,是同一种物质的有.
C ⑩CH3OH.其中属于同系物的有(填序号,下同),互为同分异构体的有,互为同素异形体的有,属于同位素的有,是同一种物质的有.
-
(2) 已知碳原子数小于或等于6的单烯烃与HBr反应,加成产物只有一种结构,符合此条件的单烯烃有种.在这些烯烃中,若与H2加成;后,所得烷烃的一卤代物的同分异构体有2种,则该烯烃的结构简式为(并命名之).名称.结构简式:.
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子。N4分子结构如图所示,下列说法正确的是( )
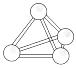
A . N4分子属于一种新型的化合物
B . N4分子中只含有非极性键
C . 1 mol N4分子所含共价键数为4NA
D . N4沸点比P4(白磷)高
下列分子中的中心原子(点“·”的原子为中心原子)上的价层电子对数正确的是( )
A . CH4 4
B . CO2 1
C . BF3 2
D . SO3 2
元素的基态原子的核外电子有3种能量状态、5种空间状态,X是其中第一电离能最小的元素;元素Y的M层电子运动状态与X的价电子运动状态相同;元素Z位于第四周期,其基态原子的2价阳离子M层轨道全部排满电子。
-
(1) X基态原子的电子排布式为。
-
(2) X的氢化物(H2X)在乙醇中的溶解度大于H2Y,其原因是。
-
(3) 在Y的氢化物(H2Y分子中,Y原子轨道的杂化类型是。
-
(4) Y与X可形成YX32−。
①YX32−的立体构型为(用文字描述)。
②写出一种与YX32−互为等电子体的分子的化学式。
-
(5) Z的氯化物与氨水反应可形成配合物[Z(NH3)4(H2O)2]Cl2 , 该配合物加热时,首先失去配离子中的配体是(写化学式)。
-
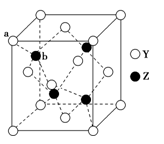
(6) Y与Z所形成化合物晶体的晶胞如图所示,该化合物的化学式为。其晶胞边长为540.0 pm,密度为g·cm−3(列式并计算),a位置Y与b位置Z之间的距离为pm(列式表示)。
下列有关物质的性质或应用的说法正确的是 ( )
A . 一定条件下用H2除去乙烷中混有的乙烯
B . 用核磁共振氢谱鉴别1—丙醇和2—丙醇
C . 间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构
D . 乙烯和苯都能使溴水溶液褪色,褪色的原理相同
下列物质中存在离子键、共价键和配位键的是( )
A . Na2O2
B . H3O+
C . NH4Cl
D . NaOH
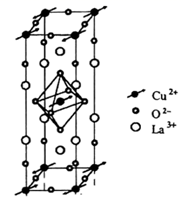
铜酸镧是一种反铁磁绝缘体,可由Cu(NO3)2和La(NO3)3为起始原料、水为溶剂、柠檬酸为络合剂,采用溶胶—凝胶法制备。
-
(1) Cu2+基态核外电子排布式为。
-
(2) 与NO
 互为等电子体的阴离子为。
互为等电子体的阴离子为。
-
(3) 柠檬酸(结构简式为
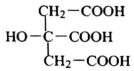 )分子中碳原子的轨道杂化类型为;1mol柠檬酸分子含σ键数目为mol。
)分子中碳原子的轨道杂化类型为;1mol柠檬酸分子含σ键数目为mol。
-
(4) 铜酸镧的晶胞结构如图所示,写出其化学式:。
下列关于化学用语的表示错误的是( )
A . Na+的轨道表示式: 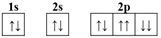 B . 氯离子的结构示意图:
B . 氯离子的结构示意图: 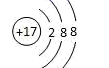 C . 原子核内有8个中子的氧原子:
C . 原子核内有8个中子的氧原子: 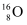 D . 硫离子的核外电子排布式:1s22s22p63s23p6
D . 硫离子的核外电子排布式:1s22s22p63s23p6
 C . 原子核内有8个中子的氧原子:
C . 原子核内有8个中子的氧原子: 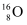 D . 硫离子的核外电子排布式:1s22s22p63s23p6
D . 硫离子的核外电子排布式:1s22s22p63s23p6
下列说法正确的是( )
A . 在共价化合物中不可能含有离子键
B . 阴阳离子之间通过静电引力形成的化学键,叫离子键
C . 含有共价键的化合物一定是共价化合物
D . 含有离子键的化合物不一定是离子化合物
下列叙述中错误的是( )
A . 氧化性:Na +<Mg2+<Al3+
B . 沸点:H2Se>H2S>H2O
C . 稳定性:HF>HCl>HBr
D . 酸性:HClO4>H2SO4>H3PO4
关于有机物的说法或表述中正确的是( )
A . 等质量的乙醇、乙烯在氧气中完全燃烧,消耗的氧气一样多
B . 与Br2反应的难易:苯>苯酚
C . 沸点: 1-丁醇>2-甲基丁烷>戊烷
D . 红外光谱仪、核磁共振仪都可用于有机物的结构分析
有机物F为重要的有机原料中间体,合成F的路线如图:
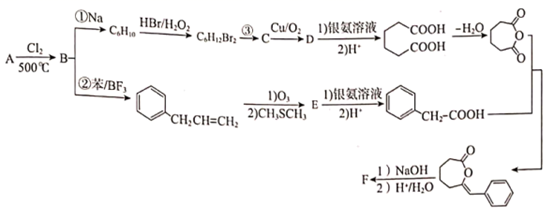
已知:I.烃A的相对分子量为42;
II.R-CH=CH2 ![]() R-CHO+HCHO:
R-CHO+HCHO:
III.R-Cl+2Na+Cl-R'→R-R'+2NaCl
IV.已知C=C-OH不稳定,原子会发生重排,例: 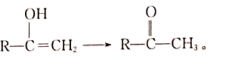
回答下列问题:
-
(1) 有机物B的名称是。
-
(2) E的结构简式是。
-
(3) 反应①的反应类型为;反应③所需的试剂和条件为。
-
(4) 反应②的化学方程式为。
-
(5)
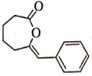 与NaOH反应的化学方程式为。
与NaOH反应的化学方程式为。
-
(6) 有机物
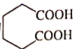 的同分异构体有多种,其中属于二元羧酸的同分异构体有种(不含立体异构)写出其中核磁共振氢谱显示只有3组峰的同分异构体的结构简式:。
的同分异构体有多种,其中属于二元羧酸的同分异构体有种(不含立体异构)写出其中核磁共振氢谱显示只有3组峰的同分异构体的结构简式:。
-
(7) 请写出用溴苯为原料制备己二酸(HOOCCH2CH2CH2CH2COOH)的合成路线(无机试剂任选)。
氮、磷属于同一主族元素,是组成生命体的重要元素,其单质及化合物在生活和生产中有许多重要用途。
-
(1) 有机铁肥中Fe的化合价为+3,Fe3+ 基态核外电子排布式为。
-
(2) (CH3)3N极易溶于H2O,除因为它们都是极性分子外,还因为。
-
(3) 如图所示的盐可用于处理黑磷纳米材料,从而保护和控制其性质。
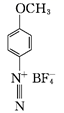
①该盐中碳原子的轨道杂化类型为。
②1 mol 该盐的阳离子含有σ键的数目为。
-
(4) 以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。磷化硼晶体晶胞的示意图是图1,图2是晶胞沿着体对角线方向的投影图。
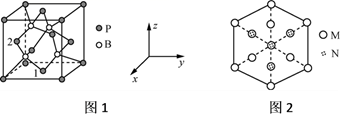
①图1中,原子1的分数坐标是
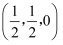 ,则原子2的分数坐标为。
,则原子2的分数坐标为。 ②图2中“N”球表示原子(填元素符号)。
根据下面图示回答问题:

-
(1) 图甲是某离子化合物的晶胞,阳离子位于体心,阴离子位于8个顶点,该化合物中阳、阴离子的个数比是。
-
(2) 若Ca、Ti、O形成的某钙钛矿型晶体的晶胞结构如图乙所示,其化学式为。
-
(3) 共价晶体硼的基本结构单元是由硼原子组成的正二十面体,如图丙。其中含有20个等边三角形和一定数目的顶角,每个顶角上各有1个原子。观察该晶胞,推断这个基本结构单元所含硼原子的个数、键角、B-B键的个数依次为、 、。
-
(4) 如图丁所示的物质结构中最外层已达8电子稳定结构的原子是(填元素符号),H3BO3晶体中B原子与极性键的个数比为。
-
(5) 金属铜具有很好的延展性传热性以及导电性,解释此现象最简单的理论是。
下列说法正确的是( )
A . H2和MgF2分子内都含有非极性共价键
B . H2O的热稳定性比H2S强,说明H2O的分子间作用力比H2S强
C . KCl、HCl和KOH的水溶液都能导电,所以它们都属于离子化合物
D . N2和CCl4分子中各原子的最外层电子数都满足8电子稳定结构
类推是化学学习和研究中常用的思维方法,下列类推正确的是( )
A . H2O2的热稳定性比H2O的弱,则C2H6的热稳定性比CH4的弱
B . 晶体中有阴离子,必有阳离子,则晶体中有阳离子,也必有阴离子
C . Mg—Al原电池,Mg的活泼性比Al强,在稀硫酸介质中,Mg做负极,则在稀氢氧化钠介质中,也是Mg做负极
D . 根据反应Fe(OH)3+3HCl=FeCl3+3H2O,可类推反应Fe(OH)3+3HI=FeI3+3H2O
稀土元素是指钪(Sc)、钇(Y)和镧系元素,共17种,位于元素周期表中第IIIB族,均为金属元素,在工业。生产中有重要的作用。回答下列问题:
-
(1) 钇(Y)位于元素周期表中钪(Sc)的下一周期,基态钇(Y)元素的原子价电子排布图为。
-
(2) 稀土元素常常能和许多配位体形成配合物。若一个配位体含有两个或两个以上的能提供孤电子对的原子,这种配位体就叫多齿配位体,其中有一个能提供孤电子对的原子为一齿(已知:碳氧双键中的氧原子不能提供孤电子对)。DEDTA(结构见图甲)是齿配位体,其中碳原子的杂化方式有,该物质中所含元素的电负性由大到小的顺序是。
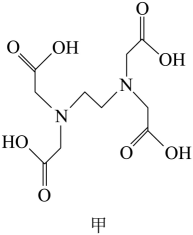
②EDTA与正二十一烷的相对分子质量非常接近,但EDTA的沸点(540.6℃)比正二十一烷的沸点(100℃)高得多,原因是。
-
(3) 钪(Sc)离子在水中以稳定的[Sc(H2O)6]3+存在,其空间构型为。
-
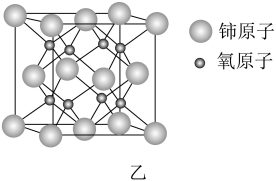
(4) 铈(Ce)属于镧系元素,氧化铈是一种重要的光催化材料。氧化铈的晶体结构如图乙所示,氧化铈的化学式为;若晶胞参数为anm,阿伏加德罗常数为NA , 则该晶体的密度=g/cm3(写出表达式)。
最近更新
- 读表1数据,回答甲地所处的地形单元为A.黄土高原 B.华北平原 C.内蒙古高原 D.长江中下游平原
- 在如下程序框图中,输入,则输出的是▲ _.
- 英语课上,老师要求同桌同学相互修改作文。假设以下便条为你同桌所写,请你对其进行修改。便条中共有10处错误,每句中最多有两
- 下图中的民居多见于我国的A.北方地区 B.南方地区 C.西北地
- 最近我国科学家在液流电池研究方面取得新进展。一种硫/碘体系(KI/K2S2)的液流电池工作原理如右图所示。下列说法正确的
- 某一生物有四对染色体,假设一个精原细胞产生的正常精细胞和异常精细胞的个数比为1:1.则该精原细胞在产生精细胞的过程中,最
- For many managers, “team building” means two days spent doin
- 质量相等的均质柔软细绳A、B平放于水平地面,绳A较长。分别捏住两绳中点缓慢提起,直到全部离开地面,两绳中点被提升的高度分
- 蒋介石曾告诉国民说:“我国自清季开始与列强订立不平等条约以来,到了去年正是百周年。我们中华民族经五十年的革命流血,五年半
- 以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是: A.该电池工作时电能转化为化学能 B.该电
- 营养学家建议青少年应多吃一些肉、蛋、鱼、奶等含蛋白质丰富的食品.因为蛋白质是() A.有机物
- 历史典故“烽火戏诸侯”中,周幽王为博宠妃一笑,点燃烽火,诸侯蜂拥而至勤王。这一典故反映的政治制度是A宗法制
- 中共十五届四中全会审议通过的《中共中央关于国有企业改革和发展若干重大问题的定》强调提出,要继续加强党对国有企业改革和发展
- 生活中,哲学无处不在、无事不有。生活与哲学的关系是( ) ①哲学指导人们更好的生活 ②哲学对我们的生活起着决定作用 ③哲
- 我国某地一寺庙佛门弟子积极参加当地架桥修路、捐资助学等活动,方丈还以80万巨资买到了电视台黄金时段前15秒公益广告权,宣
- The discovery of new evidence led to . A.the thief
- 等差数列的前n项和为,若则S等于 A. B. C.0
- 离子反应、复分解反应、置换反应和氧化还原反应之间可用集合关系表示,其正确的 是( )
- 甲、乙、丙三图分别表示几个环境因素对小麦光合作用速率的影响,除各图中所示因素外,其他因素均控制在适宜范围。请据图回答以
- 下列词语中没有错别字一项是( )。(2分) A.讴歌 深邃 五光十色 变换莫测 B.遗孀 诅咒



