第二章 分子结构与性质 知识点题库
实 验 步 骤 | 解 释 或 实 验 结 论 |
(1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空: (1)A的相对分子质量为:。 |
(2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g. | (2)A的分子式为: 。 |
(3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况). | (3)用结构简式表示A中含有的官能团: 。 |
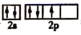
(4)A的核磁共振氢谱如下图:
| (4)A中含有 种氢原子。 |
(5)综上所述,A的结构简式 。 | |
|
元素 |
结构或性质信息 |
|
X |
原子的L层上s电子数等于p电子数 |
|
Y |
原子核外的L层有3个未成对电子 |
|
Z |
在元素周期表的各元素中电负性仅小于氟 |
|
M |
单质常温、常压下是气体,原子的M层上有1个未成对的p电子 |
|
R |
第四周期过渡元素,其价电子层各能级处于半充满状态 |
-
(1) 元素M的原子核外有 种不同运动状态的电子;
-
(2) 五种元素中第一电离能最高的是写元素符号;
-
(3) 在Y形成的单质中,
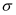 键与
键与 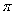 键数目之比为,在
键数目之比为,在 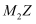 中Z原子的杂化方式为,其分子的空间构型为 ;
中Z原子的杂化方式为,其分子的空间构型为 ;
-
(4) R的一种配合物的化学式为
 。已知0.01mol
。已知0.01mol  在水溶液中用过量硝酸银溶液处理,产生0.02molAgCl沉淀,此配合物最可能是 ______填序号。
A .
在水溶液中用过量硝酸银溶液处理,产生0.02molAgCl沉淀,此配合物最可能是 ______填序号。
A . B .
B .  C .
C .  D .
D . 
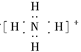 ,离子呈平面正方形结构
D . 用CCl4提取碘水中的碘单质
,离子呈平面正方形结构
D . 用CCl4提取碘水中的碘单质
①化学键断裂,一定发生化学变化
②任何物质中都存在化学键
③氢键是极弱的化学键
④离子键就是阴、阳离子之间的静电吸引力
⑤活泼金属与活泼非金属化合时能形成离子键
⑥任何共价键中,成键原子成键后均满足稳定结构
⑦验证化合物是否为离子化合物的实验方法是可以看其熔化状态下能否导电
⑧两种非金属元素形成的化合物不可能含有离子键
-
(1) 铁原子基态时核外电子排布式为,三氯化铁的熔点306℃、沸点315℃,由此判断三氯化铁属于晶体。
-
(2) 碳的电负性比硫(填“大”“小”或“相等"),碳、氮、氧元素第一电离能由大到小的顺序为 (填元素符号)。
-
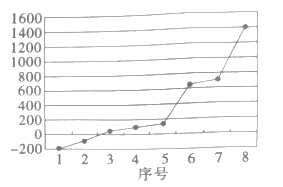
(3) 硫元素所在周期的8种元素的单质熔点如图所示,其中序号“8”代表 (填元素符号);形成最高价氧化物对应水化物酸性最强的是 (填图中的序号)。
-
(4) CS2分子的空间构型为,C原子的价层电子对数为。
-
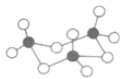
(5) 固态SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为;该分子中含有个σ键。
-
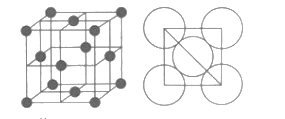
(6) 铝单质的晶胞特征及原子之间相互位置关系如图所示,若已知铝的原子半径为dcm,NA代表阿伏加德罗常数,铝的相对原子质量为M,则该晶体的密度为 g/cm3(用字母表示)。
-
(1) 金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价层电子的排布式为 ;基态 Mn原子核外有种运动状态不同的电子,M层的电子云有种不同的伸展方向。
-
(2) 第四周期元素的第一电离能随原子序数增大,总趋势是逐渐增大的,但Ga的第一电离能明显低于Zn,原因是
-
(3) NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验 K+的存在。与NO2-互为等电子体的微粒(写出一种),K3[Co(NO2)6]中存在的作用力有a.σ键 b.π键 c.配位键 d.离子键 e.范德华力
-
(4) 锰的一种配合物的化学式为 Mn(BH4)2(THF)3 , BH4-的空间构型为
-
(5) FeO 是离子晶体,其晶格能可通过下图中的 Born—Haber 循环计算得到。

可知,O原子的第一电子亲和能为 kJ•mol-1 , FeO晶格能为kJ•mol-1。
-
(6) 铜与氧可形成如图所示的晶胞结构,其中 Cu 均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(1/2,1/2,1/2),则 d 点的坐标参数为,已知该晶体的密度为ρg•cm-3 , NA是阿伏加德罗常数的值,则晶胞参数为pm
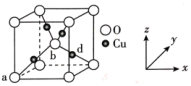
(列出计算式即可)
-
(1) Ni在元素周期表中的位置是, 其价电子层中有个未成对电子。
-
(2) 纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属于 ( 填“极性”“非极性”)分子,其立体构型为。
-
(3) 铁、钴、镍三种元素并称铁系元素,它们的性质相似。某含镍化合物的结构如图所示,则分子内不可能含有_______(填字母)。A . 离子键 B . 共价键 C . 金属键 D . 配位键 E . 氢键
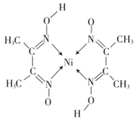
-
(4) TiO2能溶于浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形式存在的钛酰阳离子,其结构如图所示,其化学式为。阴离子
 中硫原子的杂化方式为,写出一种与
中硫原子的杂化方式为,写出一种与  互为等电子体的分子:。
互为等电子体的分子:。 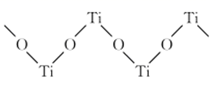
-
(5) 自然界的钛主要以金红石(主要成分为TiO2 )的形式存在。TiO2的晶胞属于四方晶系,其长方体结构如图所示,已知TiO2的摩尔质量为Mg·mol-1 , 阿伏加德罗常数的数值为NA , 根据图中所示数据可知该晶体的密度ρ= (用NA表示阿伏加德罗常数的数值,用含M、a、b、c、NA的代数式表示)g·cm-3。
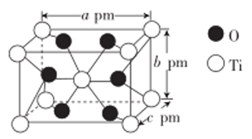
-
(1) 电负性:NO(填“>” 或“<”),基态氮原子价电子排布图不是
 ,是因为该排布方式违背了。
,是因为该排布方式违背了。
-
(2) 肼(H2N-NH2)分子中孤电子对与σ键的数目之比为,肼的相对分子质量与乙烯接近,但沸点远高于乙烯的原因是。
-
(3) 正硝酸钠(Na3NO4)为白色晶体,是一种重要的化工原料。
①写出与Na3NO4的阴离子互为等电子体的一种阴离子:(填化学式)。
②在573K条件下,实验室中用NaNO3和Na2O在银皿中反应制得Na3NO4 , Na2O的立方晶胞如图所示。Na2O晶胞的参数为a pm,则晶胞密度为g/cm3(列出计算式即可,NA为阿伏加德罗常数的值)。
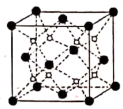
-
(1) 向NaHCO3溶液中加入A,有气体放出,说明A中含有的官能团是(写名称)。
-
(2) 向NaOH溶液中加入少许A,加热一段时间后,冷却,用HNO3酸化后再滴加AgNO3溶液,产生淡黄色沉淀,说明A中还含有的官能团是 (写名称)。
-
(3) 经质谱分析,A的相对分子质量为153,且A中只有四种元素,则A的分子式为。
-
(4) 核磁共振氢谱显示,A的氢谱有3种,其强度之比为1:2:2,则A的结构简式为 。
-
(5) 已知A可发生如图所示的转化:
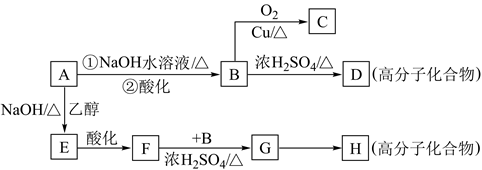
①A→E、F→G的反应类型分别为、。
②写出B→ D反应的化学方程式:。
③写出H的结构简式: 。
④C与过量的银氨溶液反应,每生成3.24gAg,消耗C的物质的量是 mol。
- ---I hear Ted got hurt badly in the caraccident yesterday.
- “世上疮痍,诗中圣哲;民间疾苦,笔底波澜。”郭沫若写的这副对联是在称颂A.屈原 B.杜甫
- 完型填空。Young people are often unhappy when they are with their
- “月亮既不会掉下来,也不会离去,那是因为它的运动正好抵消了地球的引力。”说这句话的科学家是( ) A.牛顿 B.波
- 下图为我国某区域简图,回答1~2题。1.导致甲、乙两地气温低于同纬度其他地区的主要原因是( ) A.黄河流经
- 城市化的主要动力是 ( ) A.人口数量增多 B.
- t℃时,在饱和硫酸铜溶液中加入a g无水硫酸铜,恢复至原温度可析出b g硫酸铜晶体.说法正确的是 () A.溶液中溶剂的
- (2011年福建福州,5题)下列化学用语与含义不相符的是A、AlCl3—氯化铝 B、Ca2+—钙离子 C、
- Florida farmerLohfner doesn't like moths(蛾). They eat my veg
- 若6≤a≤10,a≤b≤2a,c=a-b,求c的取值范围.
- 下列各句中语意明确的一句是 ( ) A.会计未按经理
- 下列词语中加点的字,每对读音都不相同的一组是( ) A.称道/称心如意 躯壳/金蝉脱壳 下载/
- 杠杆的平衡条件是:__________。用动力臂150厘米、阻力臂30厘米的撬杠撬起3000牛顿的石头,所用的动力至少要
- 某科学家在研究细胞膜运输物质时发现有下列四种关系,分别用四种曲线表示:在研究具体的物质X时,发现与曲线②和④相符,试问:
- 公安部10月8日公布了最新修订的《机动车驾驶证申领和使用规定》,新交通规则严格了对驾驶员的管理,新交通法规扣分细则也更为
- —Would you mind if I open the window? ---_______. We need
- David decided not to work on the program in the office becau
- 从同一地点同时开始沿同一方向做直线运动的两个物体A、B的速度图象如图所示。在0―t0时间内,下列说法中正确的是(
- By _____, water can be changed into gas.A.heating B
- Is human blood all the same? “Yes,” you may say.“It's all re