第二章 分子结构与性质 知识点题库
下列有机化合物中沸点最低的是( )
A . 乙酸乙酯
B . 乙酸丁酯
C . 丁醇
D . 乙酸
氧是地壳中含量最多的元素.
(1)氧元素基态原子核外未成对电子数为 个.
(2)H2O分子内的O﹣H键、分子间的范德华力和氢键从强到弱依次为 .  的沸点比
的沸点比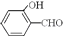 高,原因是
高,原因是
(3)H+可与H2O形成H3O+ , H3O+原子采用 杂化.H3O+中H﹣O﹣H键角比H2O中H﹣O﹣H键角大,原因为
下列分子属于手性分子的是( )
A . H2O
B . 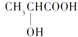 C .
C . 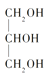 D . H2N﹣CH2﹣COOH
D . H2N﹣CH2﹣COOH
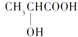 C .
C . 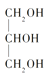 D . H2N﹣CH2﹣COOH
D . H2N﹣CH2﹣COOH
下列能跟氢原子形成最强极性键的原子是( )
A . F
B . Cl
C . Br
D . I
可确定乙二醇分子是否有极性的实验是( )
A . 测定沸点
B . 测静电对液流影响
C . 测定蒸气密度
D . 测标准状况下气体摩尔体积
铜单质及其化合物在很多领域有重要的用途,如铜用来制电缆,五水硫酸铜可用作杀菌剂.
-
(1) 将一块缺角的硫酸铜晶体置于饱和硫酸铜溶液中会慢慢变成了完整晶体,这一现象体现了晶体的性,若不考虑溶剂挥发,硫酸铜溶液的质量.(填“变大”、“变小”或“不变”)
-
(2) 往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子,已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是.
-
(3) [Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl﹣取代,能得到两种结构不同的产物,则[Cu(NH3)4]2+的空间构型为.(填“正四面体形”或“正四边形”)
-
(4) 胆矾CuSO4•5H2O可写[Cu(H2O)4]SO4•H2O,其结构示意如图1:
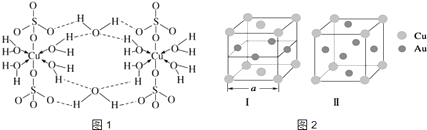
下列有关胆矾的说法不正确的是 .
A . 游泳池的池水中往往定期加一些胆矾,是因为铜离子有一定的杀菌作用 B . 胆矾中氧原子存在配位键和氢键两种化学键 C . Cu2+的价电子排布式为3d84s1 D . 胆矾中的水在不同温度下会分步失去 -
(5) 《X射线金相学》中记载了关于铜与金可形成的两种有序的金属互化物,其晶胞如图2.则图中Ⅰ、Ⅱ对应物质的化学式分别为、.设图Ⅰ晶胞的边长为α cm,对应金属互化物的密度为ρ g•cm﹣3 , 则阿伏加德罗常数NA的值可表示为.(只要求列出算式).
Co3+的八面体配合物为CoClm•nNH3 , 若1mol此配合物与AgNO3作用生成1molAgCl沉淀,则m、n的值是( )
A . m=1,n=5
B . m=4,n=3
C . m=3,n=4
D . m=4,n=5
下列各项比较中前者高于(或大于或强于)后者的是( )
A . CCl4和SiCl4的熔点
B . NH3与H2O的键角
C . SO2和CO2在水中的溶解度
D . 碳化硅和金刚石的硬度
下列说法合理的是( )
A . 液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
B . 由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S
C . 邻羟基苯甲醛沸点高于对羟基苯甲醛是因为形成了分子内氢键
D . 若X+和Y2﹣的核外电子层结构相同,则原子序数:Y<X
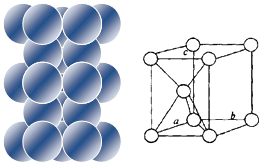
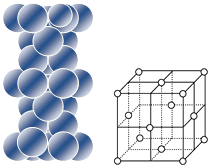
金属镁是六方最密堆积,金属铜是面心立方最密堆积,图分别给出它们的堆积状况和晶胞示意图,它们空间利用率相同,假定镁、铜原子均为刚性小球,已知球的半径分别为R1厘米、R2厘米,阿伏加德罗常数的值为NA
| ①镁原子在二维空间的配位数为 ②位于晶胞中部的镁原子与离它最近两平面(填“相离”或“相切”或”相交”) |
| ③铜原子在三维空间的配位数为 ④请用含R2、NA的数学式子表达金属铜的密度: g/cm3(根号带在分子上) |
第四周期中的18中元素具有重要的用途,在现代工业中备受青睐.
-
(1) 铬是一种硬二脆,抗腐蚀性强的金属,常用于电镀和制造特种钢.基态Cr原子中,电子占据最高能层的符号为,该能层上具有的原子轨道数为,电子数为,
-
(2) 第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,30Zn与31Ga的第一电离能是否符合这一规律?(填“是”或“否”),原因是(如果前一问填“是”,此问可以不答)
-
(3) 镓与第VA族元素可形成多种新型人工半导体材料,砷化镓(GaAs)就是其中一种,其晶体结构如下图所示(白色球代表As原子).在GaAs晶体中,每个Ga原子与个As原子相连,与同一个Ga原子相连的As原子构成的空间构型为;
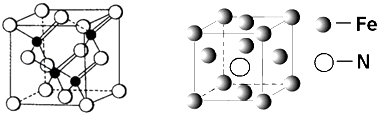
-
(4) 与As同主族的短周期元素是N、P.AsH3中心原子杂化的类型;一定压强下将AsH3和NH3 . PH3的混合气体降温是首先液化的是,理由是;
-
(5) 铁的多种化合物均为磁性材料,氮化铁石期中一种,某氮化铁的井胞结构如图所示,则氮化铁的化学式为;设晶胞边长为acm,阿伏加德罗常数为NA , 该晶体的密度为 g.cm﹣3(用含a和NA的式子表示)
下列说法错误的是( )
A . 蒸馏时应调整温度计的水银球于蒸馏烧瓶支管口附近
B . 提纯液体混合物常用重结晶法
C . 萃取是利用溶质在两种互不相溶的溶剂中溶解度的不同,使溶质从一种溶剂内转移到另一种溶剂的操作
D . 常用质谱法进行有机物相对分子质量的测定
下列分子或离子中,中心原子不是sp3杂化的是( )
A . SO42﹣
B . NO3﹣
C . CH4
D . H2S
A,B,C,D,E,F 为前四周期元素且原子序数依次增大,其中基态 A 原子的电子分布在 3 个能级,且每个能级所含的电子数相同; C 的原子核外最外层有 6 个运动状态不同的电子; D 是短周期元素中电负性最小的元素; E 的最高价氧化物的水化物酸性最强; 基态 F 原子核外最外层只有一个电子, 其余能层均充满电子。 G 元素与 D 元素同主族,且相差 3 个周期。
-
(1) 元素 A,B,C 的第一电离能由小到大的是(用元素符号表示)。
-
(2) E的最高价含氧酸中 E 原子的杂化方式为。 基态 E 原子中,核外电子占据最高能级的电子云轮廓形状为。
-
(3) F原子的外围电子排布式为, F 单质晶体中原子的堆积方式是下图中的(填写“甲”、 “乙”或“丙”) ,该晶体的空间利用率为。(保留两位有效数字)
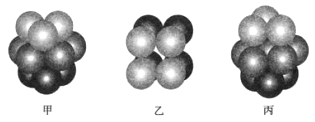
-
(4) 已知元素 A、B形成的(AB)2分子中所有原子都满足 8电子稳定结构,则其分子中 σ键与 π键数目之比为。
-
(5) 通常情况下, D 单质的熔沸点比 G 单质高,原因是。
-
(6) 已知 DE 晶体的晶胞如下图所示:
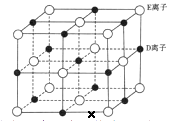
若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示 A的一种晶体的晶胞(已知 A—A 键的键长为a cm, NA表示阿伏加德罗常数),则该晶胞中含有个 A 原子,该晶体的密度是g·cm-3(列式表示) 。
某有机化合物A经李比希法测得其中含碳为70.59%、含氢为 5.88%,其余含有氧。现用下列方法测定该有机化合物的相对分子质量和分子结构。
方法一:用质谱法分析得知A的相对分子质量为136。
方法二:核磁共振仪测出A的核磁共振氢谱有4个峰,其面积之比为1∶2∶2∶3。如下图。
方法三:利用红外光谱仪测得A分子的红外光谱,如下图。
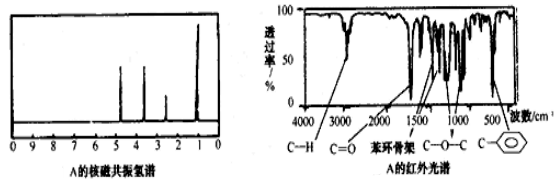
-
(1) 分子中共有种化学环境不同的氢原子。
-
(2) A的分子式为。
-
(3) 该物质属于哪一类有机物。
-
(4) A的分子中只含一个甲基的依据是(填序号)。
a.A的相对分子质量
b.A的分子式
c.A的核磁共振氢谱图
d.A分子的红外光谱图
-
(5) A的结构简式为。
-
(6) A的芳香类同分异构体有多种,其中又同时符合下列条件:①属于酯类;②分子结构中含有一个甲基。则该芳香类A的同分异构体共有种。
H2 和 I2 在一定条件下能发生反应:H2(g) +I2(g)  2HI(g) △H= -a kJ/mol
2HI(g) △H= -a kJ/mol
 2HI(g) △H= -a kJ/mol
2HI(g) △H= -a kJ/mol
已知:
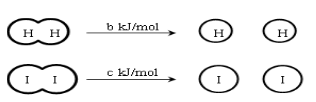 (a、b、c 均大于零)
(a、b、c 均大于零)
下列说法正确的是( )
A . 碰撞理论认为,反应速率的大小与单位时间内反应物微粒间碰撞次数成正比,只要有足够的能量就可以发生有效碰撞
B . 断开 2 mol HI 分子中的化学键所需能量约为(c+b+a) kJ
C . 相同条件下,1 mol H2 (g)和 1mol I2 (g)总能量小于 2 mol HI (g)的总能量
D . 向密闭容器中加入 2 mol H2 (g)和 2 mol I2 (g),充分反应后放出的热量为 2a kJ
NaCl的玻恩-哈伯循环如图所示。已知:将1mol金属转变成气态原子所需的最小能量称为原子化热。下列说法错误的是( )
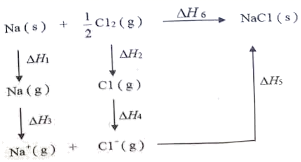
A . Na(s)的原子化热为△H1
B . Na的第一电离能为△H3
C . Cl-Cl键的键能为△H2
D . NaCl的晶格能为△H5
下列有关化学用语表示正确的是( )
A . 由H和 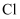 形成
形成  的过程:
的过程: 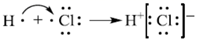 B . 任一能层的s电子电子云轮廓图的形状:圆形
C .
B . 任一能层的s电子电子云轮廓图的形状:圆形
C .  中心原子的杂化轨道类型:
中心原子的杂化轨道类型: 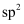 D . 聚乙烯的链节:
D . 聚乙烯的链节: 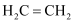
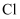 形成
形成  的过程:
的过程:  中心原子的杂化轨道类型:
中心原子的杂化轨道类型: 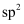 D . 聚乙烯的链节:
D . 聚乙烯的链节: 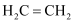
下列说法错误的是( )
A . 原子光谱是测定物质结构的基本方法和实验手段
B . 霓虹灯能够发出五颜六色的光,其发光机理与氢原子光谱形成机理基本相同
C . 原子线状光谱的产生是原子核外电子在不同的、能量量子化的状态之间跃迁所导致的
D . 钠原子光谱中的靠得很近的两条黄色谱线可以利用玻尔原子结构模型较好地解释
下列事实不能说明氮和氧非金属性相对强弱的是( )
A . 热稳定性:H2O>NH3
B . 常温下水为液体而氨为气态
C . NO中N为+2价,氧为-2价
D . NH3在纯氧中燃烧可生成N2
最近更新
- 关于秦岭一淮河线的叙述,错误的是( )A .湿润地区与半湿润地区的分界线B .亚热带与暖温带的分界线C .北方地区与南方
- 已知集合A={x∈R|ax2-3x+2=0,a∈R}. (1)若A是空集,求a的取值范围; (2)若A中只有一个元素,求
- 如图注:第六次人口普查同第五次相比,65岁及以上人口(老年人口)的比重上升1.91%。上述图表表明我国在人口方面存在的问
- 下列句子中,加粗的熟语运用不正确的一项是( ) A.世贸大楼废址已成为纽约新的旅游景点,游人看后无不神色黯然,叹为
- 阅读材料,回答问题。 信息一:改革开放以来,我国政府不断创造新形式,尝试新方法,为公民行使监督权、参与民主监督提供更多、
- 下列各组物质,按混合物、化合物、单质顺序排列的是() A.冰水共存物、干冰、氮气 B.石油、煤、天然气 C.洁净的空
- 在北方的冬季,常见的几种物态变化现象中,属于液化的是 ( ) A.室外冻冰的衣服变干 B.房间窗户玻璃的内
- 了解英国君主立宪确立之初的情况,下列文献可供参考的是 A.《权利法案》 B.《独立宣言》 C.《人
- 随着工业革命的推进,19世纪上半期英国出现的新的社会问题是 A. 清教徒受到迫害
- “硅谷”是高新技术产业基地的代名词,美国的硅谷位于A.东北部工业区B.南部工业区C.旧金山东南D.五大湖沿岸
- 电子排布式为1s22s22p63s23p5,其对应的元素为()。A. K B. S C. Cl
- 5.依次填入下面一段文字横线处的语句,衔接最恰当的一组是( )(3分) 这其实也正是一切高贵者的通病。
- 依次填入下列句中空缺处的词语恰当的一项是( ) (1)历史已雄辩地 ,人民群众的巨大支持和无私奉献,是
- 下列反应没有涉及原电池的是
- 请将六棱柱的三视图名称填在相应的横线上.
- 判断下列向量a与b是否共线.(1)a=(,),b=(-2,-3);(2)a=(0.5,4),b=(-8,64).
- ---I hear that Xiao Li was hurt in the accident. ---Yes, he
- 下列各项中最能体现中国在国际社会长期发挥了重要作用的是( ) A 担任联合国安理会常任理事国 B 在亚非会议上
- 《论语》十二章 (1)人要进步,“俯而学”和“仰而思”不可偏废。《<论语>十二章》里,孔子用“, ”阐明了“
- 下列各句中,没有语病、句意明确的一句是 A.十一届全国人大二次会议新闻中心昨天下午举行了“文化市场与文化产业发展”专题采