第四节 氨 硝酸 硫酸 知识点题库
某些的自来水是采用氯气消毒的,为了检验Cl﹣的存在,最好选用下列物质中的( )
A . 石蕊溶液
B . 四氯化碳
C . 氢氧化钠
D . 硝酸银、硝酸
下列有关化学概念或原理的论述中,正确的是( )
A . Cl2、SO2、NH3的水溶液虽都能够导电,但它们均属于非电解质
B . 在浓硝酸中加入等体积浓硫酸后,立即加入铝片,铝片发生钝化
C . 任何可逆反应,其平衡常数越大,反应速率、反应物的转化率就越大
D . 电解饱和食盐水的过程中,水的电离平衡正向移动
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解l9.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁质量增加的变化如图所示.下列分析或结果错误的是( )
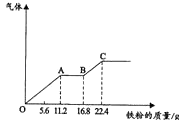
A . 原混合酸中NO3﹣物质的量为0.4mol
B . OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+ , BC段产生氢气
C . 第二份溶液中最终溶质为FeSO4
D . H2SO4浓度为2.5mol•L﹣1
某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应.其中A、F为氯气和氨气的发生装置,D为纯净、干燥的氯气与氨气反应的装置.
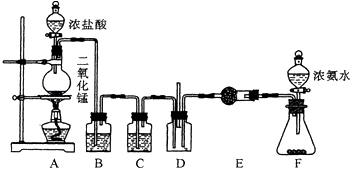
请回答下列问题:
-
(1) F中所装的固体试剂是
-
(2) 洗气瓶B的作用是.C、E都是干燥装置,其中E中干燥管内所装的试剂是
-
(3) 反应开始后装置D中出现浓厚的白烟并在容器内壁凝结,活动小组拟继续通过实验鉴定该固体的成分.请你协助他们完成该实验探究.
步骤①:取固体样品加少量水溶解,分装于两支试管中.向其中一支试管中加入浓NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口附近,红色石蕊试纸变蓝,证明该固体中含有
步骤②:
-
(4) 从绿色化学的角度考虑该装置中有一明显不合理之处,请你提出改进的意见..
某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体.为此,他们设计了如题装置验证所产生的气体.
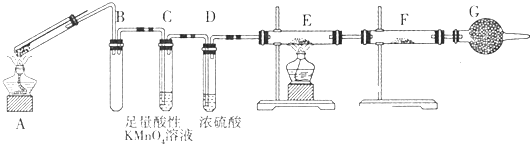
-
(1) G装置的作用是.
-
(2) 证明有SO2生成的现象是,为了证明气体中含有氢气,装置E和F中加入的试剂分别为、.
-
(3) 若将铁丝换成铜丝,反应后的溶液没有出现预计的蓝色溶液,而出现了大量白色固体,原因是.
如下图所示,集气瓶内充满某混合气体(括号内为体积比),若将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,则集气瓶中的混合气体可能是( )
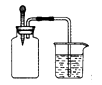
①CO、O2 (2:1) ②NH3 、O2(8:1)③NO2、O2(4:1) ④N2、H2(1:3)
A . ①②
B . ②③
C . ②④
D . ③④
下列有关实验能达到相应实验目的的是( )
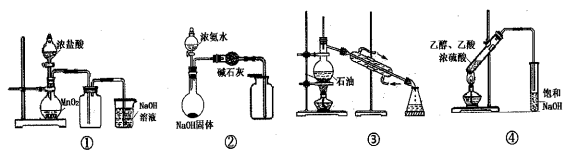
A . 实验①用于实验室制备氯气
B . 实验②用于制备干燥的氨气
C . 实验③用于石油分馏制备汽油
D . 实验④用于制备乙酸乙酯
下列叙述不属于固氮的是( )
A . 工业上合成氨
B . NH3经催化氧化生成NO
C . 闪电时,大气中生成NO
D . 豆科植物根部的根瘤菌使空气中的氮气转变为铵态氮肥
仅用下表提供的仪器和用品能够实现相应目的的是( )
| 选项 | 实验目的 | 仪器和药品 |
| A | 从碘水中提取碘 | 铁架台、烧杯、分液漏斗、酒精 |
| B | 检验溶液中是否含有SO42- | 试管、胶头滴管、BaCl2溶液 |
| C | 验证非金属性:Cl>C | 试管、胶头滴管、盐酸、小苏打 |
| D | 配制100mL0.1mol/L NaOH溶液 | 天平、药匙、烧杯、玻璃棒、100容量瓶、胶头滴管、烧碱、水 |
A . A
B . B
C . C
D . D
下列金属或氧化物可以完全溶解的是( )
A . 1molZn与含1molHCl的稀盐酸共热
B . 1molCu与含2molH2SO4的浓硫酸共热
C . 1molCu与含4molHNO3的浓硝酸
D . 1molMnO2与含4molHCl的浓盐酸共热
将3.2 gCu投入到一定浓度的HNO3 溶液中,恰好完全反应,产生NO2 和NO的混合气体共 0.08 mol。则原溶液中HNO3 的物质的量为( )
A . 0.34 mol
B . 0.38 mol
C . 0.28 mol
D . 0.18 mol
已知NH4++AlO2-+2H2O=Al(OH)3↓+NH3·H2O,向含有等物质的量的NH4+、Al3+、H+的混合溶液中,慢慢滴加NaOH溶液直至过量,并不断搅拌,发生以下离子反应:
①H++OH-=H2O
②Al(OH)3+OH-=AlO2-+2H2O
③Al3++3OH-=Al(OH)3↓
④NH4++OH-=NH3·H2O
先后顺序正确的是( )
A . ①→②→③→④
B . ①→③→②→④
C . ①→③→④→②
D . ①→④→②→③
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A . NaCl(aq)  Cl2(g)
Cl2(g)  FeCl2(s)
B . Ca(ClO)2(aq)
FeCl2(s)
B . Ca(ClO)2(aq) 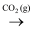 HClO(aq)
HClO(aq)  O2(g)
C . MgCl2·6H2O
O2(g)
C . MgCl2·6H2O  MgCl2
MgCl2 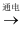 Mg
D . NH3(g)
Mg
D . NH3(g) 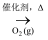 NO(g)
NO(g)  HNO3(aq)
HNO3(aq)
 Cl2(g)
Cl2(g)  FeCl2(s)
B . Ca(ClO)2(aq)
FeCl2(s)
B . Ca(ClO)2(aq) 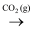 HClO(aq)
HClO(aq)  O2(g)
C . MgCl2·6H2O
O2(g)
C . MgCl2·6H2O  MgCl2
MgCl2 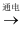 Mg
D . NH3(g)
Mg
D . NH3(g) 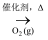 NO(g)
NO(g)  HNO3(aq)
HNO3(aq)
下列有关SO3的说法中正确的是( )
A . SO3极易溶于水,且与水反应生成H2SO4
B . SO3是碱性氧化物
C . 将SO3加入BaCl2溶液无明显现象
D . SO2、SO3均具有漂白性,能使紫色石蕊试液褪色
将铁钉投入热的浓硝酸中,一段时间后,下列说法错误的是( )
A . 铁钉表面形成致密的氧化膜
B . 溶液可能呈棕黄色
C . 铁钉会溶解
D . 产生红棕色的气体
利用下图装置进行实验,烧杯中不会出现沉淀的是( )
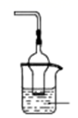
| A | B | C | D | |
| 气体 | 硫化氢 | 二氧化碳 | 氨气 | 氯化氢 |
| 溶液 | 亚硫酸 | 氯化钙 | 氯化铝 | 硝酸银 |
A . A
B . B
C . C
D . D
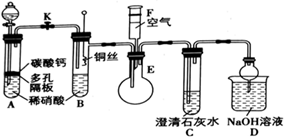
某校课外活动小组为了探究铜与稀硝酸反应产生的气体是否为NO,设计了如下实验。实验装置如图所示(已知NO、NO2能与NaOH溶液反应):
-
(1) 设计装置A的目的是:,写出试管A中发生的离子方程式:。
-
(2) 在(1)中的操作后将装置B中铜丝插入稀硝酸,并微热,观察到装置B中的现象是:;B中反应的离子方程式是:;
-
(3) 将注射器F中的空气推入E中,E中的气体变为红棕色,此时发生的化学方程式:;
-
(4) D装置的作用是:。
工业上用饱和食盐水吸收尾气 和
和 制备无水
制备无水 , 同时得到副产物
, 同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
 和
和 制备无水
制备无水 , 同时得到副产物
, 同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):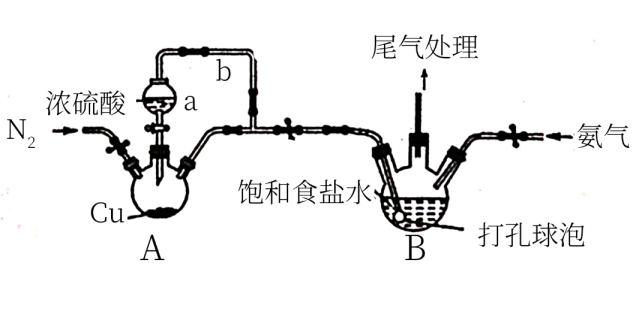
已知:浓硫酸的沸点为338℃.回答下列问题:
-
(1) 仪器a的名称,导气管b的作用.
-
(2) 装置A中发生的化学反应的化学方程式为.
-
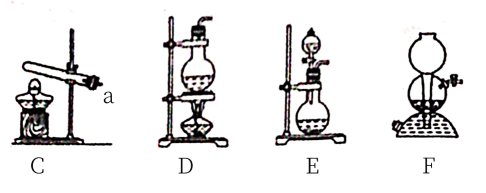
(3) 氨气的发生装置可以选择下图中的(填编号),反应的化学方程式为.
-
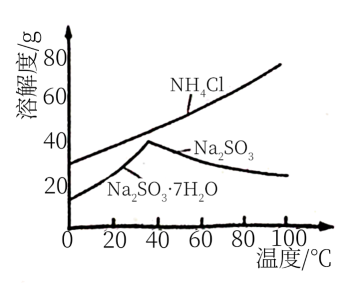
(4) 利用各物质的溶解度曲线图(见图)分离产品.取出装置B中的溶液,蒸发浓缩,趁热过滤可得,然后将滤液、过滤、洗涤、干燥可得另一产物.
-
(5) 产品中可能混有少量
 和
和 杂质,混有
杂质,混有 杂质的原因可能是检验产品中含有
杂质的原因可能是检验产品中含有 的的实验方法:取少量样品于试管中,加入适量水溶解,。(可选试剂:稀硝酸、
的的实验方法:取少量样品于试管中,加入适量水溶解,。(可选试剂:稀硝酸、 溶液、酸性
溶液、酸性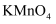 溶液、
溶液、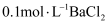 溶液、
溶液、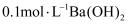 溶液、
溶液、 溶液)
溶液)
下列判断正确的是( )
A . 酸性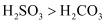 , 则硫元素的非金属性比碳元素强
B . 向含有
, 则硫元素的非金属性比碳元素强
B . 向含有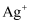 、
、 的溶液中加入足量的Fe粉,先析出Ag,后析出Cu,则金属性Fe>Cu>Ag
C . 向某无色溶液中加入少量
的溶液中加入足量的Fe粉,先析出Ag,后析出Cu,则金属性Fe>Cu>Ag
C . 向某无色溶液中加入少量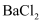 溶液,有白色沉淀产生,则该溶液中一定含有
溶液,有白色沉淀产生,则该溶液中一定含有 D . 相同质量的Al和Fe与足量的稀盐酸反应,Al放出的
D . 相同质量的Al和Fe与足量的稀盐酸反应,Al放出的 多,则Al的金属性比Fe强
多,则Al的金属性比Fe强
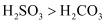 , 则硫元素的非金属性比碳元素强
B . 向含有
, 则硫元素的非金属性比碳元素强
B . 向含有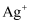 、
、 的溶液中加入足量的Fe粉,先析出Ag,后析出Cu,则金属性Fe>Cu>Ag
C . 向某无色溶液中加入少量
的溶液中加入足量的Fe粉,先析出Ag,后析出Cu,则金属性Fe>Cu>Ag
C . 向某无色溶液中加入少量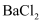 溶液,有白色沉淀产生,则该溶液中一定含有
溶液,有白色沉淀产生,则该溶液中一定含有 D . 相同质量的Al和Fe与足量的稀盐酸反应,Al放出的
D . 相同质量的Al和Fe与足量的稀盐酸反应,Al放出的 多,则Al的金属性比Fe强
多,则Al的金属性比Fe强
自然界中氮的循环如下图所示,下列有关说法正确的是( )
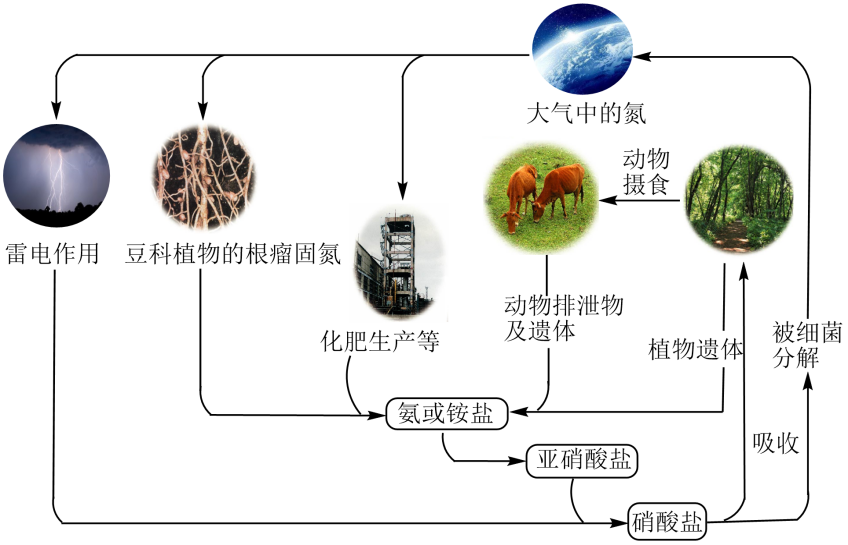
A . 氮气约占空气总体积的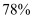 B . 豆科植物的固氮属于人工固氮
C . 雷电作用时
B . 豆科植物的固氮属于人工固氮
C . 雷电作用时 与
与 反应生成
反应生成 D .
D . 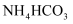 应保存在干燥、温暖之处
应保存在干燥、温暖之处
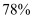 B . 豆科植物的固氮属于人工固氮
C . 雷电作用时
B . 豆科植物的固氮属于人工固氮
C . 雷电作用时 与
与 反应生成
反应生成 D .
D . 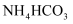 应保存在干燥、温暖之处
应保存在干燥、温暖之处
最近更新
- (08年广东卷) 把下列句子组成语意连贯的一段文字,排序最恰当的一项是 ①《禹贡》主要以山脉、河流和海洋为自然分界
- 若a=2,a﹣2b=3,则2a2﹣4ab的值为
- 化学反应在防治环境污染中扮演了重要角色。某工厂废气中的SO2,可用以下方式处理。方式一:2SO2+O2+2CaO=2Ca
- (08年盐城市摸底考试)(4分)从某金属表面逸出光电子的最大初动能与入射光的频率的图像如下图所示,则这种金属的截止频率是
- 从水平匀速飞行的直升机上向外自由释放一个物体,不计空气阻力,在物体下落过程中,下列说法正确的是( ) A.从飞机上
- 在胰岛B细胞合成、分泌胰岛素的过程中,具有降血糖作用的胰岛素最可能出现在 A.内质网腔中
- 结合语境根据拼音在田字格里写出相应的词语,为加点字注音。 优秀的文学作品,凝聚着人类灿烂的智慧和美好的感情,拨动着无数人
- 在一定条件下,若物体运动的路程s(米)与时间t(秒)的关系式为,则当时,该物体所经过的路程为()A.28米B.48米C.
- 下列各句中,没有语病的一项是 ( ) A.我写了一部描写农村现状的小说《空槐》以后,便一发而不可收拾,又接连写了几
- 夜雨寄北 李商隐 君问归期未有期,巴山夜雨涨秋池。 何当共剪西窗烛,却话巴山夜雨时。这首诗写了哪两种不同的时间和空间?
- 作文(50分)请以“我生活在 中”为题,写一篇文章。要求:①先将题目补充完整,然后写作;②你可以大胆
- 一元二次方程4x2+1=4x的根的情况是() A.没有实数根 B.只有一个实数根 C
- 如果你为四郎哭泣 龙应台 ①经济学家、社会学家、人类学家可能找得出100个方式来回答“文化为什么重要”这个问题,但是我可
- 下列叙述正确的是 A.因为水分子之间有间隙,所以水存在三态变化 B.因为原子中质子数等于中子数,所以原子不显电性 C.因
- 某化学兴趣小组为了测定当地矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀
- 恩格斯说:“封建制度巨大的国际中心是罗马天主教会。它在尽管发生各种内部战争的条件下还是把整个封建的西欧联合为一个大的政治
- 每年春节来临之际,商家们真是“商”透脑筋地搞各种各样的促销活动:或纷纷推出特价商品,或购物达到一定金额送一定的购物券,或
- 某旅行网站在2014年世界杯期间,上线了高端美食频道,使球迷在旅途中不仅可以订酒店订机票,在想看球的时候还可以查找美食场
- 产业革命时期形成的人口增长模式是: A.“低—高—低”模式 B.“高—高—
- 罗素评价人文精神的发展历程是“从古代的朦胧稚嫩发展到明确成熟”。其中“朦胧稚嫩”时期是指() A.古希腊智者学派对人的



