第四章 非金属及其化合物 知识点题库
-
(1) 硅是无机非金属材料的主角.玻璃是重要的硅酸盐产品之一,实验室保存
 溶液的试剂瓶不能用玻璃塞,原因可用化学方程式表示: .
溶液的试剂瓶不能用玻璃塞,原因可用化学方程式表示: . 铝制品表面有一层氧化铝薄膜而经久耐用,但该氧化膜易被酸、碱破坏,现要将氧化铝与氢氧化钠溶液作用,写出该反应的离子方程式:
-
(2) 生活中常用氯系消毒剂,比如漂白粉的有效成分是(写化学式),已知现榨的苹果汁中含
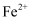 ,在空气中会由淡绿色变为棕黄色,则这个变色过程中的
,在空气中会由淡绿色变为棕黄色,则这个变色过程中的 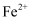 被(填“氧化”或“还原”,下同).若榨汁时加入适量的维生素C,可有效防止这种现象的发生,这说明维生素C具有性.
被(填“氧化”或“还原”,下同).若榨汁时加入适量的维生素C,可有效防止这种现象的发生,这说明维生素C具有性.
-
(3) 含硫的物质在生产和生活中有重要作用.
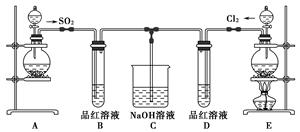
Ⅰ根据右图所示装置,回答下列问题.
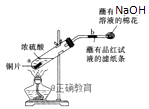
停止反应后,b处产生的现象是:;
写出a处发生反应的化学方程式:;
蘸有
 溶液的棉花的作用是:;
溶液的棉花的作用是:; -
(4) Ⅱ某化学兴趣小组选用下列装置,测定工业原料气(含
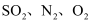 )中的
)中的  的含量.
的含量. 
若原料气的流向为从左到右,则上述装置连接的顺序是(填字母代号):原料气 →→→→→e;已知装置Ⅱ中反应为:
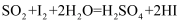 .当装置Ⅱ中出现现象时,立即停止同期.若
.当装置Ⅱ中出现现象时,立即停止同期.若 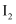 溶液的浓度为0.05
溶液的浓度为0.05 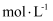 ,体积为20mL,此时收集到的
,体积为20mL,此时收集到的  与
与  的体积为297.6mL(已经折算为标准状况下的气体体积),由此可求得
的体积为297.6mL(已经折算为标准状况下的气体体积),由此可求得  的体积分数为.
的体积分数为. -
(5) 下列试剂中,可以用来代替试管中的碘的淀粉溶液的是 (填代号).A . 酸性
 溶液
B .
溶液
B .  溶液
C . 溴水
D . 氨水
溶液
C . 溴水
D . 氨水
-
(6) Ⅲ从原子利用率,减少污染等角度考虑,下列制取硫酸铜合理的方法是 (填代号)A . 铜和浓硫酸的反应 B . 铜和稀硫酸的反应 C . 氧化铜和硫酸的反应 D . 微热下,使铜屑在持续通入空气的稀硫酸中溶解
Ⅰ. (NH4)xH6-xV10O28·yH2O的制备
将NH4VO3溶于pH为4的弱酸性介质后,加入乙醇,过滤得到(NH4)xH6-xV10O28·yH2O晶体。乙醇的作用是____________________________________。
Ⅱ. (NH4)xH6-xV10O28·yH2O的组成测定
-
(1) NH4+含量测定
准确称取0.363 6 g该十钒酸铵晶体,加入蒸馏水和NaOH溶液,加热煮沸,生成的氨气用20.00 mL 0.100 0 mol·L-1盐酸标准溶液吸收。用等浓度的NaOH标准溶液滴定过量盐酸,消耗NaOH标准溶液8.00 mL。
-
(2) V10O
 (M=958 g·mol-1)含量测定
(M=958 g·mol-1)含量测定 步骤1:准确称取0.3636 g该十钒酸铵晶体,加入适量稀硫酸,微热使之溶解。
步骤2:加入蒸馏水和NaHSO3 , 充分搅拌,使V10O
 完全转化为VO2+。
完全转化为VO2+。步骤3:加适量稀硫酸酸化,加热煮沸,除去溶液中+4价硫。
步骤4:用0.020 00 mol·L-1 KMnO4标准溶液滴定,终点时消耗30.00 mL KMnO4标准溶液(该过程中钒被氧化至+5价,锰被还原至+2价)。
①写出步骤2反应的离子方程式:。
②若未进行步骤3操作,则数值y将(填“偏大”“偏小”或“无影响”)。
③通过计算确定该十钒酸铵晶体的化学式(写出计算过程)。
-
(1) 汽车排出的尾气中含有CO和NO等气体,用化学方程式解释产生NO的原因。
-
(2) 已知:N2、O2分子中化学键的键能分别是946 kJ·mol-1、497 kJ·mol-1。N2 (g)+O2 (g)=2NO (g) ΔH=+180.0 kJ·mol-1 , NO分子中化学键的键能为kJ·mol-1。
-
(3) 已知E1=134kJ·mol-1、E2=368kJ·mol-1 , 请参考题中图表,按要求填空:
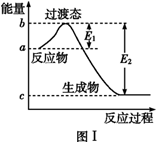
①图Ⅰ是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率加快,E1的变化是(填“增大”、“减小”或“不变”,下同),ΔH的变化是。NO2和CO反应的热化学方程式为。
②下表所示是部分化学键的键能参数:
化学键
P—P
P—O
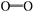
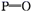
键能/(kJ·mol-1)
a
b
c
x
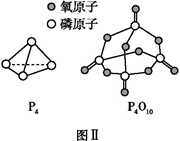
已知P4(g)+5O2(g)=P4O10(g)ΔH=-d kJ·mol-1 , P4及P4O10的结构如图Ⅱ所示。表中x=(用含a、b、c、d的代数式表示)。
-
(4) 将0.20 mol NO和0.10 mol CO充入一个容积恒定为1 L的密闭容器中,在不同条件下反应过程中部分物质的浓度变化状况如图所示。
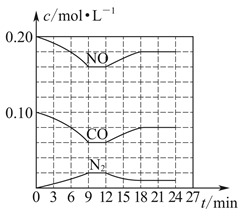
计算产物N2在6-9 min时的平均反应速率v(N2)=mol·L-1·min-1;
①反应转移的电子数目为。
②消耗硫酸的物质的量为。
③则所得气体中SO2 和 H2 的体积比约为。
 含量
C . 可直接利用超纯二氧化硅制造手机芯片
D . 淀粉溶液遇加碘食盐会直接变蓝
含量
C . 可直接利用超纯二氧化硅制造手机芯片
D . 淀粉溶液遇加碘食盐会直接变蓝
-
(1) 实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:;
-
(2) 实验室用装置E制备Cl2 , 其反应的化学方程式为MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。若有6 mol的HCl参加反应,则转移的电子总数为;
MnCl2+Cl2↑+2H2O。若有6 mol的HCl参加反应,则转移的电子总数为;
-
(3) ①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是B:,D:;
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为
B:。
D:。
 B .
B .  C .
C . 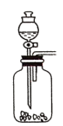 D .
D . 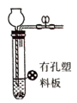
- In 1993, New York State ordered stores to charge a deposit o
- 从1820年到1830年,英国曼彻斯特、伯明翰等主要工业城市的人口增长达40%以上,是自18世纪后期以来增长最快的10年
- 近代史上,一位日本企业家在苏州开办了纺织厂。你认为此事最早可能发生在:( ) A、鸦片战争前 B、鸦片战争中
- 2008年12月4日是我国现行宪法颁布实施26周年纪念日,也是我国第八个全国法制宣传日,主题是“弘扬法治精神,服务科学发
- My parents don’t allow time nothing.A.to wa
- 王夫之是我国明末清初著名的思想家和哲学家,他在哲学上的贡献主要是总结和发展了中国传统的唯物主义。以下说法中最可能是他说的
- 下边是某同学整理的“南京条约”资料卡片。卡片中表述错误的是条约的A.签订时间 B.签订地点
- 读世界水稻种植区北界分布图,回答1~2题。 1.确定水稻种植区北界的主要依据是() A.地形 B.热量
- 做下列运动的物体,能当作质点处理的是() A.自转中的地球 B.旋转中的风力发电机叶片 C.在冰面上旋转的花样滑冰运动员
- “1947年7月—9月,解放战争形势起了一个根本的变化,即人民解放军由战略防御转入战略进攻,把战争推进取国民党统治区为
- 下列各组词语中有错别字的一组是( ) A 触目 怵目惊心 窜改 篡改历史 B 正规 走上正轨 交待 交
- 生物体内细胞没有表现出全能性,原因是( ) A. 细胞丧失了全能性 B. 基因的选择性表达 C. 基因发生了变化D
- 1840年,俄国化学家盖斯(G·H·Hess)从大量的实验事实中总结出了一条规律:化学反应不管是一步完成还是分几步完成,
- 下列重大事件按时间顺序排列正确的是① 十一届三中全会的召开 ②恢复中华人民共和国在联合国的合法地位 ③加入亚
- 阅读下面的材料,根据要求写一篇不少于800字的文章。 还在念大学的时候。雅科布·格辣与威廉·格林兄弟俩的脑子里一直萦绕着
- 细胞作为最基本的生命系统,其形态、结构、功能保持相对稳定。生命系统通过各个层次的信息和反馈调节等活动维持其自身稳定,执行
- “他们把欧洲的封建制度比作漫长的黑夜,呼唤用理性的阳光驱散现实的黑暗”。这里“他们”应该是指 A.智者学派
- 下列词语中没有错别字的一组是( ) A. 陨石 流线型 山清水秀 言者无罪,闻者足诫 B. 佩带 蒸
- 古诗文名句默写。 让我们跟着古人走进丰富多彩的诗文世界:随白居易打马春行钱塘湖,寻找“乱花渐欲迷人眼,(1)”的春意;梨
- 阅读下列材料 【材料一】 古者以天下为主,君为客。……今也以君为主,天下为客,……然则为天下之大害者,君而已矣。



