第四章 非金属及其化合物 知识点题库
下列物质的转化在给定条件下能实现的是( )
①SiO2  Na2SiO3
Na2SiO3 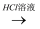 H2SiO3
H2SiO3
②Fe  Fe2O3
Fe2O3![]() Fe2(SO4)3
Fe2(SO4)3
③BaSO4![]() BaCO3
BaCO3 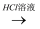 BaCl2 (Ksp(BaSO4)=1.1×10﹣10 Ksp(BaCO3)=2.6×10﹣9)
BaCl2 (Ksp(BaSO4)=1.1×10﹣10 Ksp(BaCO3)=2.6×10﹣9)
④AlCl3溶液  Al
Al  NaAlO2
NaAlO2
⑤HCHO 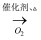 HCOOH
HCOOH  HCOOCH3 .
HCOOCH3 .
A . ①②⑤
B . ②③④
C . ②④⑤
D . ①③⑤
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
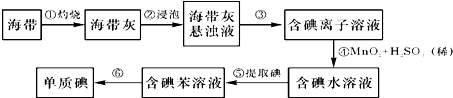
请填写下列空白:
-
(1) 从上述步骤中可知,海带中含有的碘元素的主要存在形式是.
-
(2) 步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器
是
(从下列仪器中选出所需的仪器,用标号字母填写在空白处).
A . 烧杯 B . 表面皿 C . 坩埚 D . 酒精灯 E . 干燥器 -
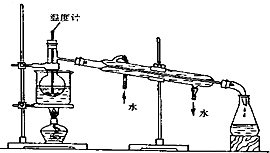
(3) 步骤⑥是从含碘苯溶液中分离出单质碘和回收苯,还需经过蒸馏,指出下列实验装置中的错误之处.
①
②
③
进行上述蒸馏操作时,使用水浴的原因是;
-
(4) 步骤④反应的离子方程式是.步骤④中的转化还可以Cl2或双氧水(H2O2),请分别写出反应的离子方程式:、.
-
(5) 检验海带中是否含有碘元素,可以在步骤④后进行,检验时可用的试剂是.
-
(6) 下列物质,不能作为从碘水中萃取碘的溶剂的是 .A . 热裂汽油 B . CCl4 C . 酒精 D . 甲苯
-
(7) 步骤③得到的溶液有时候仍是浑浊的,其通常原因是.
某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是( )
A . AlCl3
B . Na2O
C . FeCl2
D . SiO2
将少量的CO2通入下列溶液中,不能产生沉淀的是( )
A . 氯化钙溶液
B . 偏铝酸钠溶液
C . 硅酸钠溶液
D . 氢氧化钡溶液
下列说法正确的是( )
A . 为防止富脂食品氧化变质,常在包装袋中放入生石灰
B . 海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化
C . 中国的瓷器驰名世界。我们日常生活中所用到的陶瓷,主要是硅酸盐产品
D . 为缓解旱情,可以用干冰或溴化银进行人工降雨
关于NH4Cl的说法正确的是( )
A . 溶于水温度升高
B . 可作氮肥
C . 受热分解可制氨气
D . 属于共价化合物
如图所示,将SO2通入下列不同溶液中,实验现象与所得结论均正确的是( )
| 溶液 | 实验现象 | 实验结论 | | |
| A | NaOH溶液 | 无明显现象 | SO2与NaOH 溶液不反应 | |
| B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 | |
| C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 | |
| D | 紫色石蕊试液 | 溶液先变红, 后褪色 | SO2的水溶液呈酸性, 且SO2有漂白性 |
A . A
B . B
C . C
D . D
下列关于自然界中氮循环的说法错误的是( )
A . 氮肥均含有NH4+
B . 雷电作用固氮中氮元素被氧化
C . 碳、氢、氧三种元素参与了自然界中氮循环
D . 合成氨工业的产品可用于侯氏制碱法制备纯碱
利用图像,可以从不同角度研究含氯物质的性质及其转化关系,图中甲~辛均含氯元素。回答下列问题:
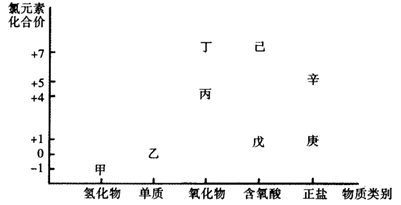
-
(1) 丙的化学式为,用途之一是;丁属于(“酸性”或”碱性”)氧化物。
-
(2) 根据氯元素的化合价判断,乙物质。
a.只有氧化性 b.既有氧化性又有还原性 c.只有还原性
-
(3) 电解甲溶液制备己的化学反应为甲+H2O
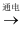 己+H2↑(未配平),配平后参与反应的甲与H2O的计量数之比是。
己+H2↑(未配平),配平后参与反应的甲与H2O的计量数之比是。
-
(4) 若庚是漂粉精的有效成分,存放不当,在空气中易失效。原因是(用化学方程式表示)。
我国在科技上不断取得重大成果,下列说法正确的是( )
A . 嫦娥五号月面五星红旗的面料“芳纶”属于合成纤维
B . 嫦娥五号登月采集的样本中含有3He,与地球上的2He 互为同素异形体
C . 我国开采的海底可燃冰是可以燃烧的水
D . 中国“奋斗者”号万米载人潜水器的钛合金材料属于新型高分子材料
下列几种气体(括号内为溶剂或反应物溶液)按如图所示装置进行实验,不能看到喷泉现象的是( )
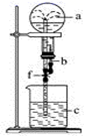
A . HCl(H2O)
B . CO2(H2O)
C . SO2(NaOH溶液)
D . NH3(KCl溶液)
下列“实验结论”与“实验操作及现象”不相符的一组是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入足量稀盐酸,无明显现象;再加入 | 原溶液中一定含有 |
| B | 某溶液中滴加 | 原溶液一定含 |
| C | 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中一定含有 |
| D | 向某溶液中加入浓 | 该溶液中一定含有 |
A . A
B . B
C . C
D . D
实验室用如图装置制取、提纯、收集Cl2、尾气处理,不能达到实验目的的是( )
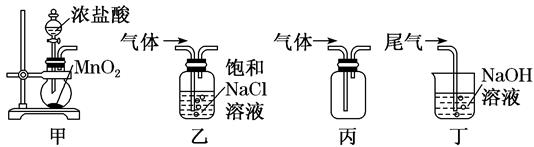
A . 用装置甲制取Cl2
B . 用装置丙收集Cl2
C . 用装置丁吸收尾气中的Cl2
D . 用装置乙除去Cl2中的少量HCl
根据下图回答问题:
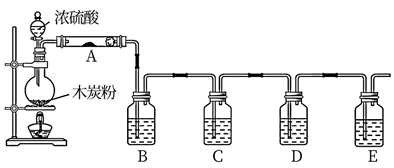
-
(1) 写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:。
-
(2) 如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中所加入试剂的名称或作用:
①A中加入的试剂是;
②C中所加的试剂的作用是。
下列实验现象与新制氯水中的某些成分(括号内物质)没有关系的是( )
A . 新制氯水显淡黄绿色(Cl2)
B . 将NaHCO3固体加入新制氯水中,有无色气泡产生(HClO)
C . 向新制氯水中滴加石蕊溶液,溶液先变红后褪色(H+、HClO)
D . 滴加AgNO3溶液有白色沉淀产生(Cl-)
近年来,我国在无机非金属材料领域的发展受到世界瞩目。下列叙述正确的是( )
A . 石墨烯是能导电的新型有机材料
B . 氮化硅陶瓷属于传统无机非金属材料
C . 陶瓷是以黏土为原料制成的
D . 二氧化硅导电性良好
研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价与物质类别关系图如下。
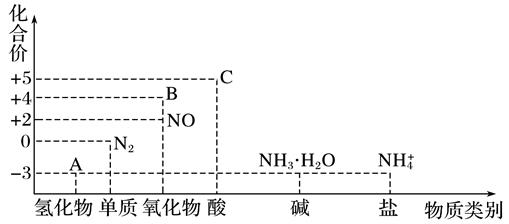
回答下列问题:
-
(1) 在催化剂和加热的条件下,物质A生成
 是工业制硝酸的重要反应,化学方程式是。
是工业制硝酸的重要反应,化学方程式是。
-
(2) 在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:。
-
(3) 实验室中,检验溶液中含有
 的操作方法是。
的操作方法是。
-
(4) 物质B为红棕色气体,写出该物质与水反应的离子方程式:,当反应消耗
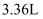 (标准状况)物质B时,转移电子的物质的量为
(标准状况)物质B时,转移电子的物质的量为 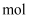 。
。
-
(5) Cu与一定浓度的硝酸溶液反应生成
 时的离子反应方程式为。
时的离子反应方程式为。
某小组探究NH3的催化氧化,实验装置图如图。③中气体颜色无明显变化,④中收集到红棕色气体,一段时间后产生白烟。
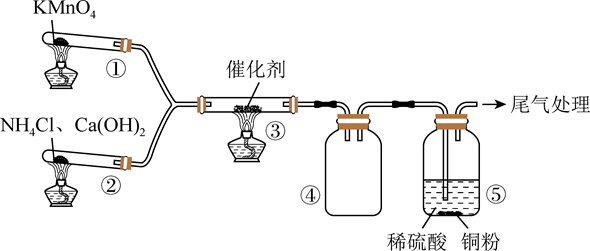
下列分析错误的是( )
A . 若②中只有NH4Cl不能制备NH3
B . ③、④中现象说明③中的反应是4NH3+5O2  4NO+6H2O
C . ④中白烟的主要成分是NH4Cl
D . 一段时间后,⑤中溶液可能变蓝
4NO+6H2O
C . ④中白烟的主要成分是NH4Cl
D . 一段时间后,⑤中溶液可能变蓝
 4NO+6H2O
C . ④中白烟的主要成分是NH4Cl
D . 一段时间后,⑤中溶液可能变蓝
4NO+6H2O
C . ④中白烟的主要成分是NH4Cl
D . 一段时间后,⑤中溶液可能变蓝
回答下列问题:
-
(1) 以Fe、CuO、H2SO4三种物质为原料,用两种方法制取铜(用化学方程式表示):
方法一:。
方法二:。
-
(2) 请写出NH4NO3的电离方程式:。
-
(3) 请写出与O2互为同素异形体的物质的化学式:
-
(4) 当光束通过下列物质时,不会出现丁达尔现象的分散系有 (填字母)。
A.氢氧化铁胶体 B.水 C.蔗糖溶液 D.氯化铁溶液 E.云、雾
在指定条件下,下列选项所示的物质间转化能实现的是( )
A . 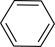

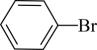 B .
B . 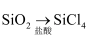 C .
C . 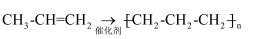 D .
D . 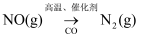

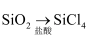 C .
C . 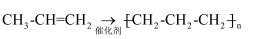 D .
D . 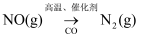
最近更新
- 阿基米德采用排水法解决了王冠掺假问题,现有一个金和银做成的王冠,用排水法测量出其体积为56.9cm3,若与王冠质量相同的
- 伊斯兰教创始人穆罕默德的诞生地在( ) A.麦地那 B.麦加 C.开罗
- 下列图象中所发生的现象与电子的跃迁无关的是()A.燃放烟花 B.霓虹灯广告 C.燃烧蜡烛 D.平面镜成像
- 14.下列说法正确的是 A.太阳辐射的能量主要来自太阳内部的核裂变反应B.汤姆生发现电子,表明原子具有核式结构C.一束光
- 以下关于细胞生命历程的说法正确的是A.细胞分裂都会出现纺锤体和遗传物质的复制B.衰老的细胞没有基因表达过程C.致癌病毒可
- 过分拔高道德典型,会出现“捧杀式”的失真;过分夸大偶然负面事件,则会出现“捧杀式”的粗暴。可见,新闻报道应当坚持
- 1.CO2是初中化学重点研究的气体之一。某化学兴趣小组设计了如下实验来探究CO2的制取和性质: (1)该兴趣小组用
- 简述恒温动物体温恒定的原因。
- 绝对值不大于3.14的所有整数的积等于.
- 2014年3月3日,全国政协十二届二次会议隆重召开,2000余位政协委员为新时期建设中的“中国梦”“改革年”“民生”等话
- 假若在一个与外界隔绝、没有食物的荒岛上,给你三只鸡(其中2只为母鸡)和40斤玉米,理论上分析,如何利用它们使你在此荒岛上
- 语言运用 指出下列各句语病的类型: (1)为充分体现志愿者的工作价值,亚运会前夕,广州亚组委志愿者部创造性地推出了“志愿
- 已知数列满足性质:对于且求的通项公式.
- 加入世界贸易组织使我国面临严峻的挑战,表现在:( ) A.民族工业将遭受灭顶之灾 B.有比较优势的产业,优势将不再存
- 我国古典名著中有许多足智多谋的人物形象,请写出其中一位及与其相关的一个故事名称。
- 李大钊在一首诗中写道:“圆明两度昆明劫,鹤化千年未忍归”“ 两度劫”发生在①鸦片战争②第二次鸦片战争③甲午战争④八国联军
- 在抗日民族统一战线旗帜下,国共两党合作抗日。八路军一一五师是在参加哪次会战中取得抗战以来首次大捷的 A.淞沪会战 B.
- 下列粒子结构示意图中,表示阳离子是( )
- 下表为人体细胞外液和细胞内液的物质组成和含量的测定数据,相关叙述错误的是A.②属于血浆,其渗透压大小主要与血浆无机盐及蛋
- 关于德国南部城市的说法,正确的是() A.德国的大城市特别发达,并分散在全国 B.德国的城市化水平高达95% C.
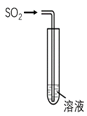
 溶液,有白色沉淀产生
溶液,有白色沉淀产生
 溶液,无明显现象;再滴加氯水,溶液呈红色
溶液,无明显现象;再滴加氯水,溶液呈红色

 溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体
溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体


