第四章 非金属及其化合物 知识点题库
近期埃博拉病毒在非洲各国肆虐,严重威胁了非洲人民的生命.在此期间,环境消毒是极其关键的,常常喷洒一种名为“84”的消毒液,其有效成分为NaClO.下列有关“84”消毒液的说法正确的是( )
A . NaClO属于共价化合物
B . “84”消毒液在空气中久置会变质
C . 1L 0.1mol∙L﹣1NaClO溶液中ClO﹣的数目为0.1NA
D . ClO﹣与Ca2+、Fe2+、Al3+ 能大量共存
下列类比分析结果正确的是( )
A . Fe3O4根据化合价规律可表示为FeO•Fe2O3 , 则Pb3O4也可表示为PbO•Pb2O3
B . CaC2能水解:CaC2+2H2O=Ca(OH)2+C2H2↑,则Al4C3也能水解:Al4C3+12H2O=4Al(OH)3↓+3CH4↑
C . Cl2与Fe加热生成FeCl3 , 则I2与Fe加热生成FeI3
D . SO2通入BaCl2溶液不产生沉淀,则SO2通入Ba(NO3)2溶液也不产生沉淀
化学在工农业生产和日常生活中都有重要应用。下列叙述正确的是( )
A . 暖贴中常有活性炭、氯化钠、水和还原铁粉等,使用时炭和铁粉发生反应放出热量
B . 糖类、油脂和蛋白质是人体必需的营养物质,故纤维素也能为人体提供营养
C . 为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
D . 《本草纲目》中“凡酸坏之酒,皆可蒸烧”所用的分离操作方法是蒸馏
下列叙述中,你认为科学的是( )
A . 某广告语:本饮料纯属天然物质,不含任何化学成分
B . 到城乡结合处燃放鞭炮,可避免污染环境
C . 在地球上分布很广,淡水资源取之不尽,用之不竭
D . 大气中二氧化碳含量的增多是造成“温室效应”的主要原因
化学与生产、生活密切相关。下列叙述错误的是( )
A . 雾霾、温室效应、光化学烟雾的形成都与氮的氧化物无关
B . 将煤汽化和液化,得到清洁的燃料和化工原料
C . 用浸泡过高锰酸钾溶液的硅藻土吸收水果中的乙烯,可实现水果保鲜
D . 光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅
工业上用洗净的废铜屑作原料来制备硝酸铜,为节约原料和防止环境污染,宜采用的方法是( )
A . Cu+HNO3(稀) 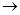 Cu(NO3)2
B . Cu+HNO3(浓)
Cu(NO3)2
B . Cu+HNO3(浓) 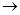 Cu(NO3)2
C . Cu
Cu(NO3)2
C . Cu 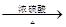 CuSO4
CuSO4 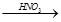 Cu(NO3)2
D . Cu
Cu(NO3)2
D . Cu 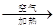 CuO
CuO 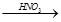 Cu(NO3)2
Cu(NO3)2
下列五种有色溶液与SO2作用,均能褪色,其实质相同的是 ( )
①品红溶液 ②KMnO4酸性溶液 ③溴水 ④滴有酚酞的NaOH溶液 ⑤淀粉碘溶液
A . ①④
B . ①②③
C . ②③⑤
D . ②③④
下列叙述正确的是( )
A . 将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2 , 产生沉淀.
B . 向FeCl3溶液中滴加氨水,产生红褐色沉淀;再加入NaHSO4溶液,沉淀消失
C . 在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解
D . 分液时,分液漏斗中下层液体从下口流出,上层液体也从下口放出
下列颜色变化与氧化还原反应无关的是 ( )
A . 湿润的红色布条遇氯气褪色
B . 棕黄色 FeCl3 饱和溶液滴入沸水中变红褐色
C . 紫色酸性 KMnO4 溶液通入乙烯气体后褪色
D . 浅黄色 Na2O2 固体露置于空气中逐渐变为白色
草酸亚铁晶体(FeC2O4·2H2O)是一种黄色难溶于水的固体,受热易分解,是生产电池、涂料以及感光材料的原材料。为探究纯净草酸亚铁晶体热分解的产物,设计装置图如图:
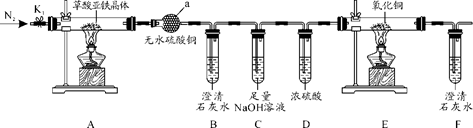
-
(1) 仪器a的名称是。
-
(2) 从绿色化学考虑,该套装置存在的明显缺陷是。
-
(3) 向盛有草酸亚铁晶体的试管中滴入硫酸酸化的KMnO4溶液,振荡,溶液变为棕黄色,同时有气体生成。已知反应中MnO
 转化为无色的Mn2+ , 则该过程中被氧化的元素是。若反应中消耗1molFeC2O4·2H2O,则参加反应的n(KMnO4)=。
转化为无色的Mn2+ , 则该过程中被氧化的元素是。若反应中消耗1molFeC2O4·2H2O,则参加反应的n(KMnO4)=。
-
(4) 草酸亚铁晶体在空气易被氧化,检验草酸亚铁晶体是否氧化变质的实验试剂是。
-
(5) 称取5.40g草酸亚铁晶体用热重法对其进行热分解,得到剩余固体质量随温度变化的曲线如图所示:
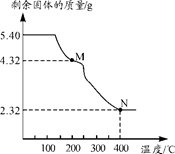
①图中M点对应物质的化学式为。
②已知400℃时,剩余固体是铁的一种氧化物,试通过计算写出该化合物与稀盐酸反应的离子方程式:。
已部分氧化的亚硫酸钠,为确定其纯度,要进行如下实验:①称取样品 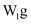 ;②将样品溶液于蒸馏水中;③给溶液加稍过量的经盐酸酸化的
;②将样品溶液于蒸馏水中;③给溶液加稍过量的经盐酸酸化的 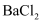 溶液;④过滤、洗涤、干燥沉淀,称其质量为
溶液;④过滤、洗涤、干燥沉淀,称其质量为  ,试回答:
,试回答:
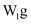 ;②将样品溶液于蒸馏水中;③给溶液加稍过量的经盐酸酸化的
;②将样品溶液于蒸馏水中;③给溶液加稍过量的经盐酸酸化的 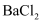 溶液;④过滤、洗涤、干燥沉淀,称其质量为
溶液;④过滤、洗涤、干燥沉淀,称其质量为  ,试回答:
,试回答:
-
(1) 怎样检查
 是否完全除去? 。
是否完全除去? 。
-
(2) 判断沉淀是否洗净的方法: 。
我国向国际社会作出“碳达峰、碳中和”的郑重承诺树立了大国形象,彰显了大国担当。下列说法错误的是( )
A . 汽车尾气催化转化器的使用可以减少温室气体的排放
B . 加大水能、风能、太阳能等一级能源的利用
C . 推动新能源汽车代替燃油车,着力降低自身碳排放水平
D . 全力推动绿色矿山绿色工厂建设,种植“碳中和林”
烟气的脱硝(除  )技术和脱硫(除
)技术和脱硫(除  )技术都是目前环境科学研究的热点。
)技术都是目前环境科学研究的热点。
 )技术和脱硫(除
)技术和脱硫(除  )技术都是目前环境科学研究的热点。
)技术都是目前环境科学研究的热点。
-
(1) 工业上可以采用“质子膜电解槽”对烟气进行脱硫脱硝,其工艺如图甲所示:
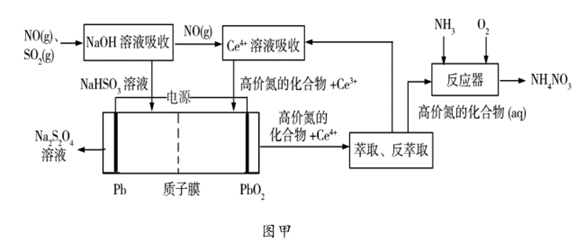
①
 溶液吸收
溶液吸收  主要反应的化学方程式为;
主要反应的化学方程式为;②电解的主要目的是,阴极的电极反应式为;
③“高价氮的化合物”中NO2在反应器中发生化合反应的化学方程式为;
-
(2) 利用活性焦炭的吸附作用,可以对烟气进行脱硫和脱硝。被吸附的
 与活性焦炭反应生成
与活性焦炭反应生成  和
和  ,当生成
,当生成 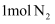 时,转移电子的物质的量为
时,转移电子的物质的量为 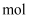 ;
;
-
(3) 一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入
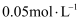 的
的 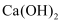 乳浊液中,发生的反应如下:
乳浊液中,发生的反应如下: 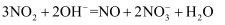 ,
, 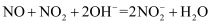 ,改变
,改变  ,
, 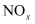 的去除率变化情况如图乙所示。
的去除率变化情况如图乙所示。 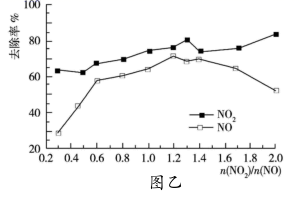
①当
 大于1.4时,
大于1.4时,  去除率升高,但
去除率升高,但  的去除率却降低。其可能的原因是;
的去除率却降低。其可能的原因是;②
 和
和  发生的主要反应为
发生的主要反应为  。保持
。保持  的初始浓度不变,改变
的初始浓度不变,改变  ,将反应后的混合气体通入
,将反应后的混合气体通入  乳浊液中吸收。为节省
乳浊液中吸收。为节省  的用量,又能保持
的用量,又能保持  去除效果,则
去除效果,则  合适的值约为;
合适的值约为; -
(4) 已知:
 ,
, 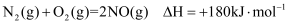 ,则
,则  。
。
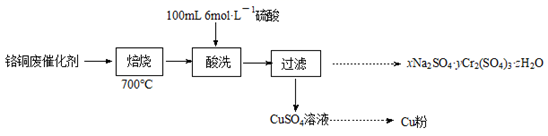
从铬铜废催化剂(主要含CuO·Cr2O3、少量有机物及水)中回收铬和铜的实验流程如下:
-
(1) 700℃“焙烧”可使Cr2O3不溶于酸,焙烧的另一目的是。
-
(2) 配制“酸洗”所用100mL6mol·L-1硫酸需要的玻璃仪器有:量筒、烧杯、100mL容量瓶、和;为使研碎的烧渣中CuO充分溶解,应采取的措施是。
-
(3) 为确定xNa2SO4·yCr2(SO4)3·zH2O的组成,进行下列实验:①称取样品1.9320g溶于水,加入足量盐酸酸化的BaCl2溶液,得到1.8640g沉淀。②另称取样品1.9320g溶于水,经H2O2在碱性条件下氧化、煮沸、酸化得Na2Cr2O7和Na2SO4的混合酸性溶液;加入稍过量的KI溶液(Cr2O
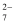 +6I-+14H+ = 2Cr3++3I2+7H2O),暗处静置5min,立刻用0.5000mol·L-1Na2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至溶液呈浅黄色,再加入1mL淀粉溶液,继续滴定至溶液蓝色刚好消失,消耗Na2S2O3溶液24.00mL。
+6I-+14H+ = 2Cr3++3I2+7H2O),暗处静置5min,立刻用0.5000mol·L-1Na2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至溶液呈浅黄色,再加入1mL淀粉溶液,继续滴定至溶液蓝色刚好消失,消耗Na2S2O3溶液24.00mL。 根据上述实验数据,确定xNa2SO4·yCr2(SO4)3·zH2O的化学式(写出计算过程)。
-
(4) 已知反应2[Cu(NH3)4]2+ + N2H4·H2O +4OH-= 2Cu↓+ N2↑+ 8NH3 + 5H2O。请补充完整由CuSO4溶液制备纯净铜粉的实验方案:,干燥得铜粉(实验中须使用的试剂有:12 mol·L-1氨水、2 mol·L-1 N2H4·H2O溶液)。
下列说法错误的是( )
A . 铅蓄电池的工作原理为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,铅蓄电池在放电过程中,负极质量增加,正极质量也增加
B . 金属铝的一种冶炼流程为:  C . 铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀,但加热反应剧烈
D . 等物质的量的稀硝酸与浓硝酸参与氧化还原反应时,稀硝酸转移电子数目多,所以稀硝酸的氧化性更强
C . 铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀,但加热反应剧烈
D . 等物质的量的稀硝酸与浓硝酸参与氧化还原反应时,稀硝酸转移电子数目多,所以稀硝酸的氧化性更强
我国自主研制的臭氧总量探测仪能对雾霾进行监测.下列有关臭氧的说法正确的是( )
A . 臭氧的摩尔质量是48g
B . 同温同压条件下,等质量的氧气和臭氧体积比为2:3
C . 氧气和臭氧互为同素异形体
D . 1.0mol臭氧中含有电子总数为18×6.02×1023
下列转化不能一步实现的是( )
A .  B .
B . 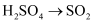 C .
C . 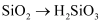 D .
D . 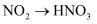
 B .
B . 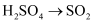 C .
C . 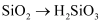 D .
D . 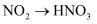
下列有关实验的说法错误的是( )
A . 中学实验室中可以将未用完的钠放回原试剂瓶
B . 纯净的氢气在氯气中安静燃烧,发出苍白色火焰
C . 干燥的氯气可以使有色鲜花变色,说明干燥的氯气有漂白性
D . 配置480m10.1mol/L硫酸铜溶液时,需要用到500ml容量瓶
在实验室中,用如图所示装置(尾气处理装置略去)进行下列实验,将①中液体逐滴滴入②中,则预测的现象正确的是( )
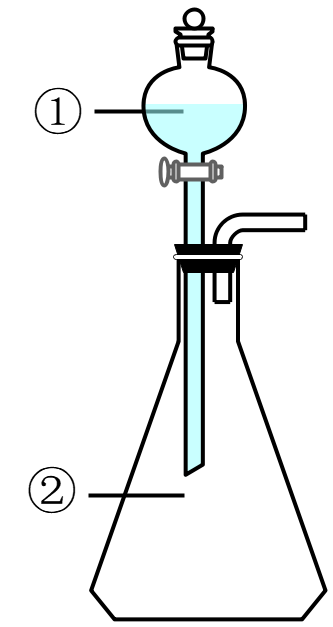
选项 | ①中的物质 | ②中的物质 | 预测②中的现象 |
A | 氯水 | 石蕊溶液 | 溶液变成红色 |
B | 双氧水 | 二氧化锰 | 无明显现象 |
C | 稀硫酸 | 碳酸钠溶液 | 开始没有气泡,一段时间后才产生气泡 |
D | 浓盐酸 | 二氧化锰 | 立即产生黄绿色气体 |
A . A
B . B
C . C
D . D
海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
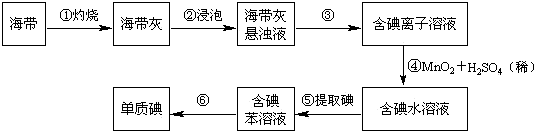
请填写下列空白:
-
(1) 步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是____;(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。A . 烧杯 B . 坩埚 C . 表面皿 D . 泥三角 E . 酒精灯 F . 干燥器
-
(2) 步骤③的实验操作名称是;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是。
-
(3) 步骤⑤中,某学生选择用苯来提取碘的理由是
-
(4) 请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
最近更新
- 21.依次填入下面一段文字横线处的语句,衔接最恰当的一组是( ) 当下,有人觉得反腐太严,感叹“官不聊生”。有这些想法
- .仔细观察下面的中国古代史年代尺,图中符号所代表的朝代应该是A.①南宋②辽③元 B.①唐②元
- 4.《资治通鉴》载:高宗初即位,欲更立武昭仪为后,犹豫未决,直恐宰臣异议耳。唐高宗所顾忌的宰臣,最主要的是 A.三公九卿
- 新疆有一座晚清名臣的祠堂,悬挂一副楹联:“提挈自东西,十年戎马书生老;指挥定中外,万里寒鸦相国寺。”它颂扬的是() A.
- 42.原本无色的物质在酶Ⅰ、酶Ⅱ和酶Ⅲ的催化作用下,转变为黑色素,即:无色物质→ X物质→Y物质→黑色素。已知编码酶Ⅰ、
- _____to train his daughter in English, he put an ad like thi
- NO PLANS FOR THE HOLIDAYS? Special StoryTi
- 下列气体在同温度、同压强、同质量时,体积最小的是 A.CO2 B.CO C.CH4
- 秦、隋是两个短命王朝分别为汉唐盛世奠定了基础,它们共同的历史贡献是 A.制定了有利于巩固统一的制度和政策 B.开辟了沟通
- 下列属于物质化学性质的是 A.还原性 B.导电性 C.导热性 D.
- (2011•杭州)人体注射葡萄糖溶液可以补充能量,葡萄糖(C6H12O6)在体内经缓慢氧化生成二氧化碳和水,释放出能量.
- 某公司需在一个月(31天)内完成新建办公楼装修工程.如果由甲、乙两队合做,12天可以完成;如果由甲、乙两队单独做,甲队单
- 下列说法不一定成立的是( ) A. 若a>b,则a+c>b+c B.若a+c>
- 在生产实际中,有些高压直流电路中含有自感系数很大的线圈,当电路中的开关S由闭合到断开时,线圈会产生很高的自感电动势,使开
- 现有以下十种物质:① 稀盐酸、 ② 氨水、 ③ 空气、 ④CaCO 3 、⑤ 食盐水、 ⑥ 石墨、 ⑦Al 、 ⑧Ba(
- (2014·盐城二模)读大陆西岸四地气压带和风带影响时长示意图,回答1~2题。1.四地中气候类型可能相同的是() A.
- 环境人口容量的变化由大到小排列,正确的是 A.原始社会—农业时期—现代社会—工业时期 B.原始社会—农业时期—工业时
- 如图所示,将一把钢尺压在桌面上,一部分伸出桌面,用手拨动其伸出桌外的一端,轻拨与重拨钢尺,使钢尺振动的 不同,则
- The Blacks usuallyhave milk and bread breakfast. A.for
- =......



