第二节 几种重要的金属化合物 知识点题库
A是一种常见的单质,B,C为中学学习的常见化合物,A,B,C均含有元素X。它们有如下转化关系(部分产物及反应条件已略去):下列判断正确的是( )
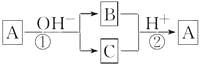
A . X元素可能为Al
B . X元素可能是金属,也可能是非金属
C . 反应①和②互为可逆反应
D . 反应①和②一定为氧化还原反应
日常生活中常用铝制炊具,它质轻且坚固耐用,其中的原因是( )
A . 铝很不活泼,不易与其他物质反应
B . 铝虽然很活泼,但是只有在高温下才能与其他物质反应
C . 铝制品表面有一层致密的氧化物薄膜,起保护作用
D . 铝制品表面镀有一层铜,可以保护铝制品
为了检验某浅黄色FeCl3溶液中是否含有Fe2+ , 下列实验方案正确的是( )
A . 滴入KSCN溶液,观察溶液是否变为血红色
B . 滴入KMnO4溶液,观察紫红色是否褪去
C . 滴入NaOH溶液,观察是否出现白色沉淀
D . 加入铁钉,观察溶液是否变为浅绿色
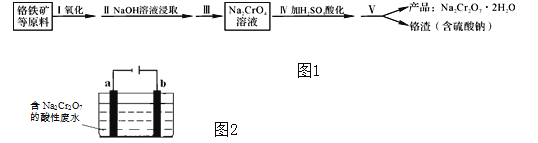
重铬酸钠(Na2Cr2O7•2H2O)是重要的化工原料,在化学工业和制药工业中常用作氧化剂.可用一种铬铁矿(主要成分:FeO•Cr2O3 , 还含有少量的Al2O3)通过以下流程来制取重铬酸钠如图1.
-
(1) 写出Cr元素基态原子的外围电子排布式
-
(2) 步骤I中反应的化学方程式为:4FeO•Cr2O3(s)+8Na2CO3(s)+7O2(g)═8Na2CrO4(s)+2Fe2O3(s)+8CO2(g),反应中被氧化的元素是 ,生成2mol Fe2O3时转移电子的物质的量为 mol.
-
(3) 步骤II中加入NaOH溶液时发生的化学反应方程式为
-
(4) +3、+6价铬都有很强的毒性,+6价铬的毒性更高,可诱发肺癌和鼻咽癌.工业上常用电解法来处理含Cr2O72﹣的废水,电解装置模拟示意图如图2(电极材料为铁和石墨).通电后,Cr2O72﹣在b极附近转变为Cr3+ , 一段时间后Cr3+最终可在a极附近变成Cr(OH)3沉淀而被除去.a电极的电极材料是 ,b电极附近生成Cr3+的反应的离子方程式是
-
(5) 将含Cr2O3为50%的铬铁矿30.4kg,按上述流程制取产品Na2Cr2O7•2H2O,假设整个流程中铬元素的利用率为80%,则最终能制得Na2Cr2O7•2H2O kg.
下列反应中,不能产生氢气的是( )
A . 红热的铁与水蒸气
B . 钠与水
C . 铝和NaOH溶液反应
D . 铁与稀硝酸反应
下列说法中不正确的是( )
A . 体积相同、c(Na+)相等的纯碱溶液与小苏打溶液,分别与足量同种盐酸反应,消耗盐酸的体积相等
B . 将铜粉加入氯化铁溶液,充分反应后,若固体有剩余,则该固体不可能含铁
C . 用AlCl3溶液制取Al(OH)3 , 沉淀剂选用氨水比选用NaOH溶液好
D . 相同质量的钠、镁、铝分别与足量的稀硫酸反应,生成气体的质量之比为27:24:23
根据下列框图分析,下列说法正确的是( )
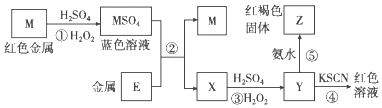
A . E2+的氧化性比M2+的氧化性强
B . 在③反应中加稀硫酸可抑制Fe2+的水解
C . 反应④的离子方程式可表示为:E3++3SCN﹣⇌E(SCN)3↓
D . 在反应①中只能用浓硫酸,既表现了酸性、又表现了氧化性
将一固体粉末含有SiO2、Fe2O3、Al2O3 , 加入足量NaOH溶液充分反应后,过滤,向所得溶液中加入过量盐酸,过滤,将所得滤渣洗涤并灼烧至恒重,最终固体成分为( )
A . SiO2
B . Fe2O3、SiO2
C . SiO2、Al2O3
D . Fe2O3
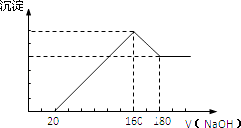
将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)求:
-
(1) 加入NaOH溶液0﹣﹣20mL过程中反应方程式为:.160﹣﹣180mL过程中反应方程式为.
-
(2) 合金中Mg的质量为g.所用HCl的物质的量浓度为mol/L.
下列物质中既能跟稀盐酸反应,又能跟氢氧化钠溶液反应的是( )
① 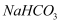 ②
②  ③
③ 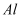 ④
④ 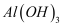 ⑤MgO ⑤Fe(OH) 3 ⑥CuSO4
⑤MgO ⑤Fe(OH) 3 ⑥CuSO4
A . 全部
B . ②③④⑤
C . ①②③④
D . ①②③④⑥
“脚印”、“笑脸”、“五环”等焰火让北京奥运会开幕式更加辉煌壮观,这些五彩缤纷的焰火与元素的焰色反应有关,下列说法不正确的是()
A . 用洁净的铂丝蘸取少量待测液在酒精灯火焰上灼烧并观察焰色
B . 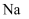 与
与  在灼烧时火焰颜色相同
C . 焰色反应一定发生化学变化
D . 可以用焰色反应来鉴别
在灼烧时火焰颜色相同
C . 焰色反应一定发生化学变化
D . 可以用焰色反应来鉴别  和
和 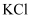
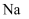 与
与  在灼烧时火焰颜色相同
C . 焰色反应一定发生化学变化
D . 可以用焰色反应来鉴别
在灼烧时火焰颜色相同
C . 焰色反应一定发生化学变化
D . 可以用焰色反应来鉴别  和
和 
X常温下为气体,a、b、c是中学化学常见物质,均由常见元素组成,转化关系(反应条件略去)如图所示, 下列说法错误的是( )
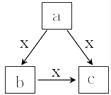
A . 若 b 为固态非金属单质,b 与 X 所含元素同主族,则c也能与 X 反应
B . 若 X 为 O2 , a 为一种固态单质,则c可能为CO2或 SO3
C . 若 a、b、c 焰色反应均呈黄色,水溶液均呈碱性,则a中可能既含有离子键又含有共价键
D . 若 b 为气态非金属单质,b 与 X 所含元素同周期,则 X 与 b 所含元素原子的核电荷数相差1
某同学分别向FeCl3溶液加入以下试剂验证Fe3+的性质,其中不能达到目的的是( )
A . KSCN溶液
B . AgNO3溶液
C . NaOH溶液
D . 铁钉
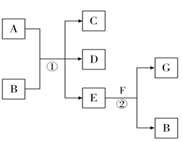
图中,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请根据图示回答下列问题:
-
(1) 写出反应①的离子方程式:。
-
(2) 写出反应②的化学方程式:。
-
(3) 实验室制取A的离子反应方程式为。A可以制漂白粉,漂白粉在空气时间长了会失效,失效的原因是(用化学方程式表示)。
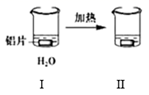
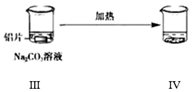
探究铝片与  溶液的反应。
溶液的反应。
 溶液的反应。
溶液的反应。 | | | |
| 无明显现象 | 铝片表面产生细小气泡 | 出现白色浑浊,产生大量气泡(经检验主要为 |
下列说法错误的是( )
A .  溶液中存在水解平衡:
溶液中存在水解平衡: 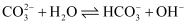 B . 对比Ⅰ、Ⅲ,说明
B . 对比Ⅰ、Ⅲ,说明  溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为:
溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为: 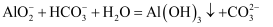 D . 加热及
D . 加热及  逸出对
逸出对  水解平衡移动方向的影响是相反的
水解平衡移动方向的影响是相反的
 溶液中存在水解平衡:
溶液中存在水解平衡: 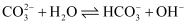 B . 对比Ⅰ、Ⅲ,说明
B . 对比Ⅰ、Ⅲ,说明  溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为:
溶液能破坏铝表面的保护膜
C . 推测出现折色浑浊的可能原因为: 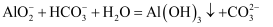 D . 加热及
D . 加热及  逸出对
逸出对  水解平衡移动方向的影响是相反的
水解平衡移动方向的影响是相反的
某酸性工业废水中含有一定量的  、
、  、
、  等离子。利用常用的酸、碱和工业生产中的废铁屑,设计如下工艺流程,从废水中回收金,并生产一定量的铁红和氧化铜。
等离子。利用常用的酸、碱和工业生产中的废铁屑,设计如下工艺流程,从废水中回收金,并生产一定量的铁红和氧化铜。
 、
、  、
、  等离子。利用常用的酸、碱和工业生产中的废铁屑,设计如下工艺流程,从废水中回收金,并生产一定量的铁红和氧化铜。
等离子。利用常用的酸、碱和工业生产中的废铁屑,设计如下工艺流程,从废水中回收金,并生产一定量的铁红和氧化铜。 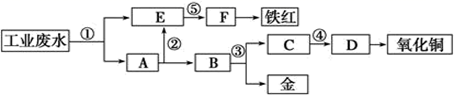
下列说法错误的是( )
A . 标号①②③处发生的反应均为氧化还原反应
B . 标号③处加入的相应物质是稀硝酸或稀硫酸
C . 标号①处发生的离子反应最多有四个
D . 铁红的化学式为  ,工业上常用作红色颜料
,工业上常用作红色颜料
 ,工业上常用作红色颜料
,工业上常用作红色颜料
三星堆两次考古挖掘举世震惊,二号祭祀坑出土商代的铜人铜像填补了我国考古学、青铜文化、青铜艺术史上的诸多空白。下列有关说法错误的是( )

A . 铜像表面的铜绿[  ]能在空气中稳定存在
B . 测定出土文物年代的
]能在空气中稳定存在
B . 测定出土文物年代的  是碳的一种同素异形体
C . X射线衍射法可对青铜器微观晶体结构进行分析
D . 青铜器的出土表明我国商代已经掌握冶炼铜技术
是碳的一种同素异形体
C . X射线衍射法可对青铜器微观晶体结构进行分析
D . 青铜器的出土表明我国商代已经掌握冶炼铜技术
 ]能在空气中稳定存在
B . 测定出土文物年代的
]能在空气中稳定存在
B . 测定出土文物年代的  是碳的一种同素异形体
C . X射线衍射法可对青铜器微观晶体结构进行分析
D . 青铜器的出土表明我国商代已经掌握冶炼铜技术
是碳的一种同素异形体
C . X射线衍射法可对青铜器微观晶体结构进行分析
D . 青铜器的出土表明我国商代已经掌握冶炼铜技术
下列关于铝的叙述错误的是( )
A . 铝是地壳中含量最多的金属元素
B . 在化学反应中,铝容易失去电子,是氧化剂
C . 在常温下,铝能与NaOH溶液反应
D . 铝是一种比较活泼的金属
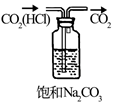
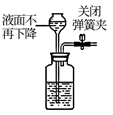
下列实验内容(装置操作或现象能达到相应实验目的的是( )
| 选项 | A | B | C | D |
| 实验目的 | 除去CO2中的HCl | 证明下列装置气密性良好 | 比较Na2CO3和NaHCO3的热稳定性 | 配置100mL 0.1mol/LNaCl溶液 |
| 实验内容 | | | | |
A . A
B . B
C . C
D . D
在指定条件下,下列选项所示的物质间转化不能实现的是( )
A . 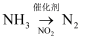 B .
B .  C .
C .  D .
D . 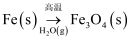
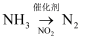 B .
B .  C .
C .  D .
D . 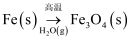
最近更新
- 伯牙善鼓琴 伯牙善鼓琴,钟子期善听。伯牙鼓琴,志在高山。钟子期曰:“善哉?峨峨兮若泰山!”志在流水,钟子期曰:“善哉,洋
- 2010年2月28日,重庆市召开“打黑除恶”专项斗争阶段总结大会。截至目前,全市共抓获涉黑涉恶人员3348人,立案查办涉
- FeS2的结构类似于Na2O2,是一种过硫化物,与稀硫酸反应生成H2S2。H2S2类似于H2O2,易发生分解:H2S2H
- 下列词语没有错别字的一项是()A.黄晕 静谧 翻来复去 波光粼粼B.取决 憔悴 咄咄逼人 披蓑带笠C.发髻 宽敞 喜出忘
- 用如图所示装置,可由乙二醛制备乙二酸,反应原理为。下列说法正确的是 A. 该装置利用上述反应将化学能转化为电能 B.
- 下列关于弹力说法中正确的是 ( )A.只要两个物体接触就一定有弹力产生B.只有接触并发生弹性形变的物体之间才会
- “二一九法令”规定土地属于( ) A.国家 B.地主 C.农民
- It has been decided that this company has the _____ right to
- When we arrived the cinema, the movie ____________ for 20 mi
- 设,则sinβ的值为( ) A. B. C. D.
- 已知椭圆的一个焦点为,则椭圆的长轴长是( ) A. B. C. D.
- --What’s your best friendlike? --- . A.
- 将一定量的NaOH和NaHCO3的混合物X放在密闭容器中加热,充分反应后生成V1 L 气体Z(V1≠0)。反应后的固体残
- 在下列溶液中,各组离子一定能够大量共存的是( ) A. 25℃由水电离的c(H+)=10-12mol/L 的溶液:F
- 下列现象中,通过做功改变物体内能的是 A将烧红的铁块投放到冷水中,水温升高 B古人钻木取火过程中,木头的温度升高
- 用右图装置电解水,一段时间后的现象如图所示。对该实验的描述错误的是( )A.甲试管中收集到的是一种可燃性气体 B.该实
- 最近一段时间,就中学阶段是否进行文理分科问题,相关媒体讨论得可谓热火朝天。全国政协委员原中国科技大学校长朱清时认为,高考
- 下列图像中,能正确描述液体压强与深度关系的是
- 古诗文默写。(共8分) (1) ,浅草才能没马蹄。(白居易《钱塘湖春行》)
- 在pH=13的无色透明溶液中,能大量共存的离子组为() A.HCO、Al3+、Na+、SO B.I-、NO、K+、NH