第二节 几种重要的金属化合物 知识点题库
有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、KCl等混合而成,为检验它们,做了如下实验:
①将固体混合物溶于水,搅拌后得无色透明溶液;
②往此溶液中滴加BaCl2溶液,有白色沉淀生成;
③过滤,将沉淀物置于足量稀硝酸中,发现沉淀全部溶解.
试判断:
-
(1) 固体混合物中肯定有,肯定没有,可能有.
-
(2) 写出实验③中的离子方程式:.
-
(3) 对可能有的物质进行确认,把③的滤液做进一步鉴别操作,写出你所设计的实验方案(包括具体操作步骤和实验现象).
火药是中国的“四大”发明,由KNO3和两种非金属元素A和B的单质组成,A为黑色固体,B为淡黄色的固体,则下列有关说法中不正确的是( )
A . 元素A与N和O同周期,B与O同主族
B . A,B分别与O组成的化合物AO和BO2均是大气的污染物
C . A和B分别与O组成的化合物均能与烧碱反应
D . 单质A在一定条件下可与B的最高价氧化物的水化物发生反应
给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
A . 粗硅  SiCl4
SiCl4  Si
B . Mg(OH)2
Si
B . Mg(OH)2  MgCl2(aq)
MgCl2(aq)  Mg
C . Fe2O3
Mg
C . Fe2O3  FeCl3(aq)
FeCl3(aq)  无水FeCl3
D . AgNO3(aq)
无水FeCl3
D . AgNO3(aq) 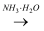 [Ag(NH3)2]OH(aq)
[Ag(NH3)2]OH(aq)  Ag
Ag
 SiCl4
SiCl4  Si
B . Mg(OH)2
Si
B . Mg(OH)2  MgCl2(aq)
MgCl2(aq)  Mg
C . Fe2O3
Mg
C . Fe2O3  FeCl3(aq)
FeCl3(aq)  无水FeCl3
D . AgNO3(aq)
无水FeCl3
D . AgNO3(aq) 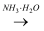 [Ag(NH3)2]OH(aq)
[Ag(NH3)2]OH(aq)  Ag
Ag
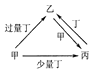
甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们在一定条件下的转化关系如图所示(部分产物已略去),下列各组物质中符合图示关系转化的是( )
选项 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
A |
| AgNO3(aq) | AgOH(s) | Ag(NH3)2OH(aq) | NH3▪H2O(aq) |
B | S(s) | SO3(g) | SO2(g) | O2(g) | |
C | NaOH(aq) | NaHCO3(aq) | Na2CO3(aq) | CO2(g) | |
D | Fe(s) | Fe(NO3)2(aq) | Fe(NO3)3(aq) | HNO3(aq) |
A . A
B . B
C . C
D . D
下列各项操作中,发生“先产生沉淀,然后沉淀又完全溶解”现象的是( )
A . 向硫酸铝溶液中逐滴加入过量氢氧化钠溶液
B . 向氯化铁溶液中逐滴加入过量氨水
C . 向硅酸钠溶液中逐滴加入过量稀盐酸
D . 向氢氧化钙溶液中缓缓通入过量二氧化碳
下列有关NaClO和NaCl混合溶液的叙述正确的是( )
A . 该溶液中,H+、NH4+、Ag+可以大量共存
B . 向该溶液中通入CO2 , 不发生化学反应
C . 该溶液可作游泳池及环境的消毒剂,有效成分是NaCl
D . 常温下,将氯气通入NaOH溶液中可以得到该溶液
随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是( )
A . 无水硫酸铜、蔗糖
B . 食盐、硫酸亚铁
C . 生石灰、硫酸亚铁
D . 硅胶、食盐
A、B、C、D是初中化学常见的物质,在一定条件下四种物质存在如下所示的转化关系:A + B → C + D。
-
(1) 若A是硫酸,B是氢氧化钠,该反应的基本类型是反应。
-
(2) 若A、C均是含同种元素的非金属氧化物,且A有毒性,D能被磁铁吸引。则C的化学式是;D的合金可用于制作炊具,主要是利用它的性。
-
(3) 若A、C是都是金属单质,B、D都是盐,该反应说明金属活动性:A(选填“<”或“>”)C。
过氧化钠能与水发生反应:2Na2O2+2H2O=4NaOH+O2↑,该反应也可用于实验室制取氧气。某同学用该反应制取标准状况下1.12L氧气。
-
(1) 计算至少需要称取过氧化钠的质量。
-
(2) 若反应所得氢氧化钠溶液的体积是200mL,计算该溶液中溶质的物质的浓度。
下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
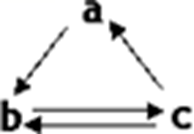
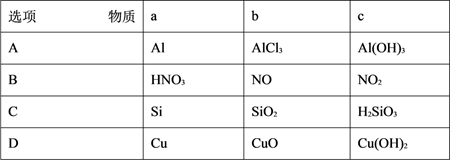
A . A
B . B
C . C
D . D
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 硝酸将Fe2+氧化为Fe3+ |
| B | 将铜粉加入1.0mol/LFe2(SO4)3溶液中 | 溶液变蓝,有黑色固体出现 | 金属铁比铜活泼 |
| C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| D | 将0.1mol/LMgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol/LCuSO4溶液 | 先有白色沉淀生成,后变为浅蓝色沉淀 | Cu(OH)2的溶度积比Mg(OH)2的小 |
A . A
B . B
C . C
D . D
研究光盘金属层含有的Ag(其它金属微量忽略不计)、丢弃电池中的Ag2O等废旧资源的回收利用意义重大。下图为从光盘中提取Ag的工业流程,请回答下列问题。
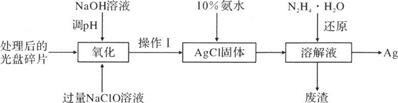
-
(1) NaClO溶液在受热或酸性条件下易分解,“氧化”阶段需在80℃条件下进行,适宜的加热方式为 。
-
(2) NaClO溶液与Ag反应的产物为AgCl、NaOH和O2 , 该反应的化学方程式为。有人提出以HNO3代替NaClO氧化Ag,从反应产物的角度分析,其缺点是。
-
(3) 操作Ⅰ的名称为。化学上常用10%的氨水溶解AgCl固体,AgCl与NH3·H2O按1:2反应可生成Cl-和一种阳离子的溶液(填阳离子的化学式)。实际反应中,即使氨水过量也不能将AgCl固体全部溶解,可能的原因是。
-
(4) 常温时N2H4·H2O(水合肼)在碱性条件下能还原(3)中生成的阳离子,自身转化为无害气体N2 , 理论上消耗0.1 mol的水合肼可提取到 g的单质Ag。
-
(5) 废旧电池中Ag2O能将有毒气体甲醛(HCHO)氧化成CO2 , 科学家据此原理将上述过程设计为原电池回收电极材料Ag并有效去除毒气甲醛。则此电池的正极反应式为 ,负极的产物有。
化学与生活密切相关,下列有关说法正确的是( )
A . 含碳量越低,钢铁的性能越好
B . 光导纤维被称为信息高速公路的骨架,其主要成分是二氧化硅
C . 燃放烟花呈现出多种颜色是由于烟花中添加了Na、Cu、Fe、Pt等金属的单质
D . 合金材料的组成元素一定全部是金属元素
下列说法正确的是( )
A . 洗涤油污常用热的碳酸钠溶液
B . 用NaOH溶液调节pH除去NH4Cl溶液中的FeCl3杂质
C . 将CuCl2溶液加热蒸干、灼烧后,所得固体为Cu(OH)2
D . 配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度
A~E为中学化学常见纯净物,其中A可用于焙制糕点,B是生活中常用的一种调味品,也是重要的化工原料。D、E均为气体,F的水溶液是一种强酸。它们之间的转化关系如下。(部分反应物、生成物已略去)
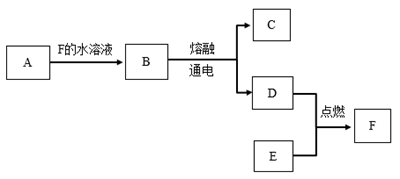
请回答下列问题:
-
(1) 写出下列物质的化学式:A,B,C。
-
(2) A→B的离子方程式是。
-
(3) D与E反应的化学方程式是,反应现象是。
甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成有关问题的解答。
-
(1) 甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有3.2g铜。
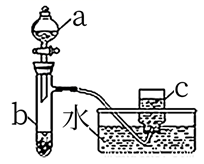
①请写出铜与稀硝酸反应的离子反应方程式:。
②在铜与硝酸的反应中,硝酸所表现出的化学性质主要有。
③若a中液体为浓硝酸,则仪器c中收集的气体主要是(填化学式)。
④待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,生成沉淀的质量是g。
-
(2) 乙组同学对铁与稀硝酸的反应进行探究。他们用amolFe和含有bmolHNO3的稀硝酸进行实验,若两种物质恰好反应都无剩余,且HNO3只被还原成NO,反应结束后溶液中含有Fe3+和Fe2+。
①反应结束后溶液中NO
 的物质的量的取值范围是(用含a的代数式表示)。
的物质的量的取值范围是(用含a的代数式表示)。②若反应结束后的溶液中Fe3+、Fe2+的物质的量之比[n(Fe3+):n(Fe2+)]为3:1,则b:a的值为。
用下列装置进行实验,能达到实验目的的是( )
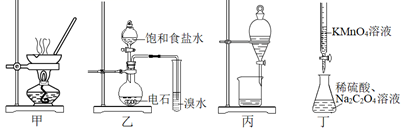
A . 用装置甲制备NaHCO3晶体
B . 用装置乙证明乙炔可使溴水褪色
C . 用装置丙分离苯和溴苯
D . 用装置丁测定KMnO4溶液的物质的量浓度
化学与生活是紧密相联的,下列说法中错误的是( )
A . 用过氧化钠作潜水艇的供氧剂
B . 将少量食醋加入“84”消毒液中,会增强其杀菌消毒效果
C . 小苏打(  )用于制作糕点
D . 地震灾区和洪涝灾区都用漂白粉消毒,主要是利用漂白粉溶液的碱性
)用于制作糕点
D . 地震灾区和洪涝灾区都用漂白粉消毒,主要是利用漂白粉溶液的碱性
 )用于制作糕点
D . 地震灾区和洪涝灾区都用漂白粉消毒,主要是利用漂白粉溶液的碱性
)用于制作糕点
D . 地震灾区和洪涝灾区都用漂白粉消毒,主要是利用漂白粉溶液的碱性
在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A .  B .
B . 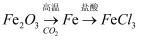 C .
C .  D .
D . 
 B .
B . 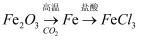 C .
C .  D .
D . 
“劳动创造幸福,实干成就伟业”。下列劳动项目所涉及的化学知识错误的是( )
选项 | 劳动项目 | 化学知识 |
A | AgBr用来制作照相胶片 | AgBr见光易分解 |
B | NaCl的溶解度随温度变化不大 | 在盐田中晾晒海水,得到粗盐 |
C | 利用含小苏打的发酵粉烘焙蛋糕 | 小苏打是碳酸氢钠 |
D | SiO2制作光导纤维 | SiO2导电 |
A . A
B . B
C . C
D . D
最近更新
- 下列词语中没有错别字的一组是(2分) ( )A.蹋败 和蔼
- 陈旭麓先生曾说过,“中国不是自己走出中世纪,而是被轰出中世纪的”。下列说法错误的是
- 存在于盐湖和热泉中的两类细菌都具有的特征是A. 在极端环境下进行遗传物质的复制B. 对利福平敏感C. 在极端环境下都不进
- 关于欧洲地形的叙述,正确的是 ( ) A、地势低平,以平原为主
- 用某种单色光照射某种金属表面,发生光电效应,现将该单色光的光强减弱,则 ( ) A.光电子的最大初动能不变
- .观察下列图形中的棋子:(1)按照这样的规律摆下去,第4个图形中的棋子个数是多少?(2)用含的代数式表示第个图形的棋子个
- 古代朴素唯物主义物质观的不足之处主要在于 A.把自然科学的物质概念等同于哲学的物质概念 B.把物质的具体形态等同于物
- 下列各句中,标点符号使用正确的一句是( ) A.她认真地看过这些信后,郑重地转给了有关部门,不知道有关部门收到这些信后作
- (05天津卷)(18分)(1)限制性内切酶Ⅰ的识别序列和切点是―G↓GATCC―,限制性内切酶Ⅱ的识别序列和切点是―↓G
- 温家宝总理在2009年《政府工作报告》中指出,做好今年的政府工作,必须坚持扩大内需、保增长的原则,充分发挥内需特别是消费
- 化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量。已知白磷和P4
- 下列叙述中,表示气候的是 A、四季如春 B、狂风暴雨 C、阴雨绵绵 D、电闪雷鸣
- 【美德:光盘行动】此“光盘”非彼“光盘”。 下面是博约同学制作的展板内容,请按要求答题。(4分) 2013年,一个热词口
- 采用小流域为单元的生态模型试验,可以检验黄土高原小流域综合治理水土流失的合理性。下表为降水量在60mm/30分钟时,“不
- 下列过程中,只发生物理变化的是()A.湿法炼铜 B.雕琢玉石 C.制造轮胎 D.葡萄酿酒
- 右图为NaCl、KNO3的溶解度曲线,下列说法正确的是A.KNO3的溶解度一定大于NaCl溶解度B.20℃时,50g水最
- 某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀硝酸,沉淀不溶解,则该溶液中A、一定有SO42- B、可能有S
- 几年前,王先生投资10万元开了一家服装店,以经营新奇服装为主,受到了很多年轻消费者的欢迎。经过几年的发展后,现在的王先生
- 53. I’m afraid I can’t keep _______ my classmates as I’ve mi
- What is the secret ingredient of tough people that enables t