第二节 几种重要的金属化合物 知识点题库
-
(1) 磁铁矿的主要成分是Fe3O4 , 其中铁元素的化合价为、.
-
(2) 采用很多方法可以鉴别Fe2+和Fe3+的溶液,下表是其中某些方法,补全下表中所缺的现象.
鉴别方法
Fe2+
Fe3+
直接观察色
棕黄色
与KSCN溶液
无现象
-
(3) 金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序.他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象如下:
金属
Ti
Mg
Cu
金属表面现象
放出气泡速度缓慢
放出气泡速度快
无变化
①三种金属的活泼性由强到弱的顺序是.
②若铜粉中混有Mg,提纯Cu时可用(填名称)除去Mg.
③Ti(钛)在化合物中的化合价为+4价,试写出Ti(钛)与盐酸反应的离子方程式.
④冶炼Ti(钛)的反应为TiO2+Cl2+2C═TiCl4+2X,其中X的化学式为.
-
(1) 请你填写下表中每步实验现象所对应的实验结论.
实验步骤及现象
实验结论(填离子符号)
取废水样品观察,呈无色
废水中不含
测所取废水样品的pH,pH=13
废水中含较多的
向废水样品中加入过量的稀盐酸,没有气泡产生
废水中不含
-
(2) 根据以上信息综合分析:
①你推测该废水中除H2O外,还含有的物质是(写化学式,下同);
②不能确定的物质是.
③为了确定可能的物质是否有,应加入的试剂是.
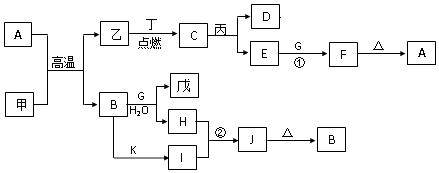
回答以下问题:
-
(1) G的电子式:
-
(2) 甲基态原子的电子排布式为,与同周期的金属元素相比,第一电离能由小到大的顺序是(用元素符号表示).
-
(3) 反应②的离子方程式:.
-
(4) 乙的高价阳离子的最高能级电子排布图为:.检验该离子常用KSCN溶液.丙的外围电子排布式为,在元素周期表中的位置为.
已知:2Na2S2O3+I2→Na2S4O6+2NaI
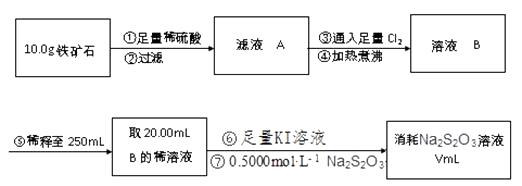
完成下列填空:
-
(1) 步骤②用到的玻璃仪器除烧杯外,还有、,步骤⑤中必须用到的定量实验仪器是。
-
(2) 步骤③对应反应的离子方程式为。
-
(3) 步骤④中煮沸的作用是。
-
(4) 步骤⑦可用淀粉作为滴定终点的指示剂,达到滴定终点时的现象是。若滴定过程中有空气进入,则测定结果。(选填“偏高”、“偏低”或“无影响”)
-
(5) 若过程⑦中消耗0.5000mol·L−1 Na2S2O3溶液20.00mL,则铁矿石中铁的百分含量为。
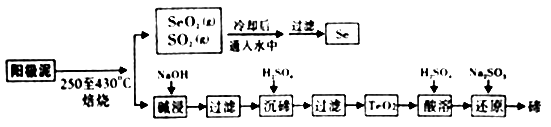
已知:①TeO2是两性氧化物。
②Se和TeO2的物理性质如下:
物理性质 | 熔点 | 沸点 | 水溶性 |
Se | 221℃ | 685℃ | 难溶于水 |
TeO2 | 733℃ | 1260℃ | 微溶于水 |
-
(1) “培烧”时,为提高原料的利用率,可采取的措施有(写一条即可)。
-
(2) “碱浸”过滤得到滤渣的主要成分是(填化学式)。
-
(3) “沉碲”时控制溶液的pH为4.5-5.0,生成TeO2沉淀。如果H2SO4的浓度过大,将导致“沉碲”不完全,原因为。
-
(4) “酸溶”将TeO2先溶于硫酸得到Te(SO4)2 , 然后加入Na2SO3溶液进行还原,还原碲的离子反应方程式是。
-
(5) SeO2与SO2的混合烟气可用水吸收制得单质Se,当有10mol电子转移时,会生成mol Se。过滤所得粗硒可采用真空蒸馏的方法提纯获得纯硒,采用真空蒸馏的目的是。
-
(6) 常温下,SeO2与NaOH溶液反应所得NaHSeO3溶液的pH7(填“>”“<”或“=”),理由是。(已知25℃时,亚硒酸(HSeO3)的Ka1=2.5×10-3 , Ka2=2.6×10-7)
-
(1) B为。
-
(2) 向一定量的Ba(HCO3)2溶液中逐滴加人C溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为,沉淀完全后,继续滴加C溶液,此时发生反应的离子方程式为。
-
(3) 向C溶液中加入Zn粒,发生反应的化学方程式为。
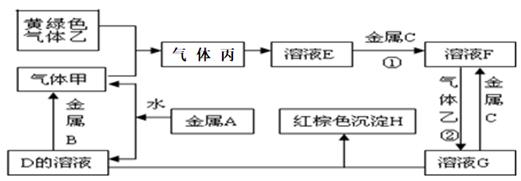
-
(1) 写出下列物质的化学式:乙、H;
-
(2) 写出反应②的离子方程式;
-
(3) 写出金属A与水反应的离子方程式;
-
(4) 写出金属B与D的溶液反应的离子方程式;
-
(5) F与D溶液反应后的产物在空气中转化为H的化学方程式;现象为。
-
(1) Ⅰ.为探究无水盐X(仅含5种元素)的组成和性质,设计并完成如下实验:
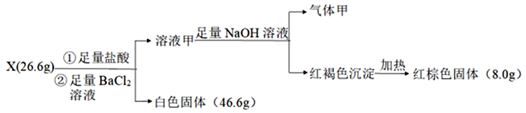
请回答:
组成X的5种元素符号是H、N;X的化学式是。
-
(2) 写出向X溶液中加入足量的浓Ba(OH)2溶液并微热的离子方程式。
-
(3) 写出检验X中金属阳离子的实验操作和现象:。
-
(4) Ⅱ.钠、镁、铁是重要的金属元素。
隔绝空气条件下,金属Na和Fe2O3粉末高温发生置换反应的化学方程式为:
-
(5) 化合物Mg (OH)2可作环保型阻燃材料,受热时按如下化学方程式分解:Mg (OH) 2
 H2O↑+MgO,该化合物作阻燃剂的可能原因是____________(填序号)
A . 氢氧化镁易升华,降低温度 B . MgO固体覆盖在可燃物表面,隔绝空气 C . 水蒸气稀释空气 D . 生成的水高温分解吸热,降低温度
H2O↑+MgO,该化合物作阻燃剂的可能原因是____________(填序号)
A . 氢氧化镁易升华,降低温度 B . MgO固体覆盖在可燃物表面,隔绝空气 C . 水蒸气稀释空气 D . 生成的水高温分解吸热,降低温度
|
| 实验 | 现象 | 结论 |
| A | 将过量铁粉加入硝酸中充分反应后滴加KSCN溶液 | 有气体生成,溶液呈红色. | 稀硝酸将Fe氧化为Fe3+ |
| B | 将铜粉加入1.0 mol·L-1的Fe2(SO4)3溶液中 | 溶液变蓝,有黑色 固体出现 | 金属Fe比Cu活泼 |
| C | 向Na2SiO3溶液中通入足量的CO2 | 产生白色胶状物质 | 非金属性:C>Si . |
| D | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 证明该溶液一定为钠盐溶液 |
-
(1) I.化合物A由三种元素组成,气体B是含氢量最高的烃。固体E既能溶于盐酸,又能溶于氢氧化钠溶液。按如下流程进行实验:
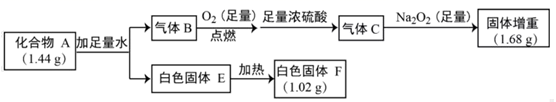
E的化学式为:,气体C与Na2O2反应的化学方程式为:
-
(2) A的化学式为:,A与足量盐酸反应的化学方程式为:
-
(3) Ⅱ.将ClO2通入NaOH和H2O2的混合溶液中,可制得一种高效漂白剂亚氯酸钠(NaClO2),实验装置如图所示:
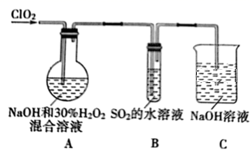
请回答:
写出A装置中发生反应的离子方程式
-
(4) 请设计实验方案探究通入足量的ClO2后,B装置溶液中存在的含有硫元素的微粒
 Cu2++2Cl-
Cu2++2Cl-
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | Na2O2可以和CO2反应产生O2 | Na2O2可用于工业制氧气 |
B | SO2具有抗氧化性且能杀菌消毒 | 葡萄酒中添加适量的SO2 |
C | SiO2具有良好的半导体性能 | SiO2可用于制备光导纤维 |
D | NH3能使酚酞溶液变红 | NH3可用于设计喷泉实验 |
- --- Look! Thetelephone is broken. Someone damaged it ______
- 材料一 2007年10月15日,中国第十七次全国代表大会召开。大会的主题是:高举中国特色社会主义伟大旗帜,以理论和“
- 非洲自然带南北对称分布明显的原因是( ) ①沙漠面积大②地形单一、海岸平直③赤道横贯中部,非洲大陆在气压带和风带位置
- (12分)阅读材料,回答问题。 材料 针对18世纪的英国市场机制究竟发挥多大作用,以及给英国社会带来怎样的影响,史学界
- 已知函数若,则实数a的取值范围是 ▲ .
- 在“探究运动和力的关系”的实验中,让小车每次从斜面顶端处由静止滑下,改变水平面的粗糙程度,测量小车在水平面上滑行的距离,
- 能对空气造成污染的一组气体是() A.氮气、稀有气体 B.稀有气体、二氧化碳 C.二氧化碳、水蒸气 D.二氧化硫、二氧化
- 如图(a)所示,实心正方体A、B放置在水平地面上,受到的重力分别为20牛和60牛,A的边长为0.2米,B的边长为0.3米
- It might sound unbelievable that two kidsunder the age of te
- 用一句话概括下面这则新闻报道的主要内容。(字数不超出空格的限制)(2分)据英国《独立报》报道,200名鸟类学家近日出席了
- 除去下列物质中括号内少量杂质的方法,合理的是()A. CaO(CaCO3):加入足量的稀盐酸 B. CO2(CO):在氧
- 元素X的原子最外电子层中具有最多的未成对单电子,元素Y的原子核只有两种形状的电 子云,且两种电子云的电子数相等,则X、Y
- 单项选择 —Do you know the first ladies ofChina and the USA had _
- 下列说法中正确的是()A.同系物之间互为同分异构体B.两个同系物之间的式量一定相差14C.所有的烯烃都一定互为同系物D.
- 下列各句中,没有语病的一项是 ( )
- 某蛋白质分子由N条肽链组成,已知它共由M个氨基酸组成,则此蛋白质中至少含有的氧原子数与氮原子数共有 A.(M+N)个
- 近来网上相继爆出令人担忧的“XX门事件”,对社会产生不良的影响,其主人公绝大多数都是“90后”的青少年。为此,青少年要
- 俄国在城市中的司法制度方面的改革措施不包括( ) A. 要在同一法院进行审判 B.要依照同一法律进行审判
- Your computer has been playing music for years, one CD at a
- 珠江三角洲利用其紧邻港澳的位置,国家特殊的政策,成为我国最早发展_____经济的地区之一



