第二节 几种重要的金属化合物 知识点题库
,反应后得到的FeCl3溶液呈棕黄色,用此溶液进行以下实验:
(1)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3 溶液,继续煮沸至溶液成红褐色,停止加热,制得的分分散系中分散质粒子直径大小为.
(2)向(2)中烧杯中的分散系中逐滴滴入过量盐酸,会再出现一系列变化:
①先出现红褐色沉淀,原因是 .
②随后沉淀逐渐溶解,溶液呈棕黄色,反应的离子方程式为 .
-
(1) 若纯碱中含NaHCO3所需盐酸用量,产生的气体;
-
(2) 若纯碱中含K2CO3所需盐酸用量,产生的气体;
-
(3) 若纯碱中含NaCl所需盐酸用量,产生的气体.
-
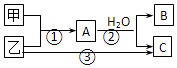
(1) Ⅰ.铁矿石中含氧量的测定,以下实验过程不完整,请在图1中补充完整.
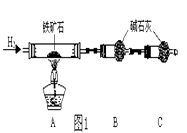
①按上图组装仪器,并;
②将8.0g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
③从左端导气管口处不断地缓缓通入H2 , ,点燃A处酒精灯;
④充分反应后,撤掉酒精灯,;
⑤测得反应后装置B增重2.25g,则铁矿石中氧的百分含量为.
-
(2) Ⅱ.铁矿石中含铁量的测定如图2所示.
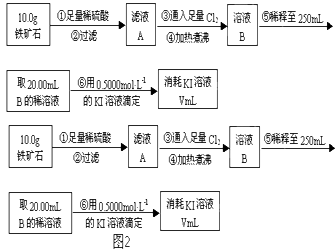
步骤④中煮沸的作用是.
-
(3) 步骤⑤中用到的玻璃仪器有烧杯、胶头滴管、250mL容量瓶、.
-
(4) 下列有关步骤⑥的操作中说法正确的是.
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.锥形瓶不需要用待测液润洗
c.滴定过程中可利用淀粉溶液作为指示剂
d.滴定过程中,眼睛注视滴定管中液面变化
e.滴定结束后,30s内溶液不恢复原来的颜色,再读数
f.滴定结束后,滴定管尖嘴部分有气泡,则测定结果偏大
-
(5) 若滴定过程中消耗0.5000mol•L﹣1的KI溶液20.00mL,则铁矿石中铁的百分含量为.
-
(6) Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为.
-
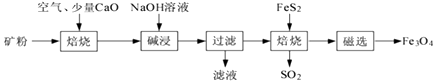
(1) 焙烧过程均会产生SO2 , 用NaOH溶液吸收过量SO2的离子方程式为 。
-
(2) 添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如题图所示。
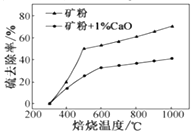
已知:多数金属硫酸盐的分解温度都高于600℃;硫去除率=(1-
 )×100%。
)×100%。①不添加CaO的矿粉在低于500℃焙烧时,去除的硫元素主要来源于。
②700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是。
-
(3) 向“过滤”得到的滤液中通入过量CO2 , 铝元素存在的形式由(填化学式)转化为(填化学式)。
-
(4) “过滤”得到的滤渣中含大量的Fe2O3 . Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2 , 理论上完全反应消耗的n(FeS2):n(Fe2O3)=。
-
(1) 在Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”(指能量相同的原子轨道在全满、半满、全空状态时,体系的能量最低),该原子的外围电子排布式为。
-
(2) 在第四周期所有元素中,基态原子未成对电子数最多的元素是(填元素符号)。
-
(3) 金属晶体热导率随温度升高会降低,其原因是。
-
(4) 铜的焰色反应呈。在现代化学中,常用于区分晶体与非晶体的方法为。
-
(5) Mn和Co的熔点较高的是,原因。
-
(6) 钴晶胞和白铜(铜镍合金)晶胞分别如图1、2所示。
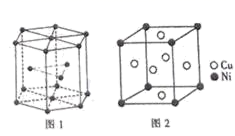
①钴晶胞堆积方式的名称为;
②已知白铜晶胞的密度为dg·cm-3 , NA代表阿伏加德罗常数的值。图2晶胞中两个面心上铜原子最短核间距为 pm(列出计算式)。
-
(1) 除去镁粉中混有的少量铝粉,加入某试剂后反应的离子方程式为
-
(2) 某同学在实验室用铝土矿(含有
 和
和  ,不考虑其他杂质)取金属铝的流程如下:
,不考虑其他杂质)取金属铝的流程如下: 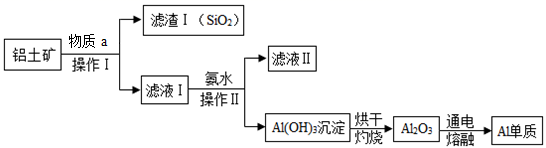
①操作Ⅰ所加物质a为(选填
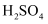 或NaOH),
或NaOH),  与a反应的离子方程式为。
与a反应的离子方程式为。②滤液Ⅱ中溶质的用途之一是。
③工业上在电解熔融的
 时,还加入了冰晶石
时,还加入了冰晶石  作熔剂,其作用是降低
作熔剂,其作用是降低  的熔点。冰晶石在物质的分类中属于(填字母)。
的熔点。冰晶石在物质的分类中属于(填字母)。a.酸 b.碱 c.盐 d.氧化物
-
(3) 铝与
 在酸性或碱性条件下均可反应,为了降低饮用水中
在酸性或碱性条件下均可反应,为了降低饮用水中  的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将  还原为
还原为 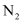 ,完善并配平该反应:
,完善并配平该反应:  ,。每消耗
,。每消耗 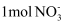 ,转移的电子数目为。
,转移的电子数目为。
-
(4) 已知:CCl4与水不相溶且密度比水大,Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色,且Br2易从水溶液中溶入CCl4中。Cl2既能氧化
 ,也能氧化
,也能氧化 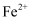 。
。 ①取
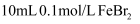 溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4 , 振荡后,下层为无色液体。以上实验结论表明还原性:
溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4 , 振荡后,下层为无色液体。以上实验结论表明还原性: 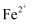
 (填“>”或“<”)。
(填“>”或“<”)。②若在
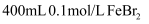 溶液中通入标准状况下672mL的Cl2 , 取少量反应后的溶液加入CCl4 , 振荡后下层液体呈色,写出该反应的离子方程式。
溶液中通入标准状况下672mL的Cl2 , 取少量反应后的溶液加入CCl4 , 振荡后下层液体呈色,写出该反应的离子方程式。
 C . 向浸取液中加入KSCN溶液,无明显现象,滴入新制氯水后,溶液变为红色,说明雾霾中Fe2+
D . 向浸取液中加入浓NaOH溶液微热,试管口附近湿润的红色石蕊试纸变蓝,说明雾霾中一定含有
C . 向浸取液中加入KSCN溶液,无明显现象,滴入新制氯水后,溶液变为红色,说明雾霾中Fe2+
D . 向浸取液中加入浓NaOH溶液微热,试管口附近湿润的红色石蕊试纸变蓝,说明雾霾中一定含有 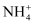
-
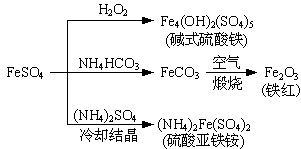
(1) 写出实验室用
 溶液制取
溶液制取 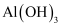 沉淀的离子方程式: 。
沉淀的离子方程式: 。
-
(2) 浓硝酸应贮存在避光低温处,原因是:(用化学方程式表示)。
-
(3) 乙烷气体(
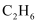 )的标准燃烧热
)的标准燃烧热 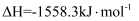 ,则乙烷气体燃烧的热化学方程式可表示为:。
,则乙烷气体燃烧的热化学方程式可表示为:。
 B .
B . 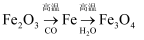 C .
C .  D .
D . 
①钠与水反应生成NaOH 和H2;所有金属与水反应都生成碱和H2
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③化合物KCl的焰色为紫色;K2CO3的焰色也为紫色
④钠钾合金的熔点应介于Na和K熔点之间
- 阅读下面的材料,回答问题。某翻译家在《文艺报》上撰文指出:有人说中国人称自己的国家为“中国”,表示自己是坐镇在世界中央的
- 下列A~D 4组,每组有两个反应,其中两个反应可用同一个离子方程式表示的一组是
- 1854年5月30日,英国战舰“欧罗巴”的船舱里装滿了供战马的草料,航行途中 突然草料着火,整个战舰瞬间变为火海。则下列
- 有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大, 已知A和B原子有相同的电子层数, 且A的L层电子数是
- 下列实验操作中,正确的是 A.倾倒液体
- 已知椭圆C:()的离心率为,点(1,)在椭圆C上. (Ⅰ)求椭圆C的方程; (Ⅱ) 在x轴上是否存在一定点E,使得对椭圆
- 如图,已知AB=AC,BD=CD,则可推出( ) A.△ABD≌△BCD B.△ABD≌△ACD C.△ACD≌△B
- -- We’re organizing a party next Saturday, and I’d like you
- I__ my raincoat inLucy’s room yesterday. A.leave B.
- 若长度分别为a,3,5的三条线段能组成一个三角形,则a的值可以是() A.1 B.2
- 木块A、B分别重50 N和60 N,它们与水平地面之间的动磨擦因数均为0.25;夹在A、B之间弹簧压缩了2cm,弹簧的劲
- 1912年4月22日《申报》刊载《西装叹》:“更有西装新少年,短衣窄袖娇自怜。足踏黄革履,鼻架金丝边。自诩开通世莫敌,爱
- 恩格斯在《法国状况》中说:“他把他的法典带到被征服的国家里,这个法典比历来的法典都优越得多”,文中“法典”根本的贡献在于
- 由于经常遭受地震袭击,智利深知大地震的破坏力无法抵抗,所以建筑设计师们广泛采用“强柱弱梁”的抗震设计,它的设计理念不是像
- 《闻一多先生的说和做》的作者是现代著名诗人 ,代表作有
- Was it ______ Expo 2010 that made Shanghai the focus of the
- 如图(a)、(b)所示,“跳橡筋”和“打陀螺”是老上海典型的弄堂游戏,其中图5______主要表示了力可以使物体发生形变
- (5分)下列各组物质:① O2和O3 ; ② 1H、2H、3H; ③ CH4和C10H22; ④乙烷和(CH3)2CHC
- 一、现代文阅读(9分,每小题3分) 阅读下面的文字,完成1~3题。 逻辑思维是正确思维的基础,而形象思维是正确思维的主要
- 下列各句没有语病的一项是( ) A.在使用电器的时候,一旦出现漏电的现象,应当立即切断电源是最要紧的。 B.老师对我



