课题1 常见的酸和碱 知识点题库

【提出问题】
问题1:铁为何称为黑色金属?
问题2:铁和氧气在不同条件下能发生哪些反应?
问题3:铁有多种氧化物,它们的性质有哪些差异?
问题4:钢铁厂在选矿时,如何测定铁矿石中的含铁量?
问题5:用一氧化碳还原氧化铁得到的黑色固体一定是单质铁吗?
Ⅱ.解决问题
【问题1】上网查寻,有两种说法
a.因为在铁表面有黑色的铁的氧化物,所以叫黑色金属
b.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属
-
(1) 你认为正确的说法是(填“a”或“b”)
-
(2) 【问题2】通过学习,已经知道铁丝在潮湿的空气中能生锈,也能在纯氧中燃烧.
请写出一种防止钢铁生锈的方法;
请写出铁丝在纯氧中燃烧的化学方程式.
-
(3) 【问题3】查阅资料:a.铁常见的氧化物有氧化铁(Fe2O3)、四氧化三铁(Fe3O4)和氧化亚铁(FeO).
b.四氧化三铁是具有磁性的黑色晶体,可以近似地看怍是氧化亚铁和氧化铁的化合物.它不溶于水,能与酸反应生成两种盐.
c.氧化亚铁是不溶于水的黑色粉末,能与酸反应,无磁性,也不能被磁铁吸引.
请写出四氧化三铁与盐酸反应的化学方程式.
-
(4) 【问题4】同学们参观了某钢铁厂,了解到钢铁厂在选矿时测定铁矿石中含铁量的方法较多,小明结合所学知识,设计了如图1所示的实验装置测定某赤铁矿样品中Fe2O3的质量分数.他称取10.0g赤铁矿,当赤铁矿中的Fe2O3全部还原为Fe时,剩余固体在CO的保护下冷却、称量.质量为7.6g(假设赤铁矿中的杂质均不与CO反应).
图中酒精灯的作用是.
-
(5) 该赤铁矿中Fe2O3的质量分数为(列出计算过程).
-
(6) 【问题5】在钢铁厂的实验室.同学们采集了用某种热分析仪记录的CO与Fe2O3进行反应时的有关数据,并得到固体质量与反应温度的关系曲线.如图2所示.
根据图象分析,写出P点时固体成分的化学式.固体质量由48.0g变为46.4g的过程中发生反应的化学方程式为.
-
(1) 给自来水消毒时常用漂白粉等含氯元素的物质,检查自来水中是否含Cl﹣的方法是
-
(2) 酸性的雨水并不都是酸雨,正常的雨水略显酸性,其原因是(用化学方程式表示).
-
(3) 铝壶用过一段时间后,会在底部形成淡黄色水垢,可用厨房中的(填物质名称)将其除去,但用该物质除水垢不能长时间浸泡,原因是.
-
(4) 柴油机在工作时由喷油嘴向气缸内喷入雾状柴油,这样做的目的是.否则会产生有毒气体.
-
(5) 用石灰浆砌墙壁,熟石灰会逐渐和空气中的二氧化碳反应生成碳酸钙,检测墙壁中熟石灰是否反应完全了的方法是.

-
(1) 依据步骤①的实验现象得出固体物质中一定不含.
-
(2) 固体物质中一定含有,可能含有,为进一步确定可能含有的物质,采用的方法是(写出实验操作).
选项 | 物质(括号内为杂质) | 除去杂质的方法 |
A | CO2(CO) | 通过NaOH溶液 |
B | N2(O2) | 通过灼热的铜网 |
C | CaCl2固体(CaCO3) | 加足量稀盐酸、蒸发、结晶 |
D | HNO3溶液(HCl) | 加适量AgNO3溶液、过滤 |

试推断:
-
(1) 气体B是(写化学式).
-
(2) 固体A中一定没有的物质是.(写名称)
-
(3) 滤液D中一定有含有的溶质是.
-
(4) 固体A的组成可能有种.
-
(5) 产生蓝色沉淀的化学反应方程式.

-
(1) 图A实验中能得到铁生锈的条件之一是:与接触
-
(2) 图B实验中热水的作用是
-
(3) 图C中用玻璃棒搅拌的目的是
-
(4) 在配制一定溶质质量分数的氯化钠溶液时,量取水的操作如图D所示,所配溶液的溶质质量分数会(填“偏大”或“偏小”)
-
(1) 不能用凉白开养鱼,原因是。
-
(2) 自热米饭用生石灰和水做热源,原因是。

-
(1) 写出下列物质的化学式:A。
-
(2) 反应Ⅰ的化学方程式为,此反应属于(填基本反应类型)反应;反应Ⅱ的化学方程式为。
-
(3) “反应Ⅰ”和“反应Ⅱ”中能体现相互转化的物质是。(填化学式)
 称量氢氧化钠固体
B .
称量氢氧化钠固体
B .  铁丝在氧气中燃烧
C .
铁丝在氧气中燃烧
C .  收集氧气
D .
收集氧气
D .  稀释浓硫酸
稀释浓硫酸
 B . 倾倒液体
B . 倾倒液体  C . 加热固体
C . 加热固体  D . 检查装置的气密性
D . 检查装置的气密性 
 闻气体气味
B .
闻气体气味
B .  稀释浓硫酸
C .
稀释浓硫酸
C .  加入大理石块
D .
加入大理石块
D .  氧气验满
氧气验满

(查阅资料)
[用法用量]外用,一日1次。将外袋剪开,取出药袋,晃动数次,使药物充分松散,接触空气,手摸有热感时,置于固定袋内,覆盖于痛患处,每袋可发热不少于15小时。
[原料层]铁、蛭石、活性炭、水等。
[作用原理]铁跟氧气和水反应生成氢氧化铁(固体),并放热。
-
(1) (实验一)验证寒痛乐成分中所含铁的化学性质。
步骤
实验操作
实验现象
①
将寒痛乐打开,将药物倒入一烧杯中,观察
药物为黑色固体粉末
②
用一条形磁铁与烧杯中的黑色粉末充分接触,取适量吸附在磁铁上的黑色粉末放于燃烧匙中,在酒精灯上点燃后伸入盛有氧气的集气瓶中,观察
剧烈燃烧,
实验结论:写出此反应的文字表达式。集气瓶中加水的作用是。
-
(2) (实验二)用寒痛乐熨剂药粉测定空气中氧气的含量。甲同学设计了如下图所示装置,进行实验。
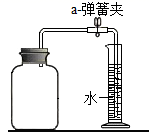
(实验记录)
步骤
实验操作
主要实验现象
实验结论及解释
①
连接好装置如上图所示,然后
装置的气密性良好
②
加入足量药品,迅速将胶塞盖严,并充分振荡
进入集气瓶内水的体积即为空气中氧气的含量。


-
(1) 实验I中,在点滴板的a、b穴中滴入NaOH溶液后,b处变为色。
-
(2) A瓶变瘪,写出A瓶中反应的化学方程式。小明认为不能证明NaOH溶液和
 反应,原因是。写出B瓶中反应的化学方程式。
反应,原因是。写出B瓶中反应的化学方程式。
| A | B | C | D |
| | | | |
| 检查装置气密性 | 称量质量 | 稀释浓硫酸 | 蒸发食盐水 |
- 日本明治维新取得巨大成功是多种因素综合作用的结果,其主导因素是 A.天皇权利至高无上,支持革新派进行改革B.废藩置县,建
- 把多项式按字母降幂排列是
- 设NA为阿伏加德罗常数。下列叙述中正确的是() A.10 gHO中所含的中子数为4NA B.1 mol苯分子中含有的碳碳
- 汉高祖刘邦想废太子(吕后所生长子,即汉惠帝刘盈)而立戚姬之子如意为新太子。御史大夫周昌说:“臣口不能言,然臣期期知其不可
- 修改下面的一个病句 雅典奥运会开幕式精彩绝伦,可以堪称一流,受到世界舆论的普遍赞誉。
- 古诗文积累:(6分)【小题1】、在《春望》中,春天的花开鸟鸣反而使诗人杜甫生出忧国和思亲之情,即所谓“_________
- 下列句子中,标点符号使用正确的一项是 A.所谓“以人为本,”在很大程度上就是顺应民心,而不是修正民心。 B.别人没想到的
- 在物理学发展的过程中,许多物理学家的科学发现推动了人类历史的进步。对以下几位物理学家所作科学贡献的表述中,与事实相符的是
- 已知反比例函数,在其图像所在的每个象限内,的值随值的增大而_______(填“增大”或“减小”);
- 如图所示,倾斜导轨宽为L,与水平面成α角,处在方向竖直向上、磁感应强度为B的匀强磁场中,金属杆ab水平放在导轨上.当回路
- 目前,“订单实训”的职业培训新型模式深受用人企业和劳动者的青睐。这种培训模式以就业为导向,以用人单位的实际需求为目标,努
- 2015年11月21日,李克强提出,愿与东盟及其它各方共同努力,力争2016年内结束区域全面经济伙伴关系协定(RCEP)
- 已知向量,,其中.函数在处取最小值. (1)求的值;(2)设,,为的三个内角,若,,求.
- 古代诗歌阅读(11分) 梅 雨 柳宗元 梅实迎时雨①,苍茫值晚春。愁深楚猿夜,梦断越鸡晨②。 海雾连南极,江云暗北津
- 下面是四位同学对他们学习小组将要共同进行的一次统计活动分别设计的活动程序,其中正确的是() A. B. C.
- 对于反应:2SO2+O2===2SO3,当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入下表空格里
- There is not enough oil in the world now. As time goes by ,i
- 下列说法中正确的是:A.我们能看到月亮,说明了月亮是一个天然光源;B.挖隧道用“激光准直”是利用了光在均匀介质中沿直线传
- 读右图回答问题: (1)A点的地理坐标是 (2)B在D的 方向。B点属于 东
- 读中国太阳年辐射总量的分布图,回答7—8题7、我国太阳年辐射总量丰富地区和最不丰富的地区是 A.准噶尔盆地、台湾岛







