第八单元 海水中的化学 知识点题库
甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是()

A . t1℃时,甲、乙的溶解度相等
B . t2℃时,甲的溶解度为50
C . 甲中混有少量的乙时,可用降温结晶的方法提纯甲
D . t1℃时,甲、乙两种饱和溶液恒温蒸发等质量的水,析出晶体的质量相等
溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
-
(1) 可以作为溶质的是。
A 只有固体 B 只有液体 C 只有气体 D 气体、液体、固体都可以
-
(2) 在盛有水的烧杯中加入以下某种物质,形成溶液后,温度下降。这种物质可能是___。A . 氯化钠 B . 硝酸铵 C . 氢氧化钠 D . 蔗糖
-
(3) 下图为甲、乙、丙三种固体物质的溶解度曲线,请回答有关问题。

①将一瓶接近饱和的丙溶液变成饱和溶液,除通过增加溶质、蒸发溶剂使其达到饱和外,还可采取的方法。
②将t3℃时等质量的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液的质量由大到的顺序为。
③t3℃时,取甲、乙两物质配制溶液。
序号
a
b
c
d
e
固体种类
甲
甲
甲
乙
乙
甲固体的质量/g
30
60
90
30
60
水的质量/g
100
100
100
100
100
-
(4) I.关于a~e所得溶液属于饱和溶液的是。
-
(5) II.下列关于a~e所得溶液的说法错误的是_____。A . b溶液恒温蒸发25g水后,与c溶液溶质质量分数相等 B . e溶液的溶质质量分数为37.5% C . 将a、d溶液降温至t1℃,均有晶体析出 D . c溶液恒温蒸发溶剂后,溶质质量分数变大
化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合下列流程图(其中部分操作和条件已略去),请回答相关问题:

-
(1) 提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有氯化镁、硫酸钠氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤加入下列三种溶液的先后顺序为(填字母序号)。
a.稍过量的Na2CO3溶液
b.稍过量的BaCl2溶液
c.稍过量的NaOH溶液
-
(2) 母液中有MgCl2 , 却经历了步骤Ⅳ、Ⅴ的转化过程,其目的是。
-
(3) 步骤Ⅱ中先向饱和食盐水中通入氨气,有利于二氧化碳的吸收,这样做的目的是,写出该反应的化学方程式。
许多物质在溶液中都以离子形式存在。我们熟悉的复分解反应就是溶液中离子间结合得到水、气体或沉淀的一类化学反应。如:氢氧化钠与盐酸的反应就是溶液中的H+和OH-结合成水分子的过程(如图)。结合信息、图示,你认为下列各组离子间不能反应的是( )

A . H+、Na+、OH-、NO3-
B . Na+、K+、Cl-、OH-
C . H+、K+、CO3²-、HCO3-
D . K+、Ba²+、Cl-、SO42-
取小苏打样品,来测定其中碳酸氢钠的质量分数(假设该样品中只含有氯化钠一种杂质)。取样品10 g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如图所示,求:
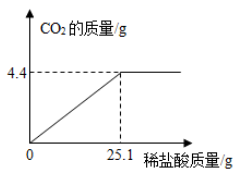
-
(1) 样品中碳酸氢钠的质量分数。
-
(2) 恰好完全反应时,所得溶液中溶质的质量分数。
将某溶液分装在两支试管中,其中一支加入氢氧化钠,另一支加入硝酸钡,结果前者产生红褐色沉淀,后者产生白色沉淀,则原溶液是( )
A . CuCl2
B . Fe2(SO4)3
C . FeCl3
D . Cu(NO3)2
下表是甲和乙在不同温度时水中的溶解度,根据此表回答:
|
温度/℃ |
10 |
20 |
30 |
40 |
50 |
|
|
溶解度/g |
甲 |
30 |
33 |
35 |
38 |
41 |
|
乙 |
21 |
31 |
45 |
65 |
88 |
|
-
(1) 从表中数据可以看出,两种物质的溶解度受温度影响变化较大的是。
-
(2) 在30℃时,100g水中加入50g甲,充分搅拌后得到的溶液质量为g。
-
(3) 由表中的数据分析可知,甲和乙在某一温度时具有相同的溶解度xg。则x取值范围是。
-
(4) 某同学取甲、乙中的一种物质,按如图所示进行实验,下列有关说法错误的是(填序号)。

①烧杯中加入的是乙
②w取值为50
③40℃时,甲、乙的饱和溶液中溶质的质量乙>甲
④将等质量的甲、乙分别加入等质量的水中,所得溶液的溶质质量分数甲=乙
甲和乙两种物质的溶解度曲线如图所示,回答下列问题:

-
(1) 在t1℃时,甲、乙溶解度大小关系为;
-
(2) 若甲物质中含有少量的乙物质,可用的方法提纯甲(填“降温结晶”或“蒸发结晶”);
-
(3) 若将甲物质的不饱和溶液变为饱和溶液,可以。
如图表示X、Y两种不含结晶水的固体物质的溶解度曲线。根据图示判断下列说法中错误的是 ( )

A . t1℃时X的溶解度大于Y的溶解度
B . X、Y都属于易溶性物质
C . 将t1℃时X、Y的饱和溶液均分别降温至t℃,析出的X比Y的多
D . 当X中含有少量Y时,能通过降温结晶的方法提纯X
下列反应属于复分解反应的是( )
A . NaOH + HCl = NaCl +H2O
B . Mg + 2HCl = MgCl2 + H2↑
C . H2CO3=H2O + CO2↑
D . CO2 + Ca(OH)2=CaCO3↓+H2O
根据如图甲、乙两种物质的溶解度曲线回答相关问题:

-
(1) 常压下,CO2在水中的溶解度随温度的变化趋势类似于(填“甲”或“乙”)曲线。
-
(2) t2℃时若将75g甲的饱和溶液稀释成10%,需加水的质量为。
-
(3) 将t2℃时,甲、乙两种物质的饱和溶液降温至t1℃(其他条件不变),所得溶液的溶质质量分数的关系是甲乙。(填“>”“<”或“=”)
海水通过晒制得到的粗盐中常含有泥沙、MgCl2、CaCl2、Na2SO4等杂质,以下是除去粗盐中可溶性杂质的过程,下列说法正确的是( )

A . BaCl2和Na2CO3的添加顺序不能颠倒,否则除不尽Ba2+
B . 滤渣中共有三种沉淀
C . 为证明所加盐酸过量,可取少量溶液B,向其中滴加硝酸银溶液,看是否有沉淀生成
D . 经过一系列除杂操作后,最终得到溶液B中的溶质只有NaCl
生活中衣、食、住、行蕴含着丰富的化学知识。下列说法错误的是( )
A . 炒菜时油锅中的油不慎着火,立即盖上锅盖灭火
B . 用食盐水除热水瓶胆内壁上沉积的水垢
C . 建造高楼大厦时所用到的钢和生铁属于铁的两种合金
D . 公交车用天然气代替汽油作燃料可减少空气污染
下面是某同学采用的几个实验装置示意图。
A  测定空气中氧气的含量
测定空气中氧气的含量
B  电解水
电解水
C  处理浑浊的水
处理浑浊的水
-
(1) 不能达到实验目的是(填字母)。
-
(2) B实验中电源正极产生的气体是。电解水的化学方程是。
-
(3) C实验中玻璃棒的作用是。
煤是重要的化石燃料之一,如图是煤的精炼和综合利用的流程图。

-
(1) 反应①的化学方程式为;脱硫属于(填物理变化、化学变化)。
-
(2) “脱硫”的目的是减少二氧化硫的排放,二氧化硫对环境的影响主要是____(填序号)。A . 臭氧层空洞 B . 沙尘暴 C . 雾霾 D . 酸雨
-
(3) 脱硫时生成硫酸钙的化学反应为:
 则 X 的化学式为,操作 a 的名称是。
则 X 的化学式为,操作 a 的名称是。
-
(4) 溴乙烷(CH3CH2Br)在一定条件下能脱去溴化氢(HBr)分子,同时生成乙烯(C2H4),该反应在有机化学中称为消去反应,反应的化学方程式为:
 。反应③也属于消去反应,写出该反应的化学方程式。
。反应③也属于消去反应,写出该反应的化学方程式。
如图为A、B两种物质的溶解度曲线。回答下列问题:

-
(1) 说出P点的意义是什么?
-
(2) t2℃时,向30gA物质中加入50g水,充分溶解后,所得溶液质量是多少?
-
(3) 将t2℃时A、B的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小的大小关系是什么?
下列对实验现象的描述或实验操作正确的是( )
A . 红磷在空气中燃烧,产生大量白雾
B . 点燃或加热可燃性气体前,检测其纯度
C . 稀释浓硫酸时,将水倒入浓硫酸中,并不断搅拌
D . 蒸发食盐水时,待蒸发皿中水分蒸干后停止加热
世界万物都是由极其微小的粒子构成的,下列有关分子、原子、离子的说法错误的是( )
A . 铁是由铁原子构成的
B . Na+、  、Ba2+、Cl-四种离子在溶液中可以共存
C . 保持氧气化学性质的最小微粒是氧分子
D . 水通电分解的过程中,分子的种类发生了变化
、Ba2+、Cl-四种离子在溶液中可以共存
C . 保持氧气化学性质的最小微粒是氧分子
D . 水通电分解的过程中,分子的种类发生了变化
 、Ba2+、Cl-四种离子在溶液中可以共存
C . 保持氧气化学性质的最小微粒是氧分子
D . 水通电分解的过程中,分子的种类发生了变化
、Ba2+、Cl-四种离子在溶液中可以共存
C . 保持氧气化学性质的最小微粒是氧分子
D . 水通电分解的过程中,分子的种类发生了变化
下列物质间的转化,不能通过一步反应实现的是( )
A . CuO→Cu(OH)2
B . H2O2→O2
C . MgO→MgCl2
D . KOH→K2SO4
如图所示是甲、乙两种固体物质(不含结晶水)的溶解度曲线。
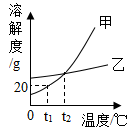
-
(1) 甲、乙的溶解度相同的温度为。
-
(2) t1℃时,将10g甲加入20g水中充分溶解,得到溶液的质量为g;将t1℃时60g甲的饱和溶液稀释为10%的稀溶液,需加水g。
最近更新
- 在“测量电阻丝的电阻率”的实验中,(1)用螺旋测微器测量电阻丝的直径为 ▲ mm:已知电阻丝的电阻RX约为10 Ω,
- (13分)已知某工业废水中含有大量FeSO4,较多的Cu2+,少量的Na+ 以及部分污泥,通过下列流程可从该废水中回收F
- 分解因式:
- 在育种上,用秋水仙素处理单倍体植株的幼苗,是为了获得 A.纯合子 B.多倍体 C.杂合
- 对于外资银行落户中国农村,有人认为:外资银行进入农村肯定赚不到钱;但也有人认为:外资银行进入农村长期发展潜力巨大。材料表
- 5.名著阅读(3分) (1)在西方,有一部小说,卢梭曾建议每个青少年,尤其是男孩子都应该读读它。小说主人公是一位孤独而顽
- 根据你对生活中物理量的认识,下列数据符合实际的是( ) A.教室里讲台的高度约为10 m
- PM2.5指标是指大气中直径小于或等于2.5 μm的颗粒物。下列措施对PM2.5的治理起不到积极作用的是A.城市道路定时
- 读图4,完成25~26题。25.右图所示的箭头中,代表近地面大气主要直接热源 的是( ) A.① B
- With science and technology advancing, plentiful kinds of me
- 如果发现了原子序数为116的元素,下列对它的叙述中正确的是( ) ①位于第7周期 ②非金属元素 ③最外电
- 一个正四棱柱的顶点均在半径为1的球面上,当正四棱柱的侧面积取得最大值时,正四棱柱的底面边长为() A. B.
- 下列各组物质中互为同系物的是( ) A.H—OH和CH3—OH B.CH3CH2OCH2
- 下列微粒中,与氩原子具有相同电子层结构的是 ( )
- 著名科学家李约瑟在《中国科技史》中提出“他们固然没有把个人和社会分开,也没有把社会人与整个自然界分开。可是他们向来主张,
- 如图:通电5min后,电极5质量增加2.16g,试回答:(1)1是_____极。 (2)若A池溶液体积为200mL(设电
- —When will Diana arrive? —Oh,she__ __.She is in the meeting
- 名著知识 ⑴“又是秋天,妹妹推我去北海看了菊花。黄色的花淡雅、白色的花高洁、紫红色的花热烈而深沉,泼泼洒洒,秋风中
- 在“探究凸透镜成像规律的实验”中,将蜡烛置于透镜前30cm处时,在另一侧的光屏上得到了一个倒立、放大清晰的像,现保持透镜
- 农作物育种上,采用的方法有:诱变育种、杂交育种、多倍体育种、单倍体育种,它们的理论依据依次是() ①基因突变 ②基因交



