第八单元 海水中的化学 知识点题库
有关物质用途错误的是( )
A . 胆矾检验水
B . 食盐水消毒伤口
C . 盐酸除铁锈
D . 一氧化碳冶炼金属
下列图像表示的对应关系正确的是( )

A . 图①表示煅烧石灰石
B . 图②表示CO2在水中的溶解性
C . 图③表示向NaOH溶液只加水
D . 图④表示将弄硫酸加入水中
对化学反应A+B=C+D的下列说法中正确的是( )
A . 若A是稀硫酸,则生成物质中一定有水
B . 若C,D是盐和水,则A,B不一定是酸和碱
C . 若A是可溶性碱,B是可溶性盐,则C,D不可能是两种沉淀
D . 若A,B,C,D都是化合物,则该反应不一定是复分解反应
磷酸铁锂(
LiFePO4)电池具有稳定性高、安全、对环境友好等优良性能,是目前最具有发展前景的锂电池正极材料。实验室可利用绿矾(FeSO4·7H2O)和磷酸(H3PO4)为原料制备LiFePO4 , 其流程如图所示。已知磷酸铁(FePO4)是一种难溶于水的白色固体。

试回答下列问题:
-
(1) NaClO中氯元素的化合价为价。
-
(2) “溶解”步骤时H3PO4不宜过量太多的原因是。
-
(3) 过滤操作中用到的玻璃仪器有:烧杯、玻璃棒和。
-
(4) 磷酸与氢氧化钠溶液反应化学方程式为:;
-
(5) 请你完成“反应2”总反应的化学方程式。2LiOH+6H2C2O4+2FePO4→2 LiFePO4+7CO2+5+7HO(在横线中填写正确的化学式)。
某校化学活动小组的同学在学习完酸、碱、盐的化学性质后,进行了如图所示的实验,现在请你来参与他们的探究活动,并回答下列问题。

-
(1) 【实验探究】甲同学观察到红色溶液逐渐变浅,从而得出稀盐酸能与氢氧化钠发生反应。乙同学不同意甲的观点,理由是 。
实验结束后,同学们将甲、乙两个试管内的物质全部倒入同一个干净的废液缸中,最终看到烧杯中液体浑浊并呈红色,过滤后得废液,由此现象得出此废液中一定不含有的离子是(填离子符号)。
-
(2) 【提出问题】废液中除了Na+和Cl-外,含有哪些离子呢? (酚酞除外)
【猜想与假设】同学们思考交流后,有如下猜想:
甲:CO32- OH 乙:CO32- 丙:OH-
请你再写出一种合理猜想:。
-
(3) 【活动与探究】甲同学进行了如右图实验

【实验与结论】于是甲同学得出自己的猜想正确,小组同学经讨论得出甲同学由实验得出的结论不正确,理由是:。
小组同学经过讨论把甲同学的实验进行了改进,最终得出了甲同学的猜想正确。
-
(4) 【继续探究】小组同学通过实验探究出了废液中可能存在的两种阴离子的存在,同学们通过实验又证明出另一种一定存在阴离子,实验步骤:重新取废液,加入溶液,然后再加入溶液,当观察到现象,即可确定阴离子的成分。
-
(5) 【反思与结论】在探究离子成分时选择试剂时要注意的问题是:。
根据如图所示实验回答问题。

①甲图实验中若止水夹未夹紧,测得氧气的体积分数(填“偏大”或“偏小”)。
②乙图实验中烧杯内热水的作用是。
③丙图为蒸发溶液的实验,当观察到时,停止加热。
④丁图实验时玻璃管中的现象是,其反应的化学方程式。
下列实验方法正确的是( )
A . 用pH试纸测定溶液pH时,应先将试纸用蒸馏水润湿
B . 做蒸发溶液实验时,需要将蒸发皿中的溶液完全蒸干后再停止加热
C . 实验室制备气体时,装药品前要先检验装置的气密性
D . 进行过滤操作时,为加快速度,可以用玻璃棒搅拌漏斗内液体
甲、乙两种固体物质在水中的溶解度曲线如图所示。据图作答:

-
(1) 甲、乙两物质的溶解度受温度影响较大的是;在0℃~t1℃之间时,相同温度下甲物质的溶解度(填“>”“<”或“=”)乙物质的溶解度。
-
(2) t2℃时,把20g甲物质加入50g水中充分溶解,所得溶液为(填“饱和”或“不饱和”)溶液,把该溶液降温到t1℃时,会析出甲物质g。
如图所示,是甲、乙、丙三种固体物质的溶解度曲线.下列说法正确的是( )

A . t℃时,甲、乙、丙三种物质的饱和溶液的质量分数相等
B . 在两份相同质量的水中分别加入甲与丙,达到饱和时溶解甲的质量大于丙
C . 相同温度时,甲、乙、丙三种饱和溶液,其质量分数关系为:甲>乙>丙
D . 甲中混有少量丙时,可采用高温制成热的饱和溶液,再蒸发结晶提纯甲
硝酸钾和氯化钾的溶解度曲线如图所示。

-
(1) P点所表示的含义是。
-
(2) t1℃时,将20g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶度质的质量分数为。
-
(3) t3℃时,将接近饱和的硝酸钾溶液变为该温度下的饱和溶液,可以采用的方法是。
-
(4) 分别将100gt3℃的硝酸钾和氯化钾的饱和溶液降温至t2℃,过滤,得到硝酸钾的溶液a和氯化钾的溶液b。对于溶液a和溶液b,下列说法错误的是(填字母)
A 溶质的质量分数a=b
B 溶液质量a<b
C 溶质质量a=b
D 溶剂质量a<b
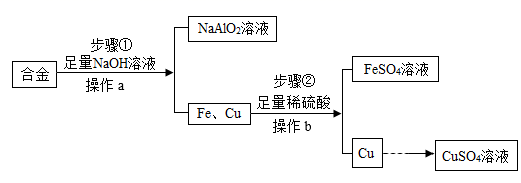
废旧共享单车应进行回收利用,下图是某工厂利用来自于回收单车的合金废料(含Fe、Cu和Al)制取FeSO4和CuSO4溶液的流程示意图(部分生成物已略):
-
(1) 实验室中操作a用到的玻璃仪器有烧杯、玻璃棒和。
-
(2) 在步骤①中,合金中的铝能和NaOH溶液中的溶质和溶剂反应生成 NaAlO2和一种可燃性气体,请写出其化学方程式为:。
-
(3) 判断步骤②中加入的稀硫酸足量的方法是。
-
(4) 由Cu制取 CuSO4溶液有以下两种途径:
Ⅰ、

Ⅱ、


你认为最佳途径是(填序号),理由是(写一点即可)。
A、B、C三种固体物质的溶解度曲线如图所示,请回答。

-
(1) A中混有少量的B,若要提纯A,可采取的结晶方法是。
-
(2) t2℃时,将三种物质的饱和溶液恒温蒸发等质量的水后,析出固体质量最多的是。
-
(3) t1℃时,取A、B、C固体各10g,分别加入三个烧杯中,再分别倒入100g水,充分搅拌后,能形成饱和溶液的是;将三个烧杯中的物质均升温至t3℃,此时,溶液中溶质质量分数的大小关系为。
净化天然水或除去物质中的杂质,都是利用混合在一起的不同物质性质之间的差异,将其分离。有时候,它们可能存在多种差异,我们要根据现实条件选择合适的方法,依据某种差异将他们分离开。说说看,我们学过了哪几种分离混合物的方法?它们各利用了物间的哪种差异?(至少写两种)
-
(1) ;。
-
(2) ;。
图中是a、b、c三种物质的溶解度曲线,回答下列问题。

-
(1) P点的含义:。
-
(2) 在t3℃时,将120g a物质加入到200g水中,充分溶解后所得到的溶液质量为g。
-
(3) b中混有少量a,提纯b的方法是(选填“蒸发结晶"或“降温结晶”)。
-
(4) 分别将t3℃时a、b的饱和溶液降温到t2℃析出晶体的质量大小关系为(选填一个序号)。
①a>b ②a<b ③a=b ④均有可能
下列说法中,正确的是( )
A . 合金、金刚石、不锈钢都是金属材料
B . 纯碱溶液呈碱性,所以属于碱类
C . 人体中含量最多的元素是氧元素
D . 微量元素在人体中可有可无
如图是氯化钠与硝酸钾的溶解度曲线,回答下列问题:

-
(1) 配置200g 0.9%的医用生理盐水,需要NaCl的质量为;
-
(2) 由图可知,℃时,硝酸钾和氯化钠的溶解度相等;
-
(3) 欲提纯混有少量氯化钠的硝酸钾固体,应采用的方法是。
如图甲、乙两种物质的溶解度曲线,下列说法正确的是( )

A . A点的甲溶液可通过蒸发溶剂加溶质制成饱和溶液
B . 乙是易溶物
C . 100℃时,甲、乙两溶液的溶质质量分数相同
D . 将90℃甲和乙的饱和溶液降温至20℃时,均成为饱和溶液
为探究硝酸钾的溶解性,进行了下图所示实验(实验过程)

结合硝酸钾在不同温度下的溶解度,判断下列说法错误的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 |
KNO3溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
A . ①③中的溶液均为不饱和溶液
B . ②③中溶液的质量:③>②
C . ②③④中溶液的溶质质量分数:③>②>④
D . ④中析出晶体的质量是0.9g
以下是KNO3和NaCl在不同温度时的溶解度和对应的溶解度曲线。请回答:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | |
-
(1) 代表KNO3溶解度曲线的是 (填“甲”或“乙”)。
-
(2) 若KNO3中混有少量NaCl,可采用 的方法提纯KNO3。
-
(3) t1的范围为____(填标号)。A.10~20A . 20~30 B . 30~40 C . 50~60
-
(4) t2℃时,将等质量的KNO3的饱和溶液和NaCl的饱和溶液分别降温到t1℃,所得溶液中溶质的质量m(KNO3) m(NaCl)(填“>”或“<”或“=”)。

如图硫酸钠的溶解度曲线,下列说法合理的是( )

A . 40℃时,硫酸钠的饱和溶液中溶质和溶液的质量比为1:3
B . 在0℃-70℃时,随着温度的升高,硫酸钠的溶解度变大
C . 70℃时,硫酸钠的饱和溶液在降温后一定还是饱和状态
D . 60℃时,将硫酸钠的饱和溶液降温至20℃,溶质质量分数先增大后减小
最近更新
- He’s making __________ great progress in his lessons that e
- There is a wonderful story about a young girl who had no fam
- 下列各纬度带人口数量最多的是 (
- 16.《论语》中“己所不欲,勿施于人”“己欲立而立人,己欲达而达人”,蕴含了丰富的人生智慧。请根据其中一句给你的启示,写
- 据台湾学者赵冈的研究,中国在唐宋两朝,大城市人口占到总人口比例的20%以上,而到1820年的晚清,竟只有6.9%。造成这
- 下列有关水的描述中不正确的是()A. 电解水时在正极产生氧气 B. 水是由氢原子和氧原子构成的 C. 可用肥皂水来区分硬
- 纳税人是直接向税务机关缴纳税款的单位和个人,负税人是实际负担税款的单位和个人。下列对应关系正确的是 ①李先生交纳1200
- 向下列各物质的水溶液中滴加稀硫酸或氯化镁溶液时,均有白色沉淀生成的是( ) A.氯化钡 B.氢氧化钡 C.碳酸钠 D.氢
- 设的内角所对的边长分别为,且,则_______
- 在1911年前后,新西兰出生的物理学家——卢瑟福把一束变速运动的α粒子(质量数为4的带2个正电荷的质子粒),射向一片极薄
- 抗日战争期间,湖北省政府曾发布《湖北省减租实施办法》,在农村推行以“减租”为内容的土地改革并取得一定成效,但未得到国民党
- 研究表明,受全球气候变暖影响,甘肃黄土高原的苹果开花期提前了14天左右,致使苹果的坐果率及品质有所下降。为此,在苹果生产
- _______, the middle-aged woman still keeps modest and never
- 对于地球的自转与公转描述正确的是() A.方向相同B.周期相同 C.自转产生的现象是四季变化D.公转产生的现象是昼夜交替
- 20世纪初,意大利经济学家基尼,根据洛伦茨曲线找出了判断分配平等程度的指标(如右图)。设实际收入分配曲线和收入分配绝对平
- Nowadays teens prefer going to the net-bar ______ they can
- 如图所示,质量为m电荷量为+q的小球用一绝缘细线悬于O点,开始时它在A、B之间来回摆动.OA、OB与竖直方向OC的夹角均
- 化学为人类社会的可持续发展做出了巨大贡献。 (1)家用太阳能发电设各与太阳能热水器一样,只要将一个太阳能板放在楼顶,就能
- 下列对所选古诗的理解和分析,不正确的两项是()( ) 闻王昌龄左迁龙标遥有此寄李白 杨花落尽子规啼,闻道龙标
- 精细陶瓷在现代科技中有广泛的应用,以SnO2和少量PbCl2研磨成极细的颗粒,经高温烧结成多孔体,具有半导体的性质并具有



