高考二轮复习知识点:化学键1
高考二轮复习知识点:化学键1
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 |
|
下列说法中正确的是( )
A . 丙烯分子中有8个σ键,1个π键
B . 60g的SiO2晶体中,含有4mol共价键
C . NCl3和BCl3分子,都是三角锥形
D . SiH4的沸点高于CH4 , 可推测PH3的沸点高于NH3
|
|
| 2. 综合题 | 详细信息 | ||||||||
|
CIGS靶材是一种主要含铜、铟(In)、镓(Ga)、硒(Se)的合金由于其良好的电学传导和光学透明性被广泛用于薄膜太阳能电池领域。回答下列问题:
|
|||||||||
| 3. 单选题 | 详细信息 |
|
氮氧化物(NOx)是一类特殊的污染物,它本身会对生态系统和人体健康造成危害。一种以沸石笼作为载体对氮氧化物进行催化还原的原理如图所示。下列叙述错误的是( )
A . 反应①变化过程可表示为2Cu(NH3)
 +O2=[(NH3)2Cu-O-O-Cu(NH3)2]2+
B . 反应③属于非氧化还原反应
C . 反应④涉及极性共价键的断裂与生成
D . 图中总过程中每吸收1molNO需要标准状态下的NH344.8L +O2=[(NH3)2Cu-O-O-Cu(NH3)2]2+
B . 反应③属于非氧化还原反应
C . 反应④涉及极性共价键的断裂与生成
D . 图中总过程中每吸收1molNO需要标准状态下的NH344.8L
|
|
| 4. 单选题 | 详细信息 |
|
下列物质中含有共价键的化合物的是( )
A . CaO
B . NaCl
C . H2
D . HCl
|
|
| 5. 单选题 | 详细信息 |
 可作为下列有机合成反应的催化剂。下列说法正确的是 ( ) 可作为下列有机合成反应的催化剂。下列说法正确的是 ( )
A .
 中σ键与π键的个数相等
B . 甲分子中采取 中σ键与π键的个数相等
B . 甲分子中采取 杂化的碳原子有6个
C . 有机物乙的沸点低于对羟基苯甲醛( 杂化的碳原子有6个
C . 有机物乙的沸点低于对羟基苯甲醛( 中 中 键比 键比 中 中 键易断裂 键易断裂
|
|
| 6. 综合题 | 详细信息 |
|
金属镍及其化合物在军工机械、生产生活中有着广泛的用途。
|
|
| 7. 单选题 | 详细信息 |
|
氮化硼(BN)晶体存在如图所示的两种结构。六方氮化硼的结构与石墨类似;立方氮化硼的结构与金刚石类似,可作研磨剂。
下列说法错误的是( )
A . 六方氮化硼层间的相互作用不属于化学键
B . 六方氮化硼可做润滑剂
C . 立方氮化硼晶胞中含有4个氮原子和4个硼原子
D . 立方氮化硼晶胞中,N和B之间不存在配位键
|
|
| 8. 综合题 | 详细信息 |
|
铀氮化合物是核燃料循环系统中的重要材料。
已知
|
|
| 9. 综合题 | 详细信息 |
|
许多元素及它们的化合物在科学研究和工业生产中具有多种用途。请回答下列有关问题:
|
|
| 10. 综合题 | 详细信息 |
|
碱土金属(IIA族)元素单质及其相关化合物的性质、合成一直以来是化学界研究的重点。回答下列问题:
|
|
高中化学 试卷推荐
- 广东、河南、湖南、湖北四省2020年高三联考模拟试卷
- 2016-2017学年北京市怀柔区高二上学期期末化学试卷
- 高中化学人教版 选修四 第四章 电化学基础 第三节 电解池 电解池第二课时(电解原理的应用)
- 2017年北京市丰台区高考化学二模试卷
- 天津市南开区2018-2019学年高二下学期化学期末考试试卷
- 安徽省宿州市埇桥区2018-2019学年高二(理)上学期化学期末考试试卷
- 广西桂林、贺州、崇左三市2017-2018学年高三理综-化学二模考试试卷
- 上海市静安区2017-2018学年高考理综-化学二模考试试卷
- 2015-2016学年浙江省金华市兰溪市兰荫中学高三上学期开学化学试卷
- 高中化学人教版 选修四 第四章 电化学基础 第四节 金属的电化学腐蚀与防护 金属的电化学腐蚀与防护
- 高中化学人教版(新课标)选修4 第二章第二节 影响化学反应速率的因素
- 云南省昆明市2017-2018学年高考理综-化学1月模拟考试试卷
最近更新
- 从以下诗句中选择三句,分别填入下面语段的横线上。(填字母序号即可) A.山寺桃花始盛开B.千叶桃花胜百花 C.红杏枝头春
- 社区将举行一场文艺演出,旨在弘扬中国传统文化。如果由你来担任这场文艺演出的 主持人,请你自己设计一段开场白。
- 考察正方体6个面的中心,甲从这6个点中任意选两个点连成直线,乙也从这6个点中任意选两个点连成直线,则所得的两条直线相互平
- 某兴趣小组同学对实验室制备氧气的条件进行如下探究实验. (1)为探究催化剂的种类对氯酸钾分解速率的影响,甲设计以下对比实
- 已知1既是与的等比中项,又是与的等差中项,则的值是( ) A、1或
- 下图为我国某一区域资源和能源分布图,图中实曲线为河流,B为特大城市,回答问题。A处每次截流都选在11月份的主要原因是(
- 如图为几种生物示意图,有关叙述错误的是()A.三种生物的繁殖方式一样B.①由蛋白质外壳和内部的遗传物质组成 C.②属于原
- In order to make students have a good knowledge of science s
- 对具有线性相关关系的两个变量y与x进行回归分析,得到一组样本数据(x1,y1),(x2,y2)…(xn,yn),则下列说
- 关于静电场的下列说法中,正确的是: A.电场强度的方向就是电荷所受电场力的方向 B.电场中某点的电场强度大小与试探电荷的
- 2010年11月16日,央行再次上调存款准备金率0.5个百分点。这是继2010年1月18日、2月25日、5月10日、10
- 制作洋葱鳞片叶内表皮细胞临时装片时,首先要在洁净的载坡片中央滴一滴 ( ) A.清水 B.生理盐水
- 美国历史学教授詹姆斯·麦佛森说:“如果这个国家可以分裂为两个,就可以分裂成3个、4个、6个、12个,林肯政府发动战争的理
- 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1m
- If you get lost, please call me ____010--55576760 or e---mai
- 紫色洋葱是生物学实验的常用材料,以下叙述不正确的是( ) A.观察质壁分离与复原,宜选取紫色外表皮细胞 B.观察有丝
- “工业革命的本质就是竞争替代了早先曾经控制了财富的生产和分配的中世纪管制。”对该观点理解最为准确的是
- 设,使是的必要但不充分条件的实数的取值范围是 A. B. C.
- 如图,在平面直角坐标系中,O为坐标原点,B(5,0),M为等腰梯形OBCD底边OB上一点,OD=BC=2,.(1)求直线
- 下列物质按单质、氧化物、化合物、混合物的顺序排列的是()A.金刚石、生石灰、粗食盐、冰水混合物 B.水银、干




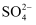 的空间构型为 ,EDTA中碳原子杂化方式为 。
的空间构型为 ,EDTA中碳原子杂化方式为 。



 与丁二酮肟生成鲜红色丁二酮肟镍沉淀,该反应可用于检验
与丁二酮肟生成鲜红色丁二酮肟镍沉淀,该反应可用于检验
 杂化,为平面正方形构型,则该分子中共面的原子最多为个。
杂化,为平面正方形构型,则该分子中共面的原子最多为个。 、
、 等。
等。 键与
键与 键数目之比为。
键数目之比为。 分子中键角略大,其原因是。
分子中键角略大,其原因是。 在氨水中可生成一种淡紫色苯包合沉淀物,苯分子位于晶胞的体心且2个碳碳
在氨水中可生成一种淡紫色苯包合沉淀物,苯分子位于晶胞的体心且2个碳碳 键长为
键长为 ,
,  键长为
键长为 。
。

 。回答下列问题:
。回答下列问题: 形成配离子的是,解释原因。
形成配离子的是,解释原因。
 , 则处于下列状态的铀原子或离子失去一个电子所需能量最高的是____(填标号)。
, 则处于下列状态的铀原子或离子失去一个电子所需能量最高的是____(填标号)。




 的空间构型为,其结构中存在大π键,可表示为(用
的空间构型为,其结构中存在大π键,可表示为(用 表示,m代表参与形成大
表示,m代表参与形成大 , U原子半径为
, U原子半径为 , N原子半径为
, N原子半径为 , 设
, 设 为阿伏加德罗常数的值,则该晶胞的空间利用率为(用含d、
为阿伏加德罗常数的值,则该晶胞的空间利用率为(用含d、 、
、 、
、
 、-CH3、CH
、-CH3、CH 都是重要的有机反应中间体。CH
都是重要的有机反应中间体。CH 。分子中的大π键可用符号π
。分子中的大π键可用符号π 表示。其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示。其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π )。咪唑分子中的大π键可表示为,咪唑比环戊烯C5H8熔点高的主要原因是。
)。咪唑分子中的大π键可表示为,咪唑比环戊烯C5H8熔点高的主要原因是。
 中孤电子对与π键比值为,碳原子的杂化方式为。
中孤电子对与π键比值为,碳原子的杂化方式为。


 取1.73)。
取1.73)。


