高考二轮复习知识点:中和滴定5
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L﹣1的三种酸(HA、HB和HD)溶液,滴定曲线如图所示,下列判断错误的是( )
A . 三种酸的电离常数关系:KHA>KHB>KHD
B . 滴定至P点时,溶液中:c(B﹣)>c(Na+)>c(HB)>c(H+)>c(OH﹣)
C . pH=7时,三种溶液中:c(A﹣)=c(B﹣)=c(D﹣)
D . 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH﹣)﹣c(H+)
|
|
| 2. 单选题 | 详细信息 |
|
下列图示与对应的叙述不相符合的是( )
A . 图甲表示燃料燃烧反应的能量变化
B . 图乙表示酶催化反应的反应速率随反应温度的变化
C . 图丙表示弱电解质在水中建立电离平衡的过程
D . 图丁表示强碱滴定强酸的滴定曲线
|
|
| 3. 单选题 | 详细信息 |
|
NaOH溶液滴定盐酸实验中,不必用到的是( )
A . 酚酞
B . 圆底烧杯
C . 锥形瓶
D . 碱式滴定管
|
|
| 4. 单选题 | 详细信息 |
|
室温下,用0.100mol•L﹣1 NaOH溶液分别滴定20.00mL 0.100mol•L﹣1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
A . Ⅱ表示的是滴定醋酸的曲线
B . pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
C . V(NaOH)=20.00mL时,两份溶液中c(Cl﹣)=c(CH3COO﹣)
D . V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)
|
|
| 5. 实验探究题 | 详细信息 |
|
(15分)水中溶解氧是水生生物生存不可缺少的条件.某课外小组采用碘量法测定学校周边河水中的溶解氧.实验步骤及测定原理如下:
Ⅰ.取样、氧的固定 用溶解氧瓶采集水样.记录大气压及水体温度.将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2 , 实现氧的固定. Ⅱ.酸化,滴定 将固氧后的水样酸化,MnO(OH)2被I﹣还原为Mn2+ , 在暗处静置5min,然后用标准Na2S2O3溶液滴定生成的I2(2S2O32﹣+I2=2I﹣+S4O62﹣). 回答下列问题:
|
|
| 6. 综合题 | 详细信息 |
|
由废铁制备FeCl2并测定FeCl2的含量。主要过程如下所示:
|
|
| 7. 单选题 | 详细信息 |
|
用一定浓度 NaOH 溶液滴定某醋酸溶液。滴定终点附近溶液 pH 和导电能力的变化分别如下图所示(利用溶液导电能力的变化可判断滴定终点;溶液总体积变化忽略不计)。下列说法不正确的是( )
A . a 点对应的溶液中:c(CH3COO-) = c(Na+)
B . a→b 过程中,n(CH3COO-)不断增大
C . c→d 溶液导电性增强的主要原因是 c(OH-)和 c(Na+)增大
D . 根据溶液 pH 和导电能力的变化可判断:V2<V3
|
|
| 8. 综合题 | 详细信息 |
|
亚硝酰氯(ClNO)是有机物合成中的重要试剂,其沸点为-5.5℃,易水解。已知:AgNO2微溶于水,能溶于硝酸,AgNO2+HNO3=AgNO3 +HNO2 , 某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度,相关实验装置如图所示。
|
|
| 9. 单选题 | 详细信息 |
|
已知 pOH=-lgc(OH-)。向20 mL 0.1 mol·L-1 的氨水中滴加未知浓度的稀 H2SO4 , 测得混合溶液的温度、pOH随加入稀硫酸体积的变化如下图所示,下列说法不正确的是( )
A . 稀H2SO4 的物质的量浓度为0.05 mol·L-1
B . 当溶液中pH=pOH时,水的电离程度最大
C . a点时溶液中存在c(NH3·H2O)+2c(OH-)=c(NH
 )+2c(H+)
D . a、b、c 三点对应 NH )+2c(H+)
D . a、b、c 三点对应 NH  的水解平衡常数:Kh(b)>Kh(a)>Kh(c) 的水解平衡常数:Kh(b)>Kh(a)>Kh(c)
|
|
| 10. 单选题 | 详细信息 |
|
在25mL0.1mol•L﹣1某一元碱中,逐滴加入0.1个mol•L﹣1醋酸,滴定曲线如图所示。则下列说法不正确的是( )
A . 该碱溶液可以溶解Al(OH)3
B . a点对应的体积值大于25mL
C . C点时,c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣)
D . D点时,c(CH3COO﹣)+c(OH﹣)=c(H+)+c(CH3COOH)
|
|
- 2018年高考化学真题分类汇编专题03:常用化学计量
- 2016年高考化学真题试卷(上海卷)
- 高中化学人教版(新课标)必修1 第四章测试题
- 山东省淄博市2017-2018学年高考理综-化学二模考试试卷
- 2015年天津市七校联考高考化学模拟试卷(4月份)
- 2015-2016学年浙江省宁波市奉化中学高一上学期月考化学试卷(10月份)
- 四川省资阳市2013-2014学年高二下学期化学期末考试试卷
- 内蒙古自治区赤峰市宁城县2018-2019学年高二上学期化学期末考试试卷
- 高中化学人教版(2019)必修第二册 第七章第四节 基本营养物质
- 高中化学人教版(新课标)选修4 第二章第三节 化学平衡
- 山东省潍坊市2020年高考化学二模试卷
- 浙江省名校协作体2020年高考理综-化学二模试卷
- 下列生活中的现象,可用分子的知识加以解释。其中不正确的是A.电解水的实验说明在化学变化中分子可以再分B.空气能被压入足球
- 14.下列各句中,没有语病的一句是( )(3分) A.现代文明不仅带来了理性化、工业化、市场化、都市化、民主化和法
- 1998年发射的“月球勘测者号”空间探测器,运用最新科技手段对月球进行近距离勘探,在研究月球磁场分布方面取得新的成果.月
- 对于一条线性回归直线=a+bx,如果x=3时,对应的y的估计值是17,当x=8时,对应的y的估计值是22,那么,可以估计
- 装品牌苏打饼干的配料和营养成分如下表,研究性学习小组対其成分进行了探究。 配料 营养成分(每100g) 小麦粉,食用植物
- 【函函游园记】函函早晨到达上海世博园D区入口处等待开园,九时整开园,D区入口处有10n条安全检查通道让游客通过安检入园,
- 蜥蜴和蛇等爬行动物的体表具有角质的鳞片或甲,这有利于 A.自由运动 B.协助呼吸 C.减少体内水分蒸发 D.保持体温
- 历代盛行的官营作坊,在明清时期受到冲击。江南城镇附近农户不事农耕,“尽逐绫绸之利”,渐成风尚,城镇中“络玮机杼之声通宵彻
- 北京奥运会“渊源共生,和谐共融”的“祥云”火炬,燃料为丙烷,其主要含有碳和氢两种元素,燃烧后只有二氧化碳和水,没有其他物
- 如图所示,兔子和乌龟在全程为12m的赛跑比赛中,兔子跑到树下用时10s,在树下睡觉用 时20s,醒来之后才发现乌龟刚好到
- 一个多边形的外角和与它的内角和相等,则多边形是( ) A.三角形
- 根据提示, 利用本单元所学知识, 完成下面的小作文。 1. 随着广告业的发展, 人们从广告中受益更多, 尤其是年轻人。(
- 美国及日本两个研究团队的报告中证实皮肤细胞经过“基因直接重组”后可以转化成为具有胚胎干细胞特性的细胞。这项发现解决了利用
- 2009年11月28日,宁西铁路西安至合肥增建第二线工程正式开工建设。此次开工建设的是宁西铁路西安至合肥952千米增建第
- 右图为某地实景图,读图回答下面两题。32. 该地质构造为 A.背斜 B.向斜C. 地垒 D.地堑 3
- (09年济南市期末)某人在静止的湖面上某高度处竖直上抛一个铁球,铁球上升到最高点后自由下落,穿过湖水并陷入湖底的淤泥中一
- 9.对下面句子所对应的人物判断不正确的一项是 A.千古诗人,蓬莱文章建安骨;一身傲气,青莲居士谪仙人。(白居易) B.何
- 在中,,,,,设,则的取值范围是 .
- 完成光路图。
- 根据短文内容和所给中文提示,写出空白处各单词的适当形式,每空限填一词。 George Stephenson was bo




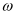 (FeCl2) (g/L) =kV(式中V——消耗的酸性高锰酸钾标准溶液的毫升数),则k=(保留四位有效数字)。
(FeCl2) (g/L) =kV(式中V——消耗的酸性高锰酸钾标准溶液的毫升数),则k=(保留四位有效数字)。








