山东省潍坊市2020年高考化学二模试卷
山东省潍坊市2020年高考化学二模试卷
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
高分子材料在疫情防控和治疗中起到了重要的作用。下列说法正确的是( )
A . 聚乙烯是生产隔离衣的主要材料,能使酸性高锰酸钾溶液褪色
B . 聚丙烯酸树脂是3D打印护目镜镜框材料的成分之一,可以与NaOH溶液反应
C . 天然橡胶是制作医用无菌橡胶手套的原料,它是异戊二烯发生缩聚反应的产物
D . 聚乙二醇可用于制备治疗新冠病毒的药物,聚乙二醇的结构简式为
|
|
| 2. 单选题 | 详细信息 |
|
曲酸和脱氧曲酸是非常有潜力的食品添加剂,具有抗菌抗癌作用,其结构如图所示。下列叙述错误的是( )
A . 两物质都能使溴的四氯化碳溶液褪色
B . 曲酸经消去反应可得脱氧曲酸
C . 1mol脱氧曲酸最多能与3molH2发生加成反应
D . 曲酸与脱氧曲酸中含有相同种类的官能团
|
|
| 3. 单选题 | 详细信息 |
|
用化学沉淀法去除粗盐中的杂质离子,包括粗盐溶解、加沉淀剂、过滤、调节pH、蒸发结晶等步骤。下列说法错误的是( )
A . 沉淀剂的添加顺序可以是NaOH溶液、BaCl2溶液、Na2CO3溶液
B . 向滤液中滴加盐酸,调节pH至滤液呈中性
C . 蒸发结晶时,当蒸发皿中出现较多固体时,停止加热,利用余热将滤液蒸干
D . 溶解、过滤、蒸发结晶等过程都使用玻璃棒搅拌溶液
|
|
| 4. 单选题 | 详细信息 |
|
最新发现C3O2是金星大气的成分之一,化学性质与CO相似。C3O2分子中不含环状结构且每个原子均满足8电子稳定结构。下列叙述错误的是( )
A . 元素的第一电离能:O>C
B . 3p轨道上有1对成对电子的基态X原子与基态O原子的性质相似
C . C3O2中C原子的杂化方式为sp3
D . C3O2分子中σ键和π键的个数比为1:1
|
|
| 5. 单选题 | 详细信息 |
|
芘经氧化后可用于染料合成。芘的一种转化路线如下:
下列叙述正确的是( )
A . 芘的一氯代物有4种
B . 甲分子中所有碳原子一定都在同一平面上
C . 1mol乙与足量NaOH溶液反应,最多消耗2molNaOH
D . 甲催化氧化后,再发生酯化反应也能得到乙
|
|
| 6. 单选题 | 详细信息 |
|
短周期主族元素X、Y、Z、W的原子序数依次增大。Z原子2p轨道上有3个未成对电子。甲、乙、丙、丁、戊是这四种元素之间形成的化合物,75%的甲溶液常用于消毒,戊是Z和X组成的10电子分子,常温下己溶液显中性,它们有如下转化关系:
则下列说法中错误的是( )
A . 四种元素原子半径由大到小的顺序为:Y>Z>W>X
B . W的氢化物中的某一种具有漂白性
C . 丙的电子式为
 D . W的氢化物沸点一定比Y的氢化物沸点高
D . W的氢化物沸点一定比Y的氢化物沸点高
|
|
| 7. 单选题 | 详细信息 |
|
SiO2是合成“中国蓝”的重要原料之一。如图是SiO2晶胞中Si原子沿z轴方向在xy平面的投影图(即俯视投影图,O原子略去。),Si原子旁标注的数字是Si原子位于z轴的高度,则SiA与SiB的距离是( )
A .
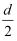 B .
B . 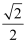 d
C . d
C . 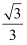 d
D . d d
D . d
|
|
| 8. 单选题 | 详细信息 | |||||||||||||||
|
根据下列实验操作和现象能得到相应结论的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 9. 单选题 | 详细信息 |
|
铋酸钠(NaBiO3) 是分析化学中的重要试剂,不溶于冷水,遇沸水或酸则迅速分解。某化学兴趣小组设计下图实验装置制取铋酸钠。装置丙中盛有Bi(OH)3(难溶于水) 与NaOH溶液混合物。下列说法错误的是( )
A . 装置乙中盛装的试剂是饱和食盐水
B . 装置丙中发生反应的离子方程式是:Bi(OH)3+3OH-+Na++Cl2=NaBiO3+2Cl-+3H2O
C . 从装置丙中获得产品的操作为:在冰水中冷却结晶、过滤、洗涤、干燥
D . 为除去所得固体中混有的Bi(OH)3 , 可用稀盐酸洗涤
|
|
| 10. 单选题 | 详细信息 |
|
金属铬(Cr) 常用于制造不锈钢和仪器仪表的金属表面镀铬。由FeCr2O4 , (亚铬酸亚铁)制备Cr的流程如下(+6价铬元素在酸性条件下以Cr2O72-的形式存在)。下列说法错误的是( )
A . FeCr2O4中Cr元素的化合价为+3价
B . 反应①中参加反应的FeCr2O4和Na2CO3的物质的量之比为3:1
C . 反应③的化学方程式为Na2Cr2O7+2C
 Cr2O3+Na2CO3+CO↑
D . 反应④中的Si可用Al来代替 Cr2O3+Na2CO3+CO↑
D . 反应④中的Si可用Al来代替
|
|
高中化学 试卷推荐
- 江苏省扬州市2015-2016学年高一下学期化学期末考试试卷
- 备考2018年高考化学二轮专题复习 专题15:无机化工流程题
- 山东省菏泽市2017-2018学年高二上学期化学期中考试试卷(B)
- 吉林省公主岭市2018-2019学年高二上学期化学期末考试试卷
- 2015-2016学年湖北省襄阳市保康一中高一下学期第一次月考化学试卷
- 江苏省苏州市2019-2020学年高二下学期化学期末考试试卷
- 北京四中2017-2018学年高二上学期化学期中考试试卷
- 广东省佛山市2018-2019学年高考理综-化学一模考试试卷(1月)
- 高中化学人教版(2019)选择性必修1 第四章第一节 原电池
- 河北省邯郸市2017-2018学年高一上学期化学期中考试试卷
- 河北省邢台市2017-2018学年高三上学期理综-化学期末考试试卷
- 天津市五区县2016-2017学年高一上学期化学期末考试试卷
最近更新
- 一个自由下落的物体,前3s内下落的位移是第1s内下落位移的( ) A.2倍 B.3倍
- 17.古诗词鉴赏 送彭将军 郎士元 双旌汉飞将,万里独横戈。 春色临边尽,黄云出塞多。 鼓鼙悲绝漠,烽戍隔长河。 莫断阴
- ___ John like chicken _____ fish? A. Does ;and B. Do;fo
- 下列实验方案中,能达到实验目的的是 () 选项 实验目
- |-5|-(-2)×+(-6)
- 哺乳动物的运动只靠运动系统来完成。 ( )
- 热机是将内能转化成 ___能的机器;热机一个工作循环由______个冲程组成,其中如图所示是热机的__________冲
- The simple joy of reading is something we take for granted.
- Not only ______interested in football but ______beginning to
- 下列各项中翻译不恰当的一项是:( ) A.外无期功强近之亲,内无应门五尺之童;茕茕独立,形影相吊。 在外面没有建功立业的
- 已知代数式的值为,则的值为 .
- 大熊猫的学名是 Ailuropoda melanoleuca,其中 Ailuropoda 和 melanoleuca 分
- 范缜与竟陵王萧子良辩论的本质是 : A.儒学与佛学的斗争 B.世俗地主与僧侣地主的斗争C.唯物论与唯心论的斗争 D
- He has left his book here on _____, so that you can read it.
- 下图是某细胞在进行某项生命活动前后几种生物膜面积的变化,在此变化过程中最可能合成的是
- 在水平面上,小猴拉着小滑块做匀速圆周运动,O点为圆心,能正确地表示小滑块受到的牵引力F及摩擦力Ff的图是(
- 基因型为ddEeFf和DdEeff的两亲本杂交: (1)其子代基因型为亲本类型的概率 ,重组类型的
- 下列是实验室制取气体和收集气体的实验装置,根据装置图回答问题. (1)实验室用氯酸钾与二氧化锰制取氧气,分数装置应选择(
- 某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将56.0L混合
- 下列各组语句中加点的虚词,意义、用法都相同的一项是( )A.作《师说》以遗之臣以险衅,夙遭闵凶。B.尝为晋君赐矣




 2Fe2++I2
2Fe2++I2




