【备考2024年】高考化学全国乙卷真题变式分层精准练第9题
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
乙醇俗称酒精,在生活中使用广泛。
资料1:乙醇分子有两个末端,一端是憎水(易溶于油)的—C2H5;一端是亲水(易溶于水)的—OH。 资料2:破坏蛋白质分子中形成蜷曲和螺旋的各种力,使长链舒展、松弛,可导致蛋白质变性。 资料3:水分子可以松弛蛋白质外部亲水基团之间的吸引力,而-OH不能;—C2H5可以破坏蛋白质内部憎水基团之间的吸引力。
|
|
| 2. 综合题 | 详细信息 |
|
铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
|
|
| 3. 综合题 | 详细信息 |
|
在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一,氰酸盐进一步被氧化为无毒物质。
|
|
| 4. 单选题 | 详细信息 |
|
部分常见含氯物质的分类与相应化合价关系如图所示。下列推断不合理的是 ( )
A .
 既可被氧化,也可被还原
B . 既可被氧化,也可被还原
B .  的浓溶液可与 的浓溶液可与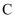 的固体反应生成 的固体反应生成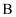 与 与 C . 实验室可通过加热
C . 实验室可通过加热 与 与 的浓溶液制得 的浓溶液制得 D . 可存在
D . 可存在 的循环转化关系 的循环转化关系
|
|
| 5. 综合题 | 详细信息 |
|
氯碱工业是高能耗产业,节能技术的研发是当前的重要课题。
|
|
| 6. 综合题 | 详细信息 |
|
根据所学知识回答下列有关问题。
|
|
| 7. 综合题 | 详细信息 |
|
|
| 8. 单选题 | 详细信息 |
|
关于化工生产,下列说法错误的是( )
A . 工业常用电解饱和食盐水的方法来制取氯气
B . 硫酸工业在常压下用SO2与O2反应制取SO3
C . 联合制碱法、氨碱法所需的CO2都来自石灰石的分解
D . 通常以海带、紫菜等为原料提取碘
|
|
| 9. 综合题 | 详细信息 | ||||||||||||||||||||
三氯化铬(
|
|||||||||||||||||||||
|
|
在不同温度下的反应现象 |
|
|
25℃ |
90-100℃ |
|
|
1 |
紫红色 |
蓝绿色溶液 |
|
2~9 |
紫红色 |
黄绿色溶液,且随 |
|
10 |
紫红色 |
澄清的橙黄色溶液 |
|
11~23 |
紫红色 |
橙黄色溶液,有棕褐色沉淀,且随 |
|
24~25 |
紫红色 |
紫红色溶液,有较多的棕褐色沉淀 |
①温度对反应的影响。
 与
与 在常温下反应,观察不到
在常温下反应,观察不到 离子的橙色,甲同学认为其中一个原因是
离子的橙色,甲同学认为其中一个原因是 离子的橙色被
离子的橙色被 离子的紫红色掩盖,另一种可能的原因是,所以必须将反应液加热至沸腾4~5min后,才能观察到反应液由紫红色逐渐变为橙黄色的实验现象。
离子的紫红色掩盖,另一种可能的原因是,所以必须将反应液加热至沸腾4~5min后,才能观察到反应液由紫红色逐渐变为橙黄色的实验现象。
② 与
与 的用量对反应的影响。
的用量对反应的影响。
对表中数据进行分析,在上述反应条件下,欲将 氧化为
氧化为 ,
,  与
与 最佳用量比为。这与由反应
最佳用量比为。这与由反应 所推断得到的用量比不符,你推测的原因是。
所推断得到的用量比不符,你推测的原因是。
| 10. 综合题 | 详细信息 |
我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下(部分物质已略去)。
已知:氨气极易溶于水,无水氯化钙可与
|
|
- 2015年湖南省长沙市高考化学模拟试卷(4月份)
- 第9讲:碳族元素 无机非金属材料
- 广西靖西市第二中学2019-2020学年高二下学期化学开学考试卷
- 内蒙古包头市2020年高考化学一模试卷
- 北京市西城区2015-2016学年高一上学期化学期末考试试卷
- 安徽省合肥市2019-2020学年高二下学期化学开学考试卷
- 辽宁省阜新市第二高级中学2019-2020学年高一下学期化学期末考试试卷
- 天津市红桥区2020年高考化学二模试卷
- 天津市和平区2017-2018学年高三上学期化学期末考试试卷
- 广东省惠州市2018-2019学年高一上学期化学期末考试试卷
- 高中化学人教版(2019)必修第一册 第二章第三节 物质的量
- 四川省凉山彝族自治州2019-2020学年高一下学期化学期末考试试卷
- 如图所示圆形区域内,有垂直于纸面方向的匀强磁场,一束质量和电荷量都相同的带电粒子,以不同的速率,沿着相同的方向,对准圆心
- 用氯气消毒过的自来水配制下列溶液时,会使所配的溶液的溶质发生变化的是( ) ①NaOH ②AgNO3 ③Na2
- 下列说法正确的是() A.缺乏维生素A会引起坏血病 B.缺铁会引起甲状腺肿 C.大米富含糖类 D.蔬菜中含大量蛋白质
- 下图为A、B两种物质间的转化关系(其中C、D是反应物,部分产物已省略)。以下判断不正确的是() A.若A是AlCl3,则
- (09年冀州中学期末)(9分)用如图所示的电路测定一节电动势约为2V的蓄电池的电动势和内阻。因蓄电池内阻非常小,为防止调
- A 、 B 、 C 、 D 都是中学化学中常见物质,其中 A 、 B 、 C 均含有同一种元素,在一定条件下相互转化关系
- 请以“如何学好英语”为题,写一篇议论文。主要内容如下: (1)要学好英语,应该坚持不断地使用英语。 (2)语法是
- 某肉联厂在鲜肉表面涂抹白色粉末A以延长保持时间.小新进行了如下实验,探究化合物A的化学组成. 【定性研究】步骤 实验操作
- 依次填入下面空白处的词语,最恰当的一组是() ①“2010CCTV形象中国·非常自我造型·形象代言人选拔大赛”将在湖南拉
- (赣州市)下列词语中没有错别字的一组是( )A.平心而论 汗流浃背 大材小用 吃闭门羹B.以逸待劳
- 基因型为Aa与基因型为Bb的动物体细胞混合用灭活的仙台病毒处理后,不可能获得下列哪种基因型的细胞 A.Aaaa
- 下列说法中不正确的是 A.20gD2O(重水)的物质的量1mol. B.黄铜合金(铜、锌)的熔点比铜高. C.玻璃、水泥
- 一架在北半球飞行的飞机,飞越晨昏线上空时,当地为8日5时。据此回答。在图所示的4个地区中,它飞越的是 A、① B、②
- (09年广东历史)《中华民国临时约法》确立了 A.总统制 B. 联邦制 C. 君主立宪制 D
- 某公园门票价格规定如下表:购票张数 1`50张 51~100张 100张以上 每张票的价格 13元 11元 9元 购票张
- 对于可逆反应A(g) + 3B(g) 2C(g),在不同条件下的化学反应速率如下,其中表示反应速率最快的是
- 为缓解北京地区的旱情,有关部门选择适宜的条件和方法,向大气中发射催雨剂,其主要成分是干冰、液氨、碘化银等。下列有关叙述不
- (4分)某学生进行蔗糖水解的实验,并检验水解产物中是否含有葡萄糖。它的操作如下:①取少量蔗糖加适量水配成溶液②在蔗糖溶液
- 如图所示,水平桌面上有一轻弹簧,左端固定在A点,自然状态时其右端位于B点。D点位于水桌面最右端,水平桌面右侧有一竖直放置
- 已知点(,),椭圆:的离心率为,是椭圆的右焦点,直线的斜率为,为坐标原点. (Ⅰ)求的方程; (Ⅱ)设过点的斜率为的直线





 的化学性质与金刚石(填“相似”或“不同”),
的化学性质与金刚石(填“相似”或“不同”), 完全燃烧时需要消耗
完全燃烧时需要消耗 , 该反应会(填“吸收”或“释放”)能量。
, 该反应会(填“吸收”或“释放”)能量。
 +3Cl-+5H2O。用
+3Cl-+5H2O。用 和
和 在高温下制备无水三氯化铬,部分实验装置如图所示,其中三颈烧瓶内装有
在高温下制备无水三氯化铬,部分实验装置如图所示,其中三颈烧瓶内装有
 , 其目的是排尽装置中的空气,在实验过程中还需要持续通入
, 其目的是排尽装置中的空气,在实验过程中还需要持续通入 ),B中反应的化学方程式为。
),B中反应的化学方程式为。 )转化为铬酸钠(
)转化为铬酸钠( ),加入过量
),加入过量 , 再加入10%HCl溶液,可以看到有气泡产生。写出用
, 再加入10%HCl溶液,可以看到有气泡产生。写出用 溶液,并用4滴
溶液,并用4滴 酸化,再分别加入不同滴数的0.1mol/L
酸化,再分别加入不同滴数的0.1mol/L
 反应生成固体
反应生成固体 。
。 ”或“
”或“



