高中化学人教版(2019)选择性必修1第四章第一节原电池
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 填空题 | 详细信息 |
|
原电池是一种将转变为的装置。电子的流动方向是从电源的极通过外电路流到电源的极。电工操作中规定,不能把铜线和铝线拧在一起连接线路,这是因为在潮湿的空气中,铜与铝接触形成原电池,其中铝做极,很快被腐蚀。
|
|
| 2. 填空题 | 详细信息 |
|
在银锌原电池中,以硫酸铜为电解质溶液:
锌为极,电极上发生的是反应(“氧化”或“还原”)电极反应式为;银电极电极反应式是;银片上观察到的现象是。 |
|
| 3. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||||
|
某同学在用稀硫酸与锌粒制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
|
|||||||||||||||||||||||||||||
| 4. 填空题 | 详细信息 |
|
某原电池装置如图所示。其中,Zn电极为原电池的极(填“正”或“负”),电极反应式是。Cu电极上发生的反应属于(填“氧化”或“还原”)
反应。
|
|
| 5. 填空题 | 详细信息 |
|
新冠肺炎最明显的症状就是出现发热,体温枪能快速检测人体体温。该体温枪所用的电池为一种银锌电池(如下图所示),该电池的总反应式为:Zn+Ag2O+ H2O=Zn(OH)2+
2Ag。
回答下列问题: ①在测体温时,电池将 转化为(填“化学能”或“电能”) 。 ②电池中电子的流向:由 到(填化学式),负极的电极反应式为。 |
|
| 6. 填空题 | 详细信息 |
|
在原电池中,较活泼的金属极上发生,是极;较不活泼的金属极上发生,是极。
|
|
| 7. 推断题 | 详细信息 |
|
从化合价和物质类别两个视角认识元素及其化合物性质是重要的化学学习方式。图1是Fe及其化合物的化合价~物质类别二维图。
回答下列问题:
|
|
| 8. 实验探究题 | 详细信息 |
|
研究化学反应中的能量变化,能更好地利用化学反应为生产和生活服务。
|
|
| 9. 实验探究题 | 详细信息 |
|
|
| 10. 推断题 | 详细信息 |
|
A、B、D、E、F、G为短周期元素,且原子序数依次增大。A、F同主族,E、G同主族。A与其他非金属元素化合时易形成共价键,F与其他非金属元素化合时易形成离子键,且
 与 与  核外电子排布相同。由以上元素组成的物质 核外电子排布相同。由以上元素组成的物质  和 和  具有相同的电子数。回答下列问题: 具有相同的电子数。回答下列问题:
|
|
- 2016-2017学年湖南省株洲市茶陵三中高二上学期开学化学试卷
- 云南省保山市2018-2019学年高考理综-化学检测考试试卷
- 天津市耀华中学2019-2020学年高三下学期化2月月考试卷
- 山西省运城市芮城县2019-2020学年高二下学期化学期末考试试卷
- 吉林省四平市双辽市第二中学2019-2020学年高二上学期化学期末考试试卷
- 江西省宜春市2018-2019学年高三上学期化学期末考试试卷
- 浙江省名校协作体(G12)2018-2019学年高二下学期化学期末考试试卷
- 四川成都田家炳中学2018-2019学年高一上学期化学12月月考试卷
- 2017年高考理综真题试卷(化学部分)(北京卷)(正式版)
- 2019年高考理综化学真题试卷(北京卷)
- 山东省临沂市2016-2017学年高一上学期化学期末考试试卷
- 人教版化学高二选修2第四单元课题2表面活性剂 精细化学品同步练习
- 下列属于世界文化遗产的是:( ) A.长江三峡水电站 B.重庆永川大佛寺 C.重庆大
- 默写,请在横线上补写所引诗文的句子.(两组中只选做一组)(共5分) (1)①看万山红遍,层林尽染; ,
- Experts warn that global warming will cause dramatic climate
- 近年来,我国商品房价格持续上涨,引起了社会各界的关注。为此国务院常务会议专门讨论并通过了六条意见,从房价、土地供应、供应
- Four Habits to Help you Succeed We all want to succeed, whet
- 中国古代有避讳制度,要避免使用本朝帝王的名字,遇有相同的字时,必须改用其他字。下列各项中属于这种情况的是 A.汉初改“相
- 下图为哺乳动物(或人体)神经和激素分泌的调节过程。请据图回答问题:(1)下丘脑参与内环境水分平衡调节的途径是(用数字和箭
- 如图,在直角坐标系中,已知点,,对△连续作旋转变换,依次得到三角形①、②、③、④…,则三角形⑦的直角顶点的坐标为
- 若实数、、满足,则称比远离.(1)若比远离0,求的取值范围; (2)对于任意两个不相等的正数、,证明:比远离; (3)已
- 图4表示我国能源生产总量、消费总量重心在经度和纬度上的变化,读图回答下面试题。 关于我国能源生产总量、消费总量重心的正确
- 设集合,则集合( ) A B C D
- 种植作物常施肥,控制无机盐进入根细胞的结构是( )A. 细胞壁 B. 细胞膜 c. 细胞核 D. 细胞
- 他是晚清状元,主张实业救国,中日甲午战争后,他愤而辞官从商,创办了大生纱厂等一系列民族资本主义企业。这位中国近代民族工商
- 一次函数y=kx+4的图象过点(﹣1,7). (1)求k的值;(2)判断点(a,﹣3a+4)是否在该函数图象上,并说明理
- 现有A、B、C、D、E五种元素,都是短周期元素,其中A、B、C原子序数依次递增并都相差1。B的阳离子的电子层结构与Ne原
- 被后人称为“美国宪法之父”的麦迪逊说:“如果人都是天使,就不需要任何政府了。如果是天使统治人,就不需要对政府有外来的或内
- 一个长方形的三个顶点坐标为(―1,―1),(―1,2)(3,―1),则第四个顶点的坐标是______________
- 已知100到999的三位数,求其中含有0的三位数有多少?
- 下列离子方程式书写正确的是 ( ) A. 酸性FeCl2溶液中加入双氧水:2Fe2++H2O2=2Fe3
- 和平与发展是当今世界的两大主题,政治多极化,经济全球化,区域一体化的进程在加快,国家间的竞争更多地表现为综合国力的竞争。





 可以去除水体中的
可以去除水体中的  (原理如图2)。若有1mol
(原理如图2)。若有1mol  ,则参加反应的
,则参加反应的 
 的能量变化如图所示。
的能量变化如图所示。 

 的硫酸溶液、导线和
的硫酸溶液、导线和  量筒设计实验,证明形成原电池可以改变反应速率所用装置如图所示,装置气密性良好,且
量筒设计实验,证明形成原电池可以改变反应速率所用装置如图所示,装置气密性良好,且 
 (已折算为标准状况,且溶液体积不变)气体时,用时
(已折算为标准状况,且溶液体积不变)气体时,用时  ,则用
,则用 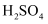 表示的平均反应速率为
表示的平均反应速率为  。
。 。
。
 的电子式为,含有化学键(填“离子键”或“共价键”)。
的电子式为,含有化学键(填“离子键”或“共价键”)。




