天津市耀华中学2019-2020学年高三下学期化2月月考试卷
天津市耀华中学2019-2020学年高三下学期化2月月考试卷
教材科目:化学
试卷分类:高三下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高三下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
对于反应2N2O5(g)→4NO2(g)+O2(g),R.A.Ogg提出如下反应历程:
第一步 N2O5⇌NO3+NO2快速平衡 第二步 NO2+NO3→NO+NO2+O2慢反应 第三步 NO+NO3→2NO2快反应 其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是( )
A . v(第一步的逆反应) < v(第二步反应)
B . 反应的中间产物只有NO3
C . 第二步中NO2与NO3的碰撞仅部分有效
D . 第三步反应活化能较高
|
|
| 2. 单选题 | 详细信息 | ||||||||||||||||||||||||||||
|
在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g) + Y(g)
 M(g) + N(g),所得实验数据如下表: M(g) + N(g),所得实验数据如下表:
下列说法正确的是( )
A . 实验①中,若5 min时测得n (M) = 0.050 mol,则0至5 min时间内,用N表示的平均反应速率υ (N) = 1.0×10-2 mol/(L·min)
B . 实验②中,该反应的平衡常数K = 2.0
C . 实验③中,达到平衡时,X的转化率为60%
D . 实验④中,达到平衡时,b>0.060
|
|||||||||||||||||||||||||||||
| 3. 单选题 | 详细信息 |
|
已知2SO2(g) + O2(g)
 2SO3(g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是( ) 2SO3(g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是( )
A . 容器内压强p:P甲=P丙> 2P乙
B . SO3的质量m:m甲=m丙> 2m乙
C . c(SO2)与c(O2)之比k:k甲=k丙> k乙
D . 反应放出或吸收热量的数值Q:Q甲=Q丙> 2Q乙
|
|
| 4. 单选题 | 详细信息 |
|
某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)
 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述错误的是( ) 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述错误的是( )
A . m=2
B . 两次平衡的平衡常数相同
C . X与Y的平衡转化率之比为1:1
D . 第二次平衡时,Z的浓度为0.4 mol·L-1
|
|
| 5. 单选题 | 详细信息 |
|
某反应过程能量变化如图所示,下列说法错误的是( )
A . 反应过程b有催化剂参与化学反应
B . 该反应为放热反应,热效应等于ΔH
C . 使用催化剂,可以提高活化分子百分数
D . 有催化剂条件下,反应的活化能等于E1+E2
|
|
| 6. 单选题 | 详细信息 |
|
SO2(g)+2CO(g)
 2CO2(g)+S(l)ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是( ) 2CO2(g)+S(l)ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
A . 平衡时,其他条件不变,通入一定量的氮气,压强增大,n(CO2)增大
B . 平衡时,其他条件不变,分离出硫,正反应速率加快
C . 平衡时,其他条件不变,升高温度可提高SO2的转化率
D . 若在原电池中进行,反应放出的热量减少
|
|
| 7. 单选题 | 详细信息 |
|
向绝热恒容密闭容器中通入SO2和NO2 , 一定条件下使反应
 达到平衡,正反应速率随时间变化的示意图如下所示。下列叙述正确的是( ) 达到平衡,正反应速率随时间变化的示意图如下所示。下列叙述正确的是( )
A . 反应在c 点达到平衡状态
B . 反应物浓度:
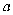 点小于 点小于 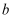 点
C . 反应物的总能量低于生成物的总能量
D . 点
C . 反应物的总能量低于生成物的总能量
D .  时,SO2的转化率: 时,SO2的转化率:  段小于 段小于  段 段
|
|
| 8. 单选题 | 详细信息 |
|
在恒容密闭容器中通入X并发生反应:2X(g)
 Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是( ) Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是( )
A . 该反应进行到M点放出的热量大于进行到W点放出的热量
B . T2下,在0~t1时间内,υ(Y)=
 mol/(L·min)
C . M点的正反应速率υ正大于N点的逆反应速率υ逆
D . M点时再加入一定量的X,平衡后X的转化率减小 mol/(L·min)
C . M点的正反应速率υ正大于N点的逆反应速率υ逆
D . M点时再加入一定量的X,平衡后X的转化率减小
|
|
| 9. 单选题 | 详细信息 |
|
CH4-CO2催化重整反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g)。反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。已知:
积碳反应:CH4(g)=C(s)+2H2(g)ΔH=+75kJ·mol-1 消碳反应:CO2(g)+C(s)=2CO(g)ΔH=+172kJ·mol-1在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙述正确的是( )
A . K积、K消均减小
B . v消增加的倍数比v积增加的倍数大
C . K积减小,K消增加
D . v积积减小,v消增加
|
|
| 10. 单选题 | 详细信息 |
|
研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3H2(g) CO2(g)+H2(g) 某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据: 有利于提高CO2转化为CH3OH平衡转化率的措施有( )
A . 投料比不变,增加反应物的浓度
B . 使用催化剂Cat.2
C . 升高反应温度
D . 增大CO2和H2的初始投料比
|
|
高中化学 试卷推荐
- 内蒙古呼和浩特市2022届高三第一次质量数据监测理科综合化学试题
- 四川省成都市蓉城高中教育联盟2021-2022学年高二上学期期末联考化学试题
- 四川省乐山市2020-2021学年高二下学期期末考试化学试题
- 辽宁省沈阳郊联体2021年高考化学5月模拟试卷
- 浙江省Z20联盟(名校新高考研究联盟)2021-2022学年高三上学期第二次联考化学试题
- 河北省邯郸市2022届高三二模考试化学试题
- 天津市河东区2022届高三学业水平等级性考试第二次模拟考试化学试题
- 2022年海南省高考真题化学试题
- 安徽省泗县第一重点高中2021-2022学年高二上学期化学开学考试试卷
- 山东省烟台市2020-2021学年高二下学期化学期中考试试卷
- 湖南省怀化市2020-2021学年高三上学期化学期中考试试卷
- 江苏省南通市海门区2021-2022学年高三12月第二次诊断测试化学试题
最近更新
- 用图甲的装置研究小车沿斜面在不同材料表面运动的情况.图乙是某同学在实验中获得的一条纸带.打点计时器的电源频率为50Hz.
- 清朝中后期,一支英国的贸易船队要到中国进行商业贸易,它的下列哪一行为是正确的() A.到中国内地采购货物
- 氮可以形成多种离子,如N3-、NH、N、NH、N2H、N2H等,已知N2H与N2H是由中性分子结合质子形成的,类似于NH
- 如图是某固态物质的溶解度曲线,图中的4个点分别表示在某条件下,该溶质的溶液所处的一种状况.下列说法正确的是()A.t℃时
- (2007·山东文综,24)“几十年的经验使我深刻体会到,学点哲学的确可以使人做事情少犯错误,做研究少走弯路。”下列观点
- 若复数a+bi(a,b∈R)的平方是纯虚数,则( )A.a=-b B.a=|b|
- . 如图,8块相同的长方形地砖拼成一个长方形,每块长方形地砖的长和宽分别是多少?现在请你设未知数列方程组来解决这个问题。
- 如图:直三棱柱ABC﹣A1B1C1中,∠ACB=90°,AA1=AC=BC=2,D为AB中点. (1)求证:BC1∥平面
- 设
- 1922年有一位苏俄农民在完成固定的粮食税后,把余粮运到苏俄境内的一个集市上出售,当地政府官员的正确态度是( )
- 我国即临渤海、又临黄海的省是( ) A、鲁、苏 B、辽、翼 C、辽、鲁 D、翼、鲁
- 下面是某家族的某种遗传病系谱图,请根据下图回答问题:(1)该病属于______性遗传病,其致病基因在_____染色体上。
- ,直挂云帆济沧海。(李白《行路难》)
- 化简
- 下面关于质点的说法中,正确的是()A. 火车的长度较长,所以不能把火车看成质点 B. 研究百米运动员跑步过程中的动作时,
- 补写出下列名篇名句的空缺部分 (1)书曰:“满招损,_________ 。”忧劳可以兴国,_________ ,自然之理
- 如图所示,在烧杯甲中装入蒸馏水,滴入2滴酚酞试剂,得到无色溶液。在烧杯乙中装入浓氨水。用一只大烧杯把甲、乙罩在一起。几分
- — What do you think of Zhang Liang Ying's English songs?
- 下列王安石变法的措施中,能直接体现“因天下之利以生天下之财”和“民不加赋而国用足”思想的有 ①青苗法 ②农田水利法
- 为了了解目前我国高中阶段师生关系的现状,BBC UK China站互动专区推出“高中师生关系大家谈”英文栏目。假如你叫李








