2015-2016学年黑龙江省哈尔滨三十二中高三上学期期末化学试卷
2015-2016学年黑龙江省哈尔滨三十二中高三上学期期末化学试卷
教材科目:化学
试卷分类:高三上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高三上学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
一定温度下,下列溶液的离子浓度关系式正确的是( )
A . pH=5的H2S溶液中,c(H+)=c(HS﹣)=1×10﹣5mol•L﹣1
B . pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C . pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH﹣)+c(HC2O4﹣)
D . pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
|
|
| 2. 单选题 | 详细信息 |
|
在25℃101kPa下,①2Na(s)+
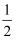 O2(g)═Na2O(s)△H1=﹣414kJ/mol, O2(g)═Na2O(s)△H1=﹣414kJ/mol, ②2Na(s)+O2(g)═Na2O2(s)△H2=﹣511kJ/mol, 下列说法正确的是( )
A . ①和②产物的阴阳离子个数比不相等
B . ①和②生成等物质的量的产物,转移电子数不同
C . 常温下Na与足量O2反应生成Na20,随温度升高生成Na20的速率逐渐加快
D . 25℃101kPa下,Na202(s)+2Na(s)═2Na20(s)△H=﹣317kJ/mol
|
|
| 3. 单选题 | 详细信息 |
|
在2A+B⇌3C+4D反应中,表示该反应速率最快的是( )
A . v(A)=0.3mol/(L•s)
B . v(B)=0.3mol/(L•s)
C . v(C)=0.3mol/(L•s)
D . v(D)=1mol/(L•s)
|
|
| 4. 单选题 | 详细信息 |
|
在密闭容器中,加入3mol A和1mol B,一定条件下发生反应3A(g)+B(g)⇌2C(g)+D(g),达平衡时,测得C的浓度为w mol/L,若保持体积和温度不变,重新按下列配比作起始物质,达到平衡时,C的浓度仍然为w mol/L的是( )
A . 6mol A+2mol B
B . 1.5mol A+0.5mol B+1mol C+0.5mol D
C . 3mol A+1mol B+2mol C+1mol D
D . 4mol C+1mol D
|
|
| 5. 单选题 | 详细信息 |
|
在2000K时,反应CO(g)+
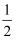 O2(g)⇌CO2(g) 的平衡常数为K1 , 则相同温度下反应2CO2(g)⇌2CO(g)+O2(g)的平衡常数K2为( ) O2(g)⇌CO2(g) 的平衡常数为K1 , 则相同温度下反应2CO2(g)⇌2CO(g)+O2(g)的平衡常数K2为( )
A .
 B . K12
C .
B . K12
C .  D . K1
D . K1 
|
|
| 6. 单选题 | 详细信息 |
|
某温度下,水的离子积约为10﹣12 , 将Va L pH=2的硫酸溶液与Vb L pH=11的NaOH溶液混合,若混合溶液的pH=10,体积是(Va+Vb) L,则Va:Vb为( )
A . 2:11
B . 2:9
C . 11:2
D . 9:2
|
|
| 7. 单选题 | 详细信息 |
|
可逆反应aA(g)+bB(g)⇌cC(g)+dD(g);△H同时符合下列两图中各曲线的规律的是( )
A . a+b>c+d T1<T2△H<0
B . a+b>c+d T1<T2△H>0
C . a+b<c+d T1>T2△H<0
D . a+b>c+d T1>T2△H>0
|
|
| 8. 单选题 | 详细信息 | |||||||||||||||
|
向10mL一定物质的量浓度的盐酸中滴加一定物质的量浓度的NaOH溶液,其pH变化如图所示,则两溶液的物质的量浓度分别是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 9. 单选题 | 详细信息 |
|
2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系.下列叙述错误的是( )
A . a为电池的正极
B . 电池放电反应为LiMn2O4=Li1﹣xMn2O4+xLi
C . 放电时,a极锂的化合价不发生变化
D . 放电时,溶液中的Li+从b向a迁移
|
|
| 10. 单选题 | 详细信息 |
|
室温下,将1mol的CuSO4•5H2O(s)溶于水会使溶液温度降低,热效应为△H1 , 将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2:CuSO4•5H2O受热分解的化学方程式为CuSO4•5H2O(s)
 CuSO4(s)+5H2O(l),热效应为△H3 , 则下列判断正确的是( ) CuSO4(s)+5H2O(l),热效应为△H3 , 则下列判断正确的是( )
A . △H2>△H3
B . △H1<△H3
C . △H1+△H3=△H2
D . △H1+△H2>△H3
|
|
高中化学 试卷推荐
- 备考2019年高考化学二轮专题 09 水溶液中的离子平衡
- 人教(新课标)高中化学一轮复习:专题9化学反应与能量
- 2015-2016学年山东省聊城市莘县实验高级中学高三上学期期中化学试卷
- 广东省肇庆市2016-2017学年高一上学期化学期末考试试卷
- 吉林省榆树一中五校联考2018-2019学年高一上学期化学期末考试试卷
- 高中化学鲁科版(2019)必修第一册 第1章 单元测试
- 上海市黄浦区2018-2019学年高考化学一模考试试卷
- 福建省福州八县一中2018-2019学年高一上学期化学期中考试试卷
- 山东省菏泽市2018-2019学年高考理综-化学一模考试试卷
- 江苏省盐城市2017-2018学年高一下学期化学期末考试试卷
- 上海市浦东新区2016-2017学年高二上学期化学期末考试试卷
- 高中化学人教版(2019)必修第二册 第六章测试卷
最近更新
- 下列物质中,不能用稀硫酸和金属反应直接值得的是( ) A.硫酸锌 B.硫酸镁 C.硫酸铁 D.硫酸铝
- 若a+b>0,且b<0,贝a,b,-a,-b的大小关系为 ( ) A.-a<-b<b<
- 如图为细胞核结构模式图,下列有关叙述正确的是()A.①是由DNA和蛋白质组成的环状结构 B.②是产生核糖体、mRNA和蛋
- 下列各组离子,能在指定溶液中大量共存的是:①无色溶液中:K+、Cl―、Na+、HCO3-、OH-②使pH试纸变深蓝的溶液
- Youcan borrow my car ________ you promise not to drive too f
- 图12-1-3所示是以质点P为波源的机械波沿着一条固定的轻绳传播到质点Q的波形图,则质点P刚开始振动时的方向为(
- 磁电式电表在没有接入电路(或两接线柱是空闲)时,由于微扰指针摆动很难马上停下来,而将两接线柱用导线直接相连,摆动着的指针
- 游乐场的过山车可以抽象成如图所示的模型:圆弧轨道的下端与圆轨道相接于M点,使一质量为m的小球从弧形轨道上距M点竖直高度为
- 15.将下列四句话填在下面的横线上,顺序最恰当的一组是( ) ①就像勇猛的战士一样,②不顾一天行军的疲劳,③马上扔下
- 如右图是根据某校10位高一同学的身高(单位:cm)画出的茎叶图,其中左边的数字从左到右分别表示学生身高的百位数字和十位数
- 豌豆种子的形状圆粒和皱粒为相对性状,下列杂交实验中能判断显、隐性关系的是( ) A. 圆粒×圆粒→圆粒
- 如图5-3-2所示,线圈L的自感系统和电容器的电容C都很小(如L=100 μH,C=100 pF),此电路的主要作用是(
- 镭是元素周期表中第七周期第ⅡA族元素,下列关于镭的性质的描述中不正确的是A.在化合物中呈+2价B.氢氧化物呈两性C.单质
- 设函数f(x)=ax-2-lnx(a∈R). (Ⅰ)若f(x)在点(e,f(e))处的切线为x-ey+b=0,求a,b的
- 下列关于生态系统成分的说法中正确的是( ) A.绿色植物一定是生产者,生产者一定是绿色植物 B.动物一定是消费者,
- 下列各句横线处应填入的词句,最恰当的一组是 ①我们在送别朋友时,常常引用“___________________”,以表
- 在新民主主义革命时期,中华民族精神的主体是 A.雷锋精神
- 材料: 纸币的发行量是世界各国宏观调控中的一个重要方面,对于纸币量的调控能力是国家宏观调控能力的最重要方面之一。人民币的
- 将函数的图象上各点的横坐标伸长到原来2的倍,再向左平移个单位,所得图象的函数解析式是( ) A.
- I hope my teacher will take my recent illness into _____ whe






