高三化学试题
在某温度下可逆反应:Fe2(SO4)3+6KSCN![]() 2Fe(SCN)3+3K2SO4达到平衡状态后加入少量下列何种固体物质,该平衡几乎不发生移动( )
2Fe(SCN)3+3K2SO4达到平衡状态后加入少量下列何种固体物质,该平衡几乎不发生移动( )
A、NH4SCN B、K2SO4 C、NaOH D、FeCl3·6H2O
某学生准备用37%、密度为1.19 g/mL的浓盐酸配制0.1 mo1·L-1的稀盐酸500 mL。请回答下列问题:
(1)量取浓盐酸的体积为 mL,应选用量筒的规格为 mL。
(2)配制时应选用容量瓶的规格为 mL。
(3)配制时(除容量瓶外)还需选用的仪器主要有烧杯、 、 和试剂瓶。
某有机反应中间体(M)的一种合成路线如图所示.
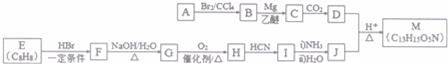

已知:①R﹣Br![]()
![]() PMgBr
PMgBr![]()
![]() RCOOH
RCOOH
②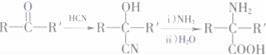
 (R′表示氢原子或烃基)
(R′表示氢原子或烃基)
③标准状况下,气态烃A的密度是H2的14倍
④芳香族化合物H能发生银镜反应
请回答:
(1)B的名称(系统命名)为 ;H→I的反应类型为 .
(2)E中官能团的结构简式为 ,
( 3)F→G的化学方程式为 .
(4 )D+J→M的化学方程式为 .
(5)写出符合下列条件的J的所有同分异构体的结构简式 、
 (不考虑立体异构).
(不考虑立体异构).
①苯环上连有﹣NO2 ②核磁共振氢谱有3个峰
(6)结合已有知识和相关信息,写出以CH3CHO和E为原料,经三步制备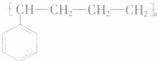
 的合成路线流程图(无机试剂任用)合成路线流程图示例为:CH3CHO
的合成路线流程图(无机试剂任用)合成路线流程图示例为:CH3CHO![]()
![]() CH3COOH
CH3COOH![]()
![]() CH3COOCH3.
CH3COOCH3.
短周期主族元素X、Y、Z、W原子序数依次增大,其中只有Y、Z处于同一周期且相邻,Z是地壳中含量最多的元素,W是短周期中金属性最强的元素。下列说法正确的是( )
A.原子半径:r(X) < r(Y) < r(Z) < r(W)
B.W的最高价氧化物的水化物是一种弱碱
C.Y的单质的氧化性比Z的强
D.X、Y、Z 三种元素可以组成共价化合物和离子化合物
氮及其化合物的转化过程如图所示。下列分析合理的是

A.催化剂a表面发生了极性共价键的断裂和形成
B.N2与H2反应生成NH3的原子利用率为100%
C.在催化剂b表面形成氮氧键时,不涉及电子转移
D.催化剂a、b能提高反应的平衡转化率
某学习小组设计了下列装置进行相关实验,装置和使用的药品均正确且能达到相应实验目的的是( )
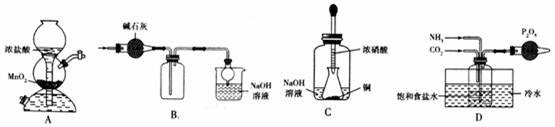
A.制备Cl2 B.干燥并收集SO2
C.制硝酸铜 D.制备NaHCO3
根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的的是( )

氮的氧化物是大气的主要污染物,是当前环保工作的重要研究内容之一。
(1)氨气还原氮的氧化物
①N2(g)+O2(g)=2NO(g) △H1 ②4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H2
则4NH3(g)+6NO(g)=5N2(g)+6H2O(1) △H=________。(用含△H1、△H2的式子表示)
依据反应②,可将氨气直接用于燃料电池,用KOH溶液作电解质溶液,写出负极电极反应式: 。
 (2)一定温度下,向2L恒容密闭容器中充入4.0mol NO2和4.0mol CO,在催化剂作用下发生反应4CO(g)+2NO2(g)
(2)一定温度下,向2L恒容密闭容器中充入4.0mol NO2和4.0mol CO,在催化剂作用下发生反应4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g) △H<0,测得相关数据如下:
N2(g)+4CO2(g) △H<0,测得相关数据如下:
①0~5min,用NO2的浓度变化表示的反应速率为____。
②以下表述能说明该反应己达到平衡状态的是____。
A.气体颜色不再变化 B.气体密度不再变化 C.气体平均相对分子质量不再变化
③20 min时,保持温度不变,继续向该容器中加入l.0mol NO2和l.0molCO,在t1时反应再次达到平衡,则NO2的转化率比原平衡____(填“增大”、“减小”或“不变)。
④该温度下反应的化学平衡常数K= _____。
(3)湿法脱硝:采用NaClO2 溶液作为吸收剂可对烟气进行脱硝。323 K 下,向足量碱性NaClO2 溶液中通入含NO 的烟气,充分反应后,溶液中离子浓度的分析结果如下表:
| 离子 | NO3- | NO2- | Cl- |
| c/(mol • L-1) | 2.0×10-4 | 1.0×10-4 | 1.75×10-4 |
①NaClO2 溶液显碱性,用离子方程式解释原因_______________________。
②依据表中数据,写出NaClO2溶液脱硝过程中发生总反应的离子方程式____________。
纯碱和小苏打是厨房中两种常见的用品,它们都是白色固体。下列区分这种两种物质的方法正确的是
A.分别用炒锅加热两种样品,全部分解挥发,没有物质残留的是小苏打
B.用洁净铁丝蘸取两种样品在煤气火焰上灼烧,使火焰颜色发生明显变化的是小苏打
C.用两只小玻璃杯,分别加入少量两种样品,再加入等量食醋,产生气泡快的是小苏打
D.先将两样品配成溶液,分别加入石灰水,无白色沉淀生成的是小苏打
中国古代“炼丹术”中蕴含了丰富的化学知识,为近代化学的建立和发展奠定了基础。下列关于“炼丹术”中涉及的史实解释错误的是
| 选项 | 史实 | 解释 |
| A | “胡粉 | 复分解反应原理 |
| B | “有硇水者,剪银塊(Ag)投之,则旋而为水” | 氧化还原反应原理 |
| C. | “曾青(硫酸铜)涂铁,铁赤色如铜……外变而内不化也” | 置换反应原理 |
| D | “铁釜代替土釜,加热丹砂(HgS),可增采也” | 平衡移动原理 |
A.A B.B C.C D.D
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
回答下列问题:
(1)为尽量少引入杂质,试剂①应选用NaOH溶液,若选用H2SO4溶液,其后果是_________。
(2)易拉罐溶解过程中主要反应的化学方程式为_______________;滤液A中的某种离子与NH4+,HCO3-均能反应生成沉淀B,该离子与NH4+反应的离子方程式为___________。
(3)Al(OH)3在水中存在两种电离方式,其中:Al(OH)3(aq)![]() AlO2-+H+(aq)+H2O(l) Ka=2.0×10-13(25℃),则25℃时Al(OH)3与NaOH溶液反应的平衡常数K=________________(列出含Kw、Ka的表达式并计算)
AlO2-+H+(aq)+H2O(l) Ka=2.0×10-13(25℃),则25℃时Al(OH)3与NaOH溶液反应的平衡常数K=________________(列出含Kw、Ka的表达式并计算)
(4)明矾与硫磺焙烧时发生反应的化学方程式为:KAl(SO4)2·12H2O+S![]() K2SO4+Al2O3+SO2↑+H2O(未配平),配平后的化学计量数依次为____________;每生成67.2L标准状况下的SO2,转移电子的物质的量为________;焙烧产生的SO2经催化氧化、吸收等过程可制得硫酸,若SO2催化氧化时的转化率为96.0%,则理论上用该法生成硫酸时硫元素的总转化率为__________。
K2SO4+Al2O3+SO2↑+H2O(未配平),配平后的化学计量数依次为____________;每生成67.2L标准状况下的SO2,转移电子的物质的量为________;焙烧产生的SO2经催化氧化、吸收等过程可制得硫酸,若SO2催化氧化时的转化率为96.0%,则理论上用该法生成硫酸时硫元素的总转化率为__________。
(1)X、Y、Z三种液体的近似pH如图,下列判断正确的是___________。

A.X一定是酸或强酸弱碱盐溶液 B.Y一定是90℃时的纯水
C.Y液体一定呈中性 D.Z可能是Na2SiO3溶液
(2)物质的量浓度相同的三种溶液:①NH4Cl②氨水③NH4HSO4,c(NH4+)大小顺序正确的
是___________。
A.①>②>③ B.③>①>② C.②>③>① D.③>②>①
(3)比较填空(选填“>"或“ <"或"=”)
①常温下两种溶液:a.pH=4盐酸 b.pH=4NH4Cl溶液,其中水的电离程度大小:a__________b。
 ②已知某可逆反应aA(g)+bB(g)
②已知某可逆反应aA(g)+bB(g)![]() cC(g)+dD(g)。当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如右图所示,则反应物和生成物的化学计量数之和:a+b ______c+d。
cC(g)+dD(g)。当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如右图所示,则反应物和生成物的化学计量数之和:a+b ______c+d。
(4)在一定体积的密闭容器中加入1molCO2和1mol H2,进行如下化学反应:CO2(g)+ H2(g) ![]() CO(g)+H2O(g) ,其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g) ,其化学平衡常数K和温度T的关系如下表:
| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应的化学平衡常数表达式为K=__________________________。
②反应为___________反应(填“吸热”或“放热”)。
③800℃,向容器内充入lmolCO2、lmolH2、lmol CO、lmolH2O,此刻反应的v正_______v逆(填“>"或“<”或“=”)
(1)有机反应类型很多,下列反应类型中可能属于加成反应范畴的是(填编号) 。
A.氧化反应 B.还原反应
C.加聚反应 D.缩聚反应
E.硝化反应 F.酯化反应
G.裂化反应 H.磺化反应
L.水解反应 J.皂化反应
K.油脂的氢化反应
(2)已知1 mol某有机物含碳原子n mol,在恰好完全燃烧时消耗氧气1.5 n mol,生成产物只有二氧化碳和水,则该有机物的化学式可能为 (用n表示分子内碳原子数,你认为有几种化学式就填几种)。
下列说法正确的是( )
A.乙烯和甲烷都能发生加聚反应
B.甲烷和乙烯都可以与氯气反应
C.酸性高锰酸钾溶液可以氧化苯和甲烷
D.乙烯可以与氢气发生加成反应,苯不能与氢气加成
在复习元素周期律过程中,某研究性学习小组的几位同学拟通过具体的实验来探讨某些金属元素的性质差异,下面是他们设计的探究性实验方案,请填写下列空白:
(1)实验目的:比较钠、镁、铝金属性强弱。
(2)实验用品:酒精灯、 、试管、试管夹、砂纸、滤纸;
钠、镁条、铝片、酚酞、蒸馏水、6 mol·L-1的盐酸
(3)实验过程与现象记录
Ⅰ.甲同学的方案如下:
| 实验过程 | 预期现象 | 实际观察到的现象 |
| a取已切去表皮的一小块金属钠,放入盛有水的某容器中 | 立即剧烈反应 | 开始时钠块浮在水面上不反应,稍后才开始与水剧烈反应 |
| b向盛有适量水(内含2滴 酚酞的试管中加入一小段镁条 | 有气泡产生,溶液变红色 | 没有相应现象,加热后仍无明显变化 |
| c向两支盛有3mL6mol·L-1盐酸的试管中加入大小相同的镁片和铝片 | 镁、铝与盐酸反应产生气泡剧烈程度不同 | 镁与盐酸反应产生气泡速率较快 |
①你认为a、b两步实验中出现异常现象的可能原因是:
a ;
b 。
②上面的实验表明:钠、镁、铝三种元素的金属性由强到弱的顺序为 。
Ⅱ乙同学的方案:他认为只需要一种试剂就可以确定钠、镁、铝的金属性强弱,预计他的主要实验操作是 。
向0.1 mol·L-1的Al2(SO4)3溶液中滴加1.0 mol·L-1的NaOH溶液,滴加过程中溶液pH随 NaOH溶液体积变化的曲线如右图所示。下列分析不正确的是( )
A. a点pH < 7的原因:Al3+ + 3H2O ![]() Al(OH)3 + 3H+
Al(OH)3 + 3H+
B. bc段发生的主要反应:Al3+ + 3OH- === Al(OH)3↓
C. ef段发生的主要反应:Al(OH)3 + OH- === AlO2- + 2H2O
D. d点,溶液中大量存在的离子是Na+、AlO2-和SO42-
某同学为了验证海带中含有碘,拟进行如下实验,请回答相关问题。
(1)第1步:灼烧。操作是将足量海带灼烧成灰烬。该过程中将使用到的硅酸盐质实验仪器除F外还有 (填代号,限填2项)。
A.试管 B.瓷坩埚 C.坩埚钳 D.铁三脚架
E.泥三角 F.酒精灯 G.烧杯 H.量筒
(2)第2步:Iˉ溶液的获取。操作是 。
(3)第3步:氧化。操作是依次加入合适的试剂。下列氧化剂最好选用(填代号)____________。
A.浓硫酸 B.新制氯水 C.KMnO4溶液 D.H2O2
理由是
(4)第4步:碘单质的检验。取少量第3步的溶液,滴加淀粉溶液,如果溶液显蓝色,则证明海带中含碘。
同物质的量浓度的KCl、CaCl2、AlCl3三种溶液的体积比为3 : 2 : 1,这三种溶液中Cl-的物质的量之比
A.3 : 2 : 1 B.1 : 2 : 3 C.3 : 4 : 3 D.2 : 3 : 1
关于氧化物的叙述正确的是( )
A、酸性氧化物都可以跟强碱溶液反应
B、与水反应可生成酸的氧化物都是酸性氧化物
C、金属氧化物都是碱性氧化物
D、不能跟酸反应的氧化物一定能跟碱反应
下列各组物质中,前者属于电解质,后者属于非电解质的是( )
A.二氧化碳、BaSO4 B.盐酸、蔗糖 C.KNO3、乙醇 D.NaOH、氯气
- 下列图示的四种实验操作名称从左到右依次是( ) A.蒸发、蒸馏、过滤、萃取 B.过滤、蒸馏、蒸
- The jobs ofthe future have not yet been invented, 36 Byh
- 19.补写出下列句子中的空缺部分。 ①孔子在《论语·雍也》中提出“文质彬彬,然后君子”,作为君子“文”和“质”二者不可偏
- 已知集合,,则( ) A. B. C. D.
- 阅读下面的文言文,完成后面题。 戴震,字东原,休宁人。读书好深湛之思,少时塾师授以说文,三年尽得其节目。年十六七,研精注
- 为探究物质的燃烧条件,某同学做了如右图所示实验:已知白磷着火点是40 ℃,红磷着火点是240 ℃;发现水中白磷和铜片上红
- 下列对文学常识的表述不正确的一项是( ) A.柳宗元是中国游记文学的奠基人,他的《永州八记》更是后世游记文学
- 下面句子各有一处语病,请在原句上修改。 (1) 我们要引导广大青少年学生用美的心灵去感受世界,用美的眼光去观察世界
- 南水北调工程是我国最大的水利工程,为了保证南水北调工程的顺利实施,2005年5月,在山东省沿东线工程的一些县区,环保部门
- “飞花两岸照船红,百里榆堤半日风。卧看满天云不动,不知云与我俱动” 。从生活与哲学角度看,这首诗说明了 A.运动是物质的
- 如图在的网格图(每个小正方形的边长均为1个单位长度)中,⊙A的半径为2个单位长度,⊙B的半径为1个单位长度,要使运动的⊙
- “少小离家老大回,乡音无改鬓毛衰。”这句诗说明文化对人的影响是( ) A.潜移默化的 B
- 如图12-7-6所示,实线表示波峰,S为波源,设波源频率为20Hz,且不运动,而观察者在1 s内由B运动到A,观察者接收
- 在下列四个结论中,正确的有________________.(填序号) (1)若A是B的必要不充分条件,则非B也是非A的
- (09杭州市质检)(12分)果蝇是非常好的遗传实验材料,请结合相关知识分析回答:(1)图A和图B表示果蝇甲和果蝇乙某染色
- 第Ⅱ卷(非选择题 共35分) 第四部分:写作(共两节,满分35分) 第一节 短文改错(满分10分) 此题要求改正所给
- “一家炒菜十家香”,这句话说明分子具有的主要性质是 A. 分子的体积很小 B. 分子间间隔很小 C. 分子可以再分 D.
- 以下是小瑛和小方设计的证明分子运动的实验:小方的实验如图(1)所示,图(2)是小瑛的实验,在锥形瓶中的小瓶里装着浓氨水,
- 下图为某季节某一条纬线上气压中心分布示意图(单位:百帕)。据此完成下面试题。线上四点对应的陆地表面的气压数值最低的是(
- 合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3。当催化剂中FeO与Fe2O3的质量之比为9∶20时,



