高三化学试题
下列离子在稳定人体血液的pH中起作用的是( )
A.Fe2+ B. Na+ C. HCO3- D. Cl-
在硫酸铁电化浸出黄铜矿精矿工艺中,有一主要反应:
CuFeS2+4Fe3+===Cu2++5Fe2++2S
反应结束后,经处理获得单质硫x mol。下列说法正确的是( )
A.反应中硫元素被氧化,所有铁元素均被还原
B.氧化剂是Fe3+,氧化产物是Cu2+
C.反应中转移电子的物质的量为x mol
D.反应结束后,测得溶液中三种金属离子的总物质的量为y mol,则原Fe3+的总物质的量为(y-x) mol![]()
实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为:
4CuI+Hg=Cu2HgI4+2Cu
(l)上述反应产物Cu2HgI4中,Cu元素是_______价:
(2)以上反应中的氧化剂为_______,当有1mol CuI参与反应时,转移电子_______mol;
(3) CuI可由Cu2+与I-直接反应制得,请配平下列反应的离子方程式.
____Cu2++ ____ I- --- ________CuI + _____I3-。
为了探究乙醇和金属钠反应的原理,做了如下四个实验:
实验一:向小烧杯中加入无水乙醇,再放入一小块金属钠,观察现象,并收集产生的气体。
实验二:设法检验实验一收集到的气体。
实验三:向试管中加入3 mL水,并加入一小块金属钠,观察现象。
实验四:向试管中加入3 mL乙醚(CH3CH2OCH2CH3),并加入一小块金属钠,发现无任何现象发生。
回答以下问题:
(1)简述实验二中检验气体的实验方法及作出判断的依据:
_____________________________________________________。
(2)从结构上分析,该实验选取水和乙醚做参照物的原因是
_____________________________________________________。
(3)实验三的目的是欲证明__________;实验四的目的是欲证明____________;根据实验三和实验四的结果,可以证明乙醇和金属钠反应的化学方程式应为________________________。
利用异戊二烯合成异戊烯醇和香料乙位紫罗兰酮的流程如下图所示(部分反应条件和产物已略去):

已知:![]()
回答下列问题:
(1) 利用系统命名法对异戊二烯命名___________________________________。
(2) 写出异戊烯醇的结构简式___________________________________。
(3) E 中官能团的名称为___________________________________。
(4) 由B→G的反应类型为_______________________________;由B→C 的反应类型为_________________。(5) 有关有机物D的说法中正确的是______________。
a.存在顺反异构 b.化学式为C10H16O
c.能被银氨溶液和酸性高锰酸钾溶液氧化 d.能被氢气还原
(6) H的同分异构体有多种,则属于醛和酮的异构体共有______种(不考虑立体异构),核磁共振氢谱有两组峰,且峰的面积之比等于2:3的同分异构体的结构简式为_________________________________。
(7) 以乙醛为初始原料设计制备![]() 的合成路线_______________________________________________。
的合成路线_______________________________________________。
用含4 mol HCl的浓盐酸与足量的MnO2共热,生成的氯气为( )
A.2 mol B.1 mol C.小于1 mol D.小于2 mol,大于1 mol
能正确表示下列反应的离子方程式是( )
A.将铜屑加入Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+
B.将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
C.将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑
D.将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
.某新型药物H(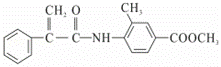 )是一种可用于治疗肿瘤的药物,其合成路线如图所示:
)是一种可用于治疗肿瘤的药物,其合成路线如图所示:
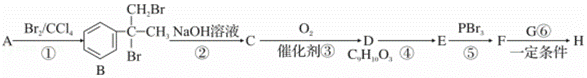
已知:(1)E的分子式为C9H8O2,能使溴的四氯化碳溶液褪色
(2)![]() (R为烃基)
(R为烃基)
(3)![]()
请回答下列问题:
(1)A的结构简式为_____;D的官能团的名称为_____。
(2)①的反应类型是_____;④的反应条件是_____。
(3)写出B→C的化学方程式_____。
(4)写出F+G→H的化学方程式_____。
(5)参照H的上述合成路线,设计一条由乙醛和NH2CH(CH3)2为起始原料制备医药中间CH3CONHCH(CH3)2的合成路线_____。
已知:
2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol;
Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g)△H=﹣226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为283 kJ
B.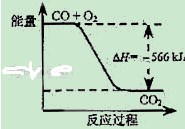 如图可表示由CO生成CO2的反应过程和能量关系
如图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>﹣452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15, X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
A. 原子半径:W>Z>Y>X>M
B. 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
C. XZ2, X2M2, W2Z2均为直线型的共价化合物
D. 由X元素形成的单质不一定是原子晶体
下列应用不涉及物质氧化性或还原性的是( )
A.用葡萄糖制镜或保温瓶胆 B.用ClO2杀菌、消毒
C.用Na2SiO3溶液制备木材防火剂 D.用浸泡过高锰酸钾溶液的硅藻土保鲜水果
实验室提供下列仪器(用品)和药品:
仪器(用品):①铁架台(附铁圈、铁夹);②酸(碱)式滴定管;③烧杯;④玻璃棒;⑤胶头滴管;⑥天平(含砝码、镊子);⑦滤纸;⑧分液漏斗;⑨普通漏斗;⑩双孔橡皮塞;![]() 烧瓶
烧瓶
药品:碱石灰、Na2CO3固体,NH4C1固体、MnO2、标准NaOH溶液、未知浓度的HCl
溶液、H2O2溶液、蒸馏水。
请按要求填空:
(1)过滤时,应选用的仪器是 (请填写序号)。
(2)欲配制500m L0.1 mol/L的Na2CO3溶液,还缺少的仪器是 ;
若测定未知HCl溶液的浓度,还缺少的仪器是 。
(3)可用上述提供的药品和仪器来制取的气体是 (请填写化学式)。
1942年,我国化工专家侯德榜以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱,他的“侯氏制碱法”为世界制碱工业做出了突出贡献。有关反应的化学方程如下:
NH3+CO2+H2O === NH4HCO3;NH4HCO3+NaCl === NaHCO3↓+NH4Cl;
2NaHCO3 ![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(1)“侯氏制碱法”把合成氨和纯碱两种产品联合生产,请写出工业合成氨的化学反应方程式 ;已知合成氨为放热反应,若从勒夏特列原理来分析,合成氨应选择的温度和压强是 (选填字母)。
a.高温 b.低温 c.常温 d.高压 e.低压 f.常压
(2)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 (选填字母)
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(3)某探究活动小组根据上述制碱原理,欲制备碳酸氢钠,同学们按各自设计的方案进行实验。
第一位同学:将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
请回答:
①写出甲中发生反应的离子方程式 。
②乙装置中的试剂是 。
③实验结束后,分离出NaHCO3晶体的操作是 (填分离操作的名称)。
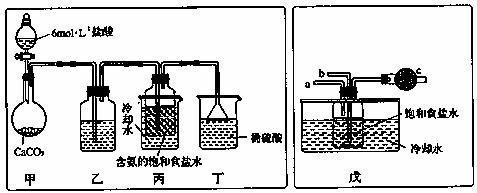
第二位同学:用图中戊装置进行实验(其它装置未画出)。
①为提高二氧化碳在此反应溶液中被吸收的程度,实验时,须先从a管通入 气体,再从b管中通入 气体。
②装置c中的试剂为 (选填字母)。
e.碱石灰 f.浓硫酸 g.无水氯化钙
(4)请你再写出一种实验室制取少量碳酸氢钠的方法(用简要的文字和相关的化学反应方程式来描述): 。
纵观古今,化学与生活皆有着密切联系。下列有关说法错误的是( )
A. “梨花淡自柳深青,柳絮飞时花满城”中柳絮的主要成分和棉花的相同
B. 制作烟花的过程中常加入金属发光剂和发色剂使烟花放出五彩缤纷的颜色
C. 草莓棚中使用的“吊袋式二氧化碳气肥”的主要成分可以是碳酸钙
D. 《本草纲目》记载的“凡酸坏之酒,皆可蒸烧”的实验方法可用来分离乙酸和乙醇
下列图示的实验操作,不能实现相应实验目的的是( )
|
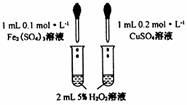
A.研究不同催化剂对双氧水分解速率的影响 |
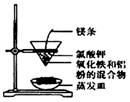
B.实验室演示铝热反应 |
|
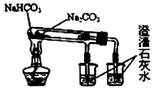
C.比较碳酸钠与碳酸氢钠的热稳定性 |
D.验证铁与水燕气反应的气体产物H2 |
汽车尾气中的CO、NOx以及燃煤废气中的SO2都是大气污染物,对它们的治理具有重要意义。
(1)氧化还原法消除NOx的转化如下:
NOO3反应ⅠNO2CO(NH2)2反应ⅡN2
①反应 Ⅰ 为NO+O3===NO2+O2,生成标准状况下11.2 L O2时,转移电子的物质的量是___ mol。
②反应Ⅱ中,当n(NO2)∶n[CO(NH2)2]=3∶2时,氧化产物与还原产物的质量比为__。
(2)吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如图所示(Ce为铈元素)。
装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO和NO,请写出生成等物质的量的NO和NO时的离子方程式:__。

(3)装置Ⅲ的作用之一是用质子交换膜电解槽电解使得Ce4+再生,再生时生成的Ce4+在电解槽的__ __(填“阳极”或“阴极”),同时在另一极生成S2O的电极反应式为__。
(4)已知进入装置Ⅳ的溶液中NO的浓度为a g·L-1,要使1 m3该溶液中的NO完全转化为NH4NO3,至少需向装置Ⅳ中通入标准状况下的氧气__ L(用含a的代数式表示,结果保留整数)。
某温度下2 L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如下表所示。下列说法正确的是( )
| X | Y | W | |
| n(起始状态)/mol | 2 | 1 | 0 |
| n(平衡状态)/mol | 1 | 0.5 | 1.5 |
A.该温度下,此反应的平衡常数K=6.75
B.升高温度,若W的体积分数减小,则此反应ΔH>0
C.增大压强,正、逆反应速率均增大,平衡向正反应方向移动
D.该温度下,此反应的平衡常数表达式是
K=![]()
合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
【实验方案一】将铝镁合金与足量NaOH溶液反应,测定剩余固体质量.实验中发生反应的化学方程式是______
【实验步骤】
(1)称取5.4g铝镁合金粉末样品,溶于VmL 2.0mol/LNaOH溶液中,充分反应.则NaOH溶液的体积V≥ ______ .
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将______ (填“偏高”、“偏低”或“无影响”).
【实验方案二】
将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01105Pa)的体积.
【问题讨论】
(3)同学们拟选用图1实验装置完成实验:
![]()
①你认为最简易的装置其连接顺序是:A接______ 接______ 接______ (填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因.______ .
③实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是______ .
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平,读取量筒中水的体积
(4)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小.于是他们设计了图2所示的实验装置.
①装置中导管a的作用是______ .
②实验前后碱式滴定管中液面读数分别为V1mL、V2mL.则产生氢气的体积为______ mL.
广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其它简单仪器组成各种功能的装置.下列各图中能用作防倒吸安全瓶的是( )
A. 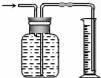 B.
B. 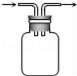 C.
C.  D.
D. 
生活中碰到的某些问题,常需要用化学知识解释,下列说法不正确的是
A.做馒头时加少量小苏打,是为了使馒头更加松软
B.药皂中掺入少量的苯酚,是由于苯酚有杀菌作用
C.食盐中加入少量碘酸钾,人食用后可补充人体内碘元素的不足
D.腌制火腿时添加少量NaNO2,是为了使火腿肉的味道更加美味可口
- 下图是关于反应A2(g)+3B2(g)2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是
- (8分)在天平两端各放等质量的两个锥形瓶(瓶口用单孔塞和导管连接起来,气球中装有等质量的大理石),如图所示。左盘锥形瓶中
- 设,若方程有两个实数解,求实数的取值范围.
- 下列关于食品添加剂的叙述中不正确的是( ) A、醋通常用作调味剂去除腥味 B、亚硝酸钠可以用作发色剂 C、我
- 已知二次函数的图象如图所示,有下列5个结论:① ;② ;③ ;④ ; ⑤,(的实数)其中正确的结论有( )
- 如图,下列水平放置的几何体中,主视图不是长方形的是 ( ▲ ).
- 已知全集,,则下图中阴影部分表示的集合是 A. B. C.
- 经测定C3H7OH和C6H12 组成的混合物中氧的质量分数为8%,则混合物中碳的质量分数是 A.22% B. 7
- 下列操作中,溶液的颜色不发生变化的是( ) A. 碳酸氢钠溶液中滴加稀盐酸 B. 硫酸铁溶液中滴加硫氰化钾溶液 C.
- “海宝”(见下图)是以汉字“人”为创意的2010年上海世博会吉祥物。“海宝”的设计强调了以人为中心的理念。下列历史事件
- The teacher _______some old friends on his vacation trip to
- 下列句子中,划线的词使用不当的一项是( )(2分)A.目前,水资源短缺情况正以锐不可当之势影响着我们的工作和生活。B.
- Suan: Oh, no! The door and the window______!Victor:
- 湖北起义军曾于1911年10月12日颁布公告,明确规定:“虐待商人者,斩。扰乱商务者,斩。关闭店铺者,斩。繁荣商业者,奖
- 下列各项中能视为进入人体内环境或在内环境中发生的是( ) ①食物进入消化道 ②CO2由线粒体进
- 依法有序扩大公民的政治参与,是实现全面建设小康社会奋斗目标的新要求。公民参与政治生活,必须坚持以下原则( ) ①公
- 下面划线的成语使用不当的一项是:( )(2分)A.真想不到当年拿起英语就头痛的他,竟能说出一口流利的英语,真得让人刮目
- 有一种WSJ-60型号电热壶,其铭牌标志如图所示。先将一壶20℃的水在额定电压下烧开需时5min,已知外界大气压为1标准
- 如图所示,一质量为m=1 kg、长为l=1 m的直棒上附有倒刺,物体顺着直棒倒刺下滑,其阻力只为物体重力的1/5,逆着倒
- (12分) (1)下列曲线分别表示元素某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质),把与下面的元素有关性