高一化学试题
取标准状况下CH4和过量O2的混合气体840mL,点燃,将燃烧后的气体用过量碱石灰吸收,碱石灰增重0.600g.请计算:
-
(1) 碱石灰吸收后所剩气体的体积(标准状况下);
-
(2) 原混合气体中CH4与O2的体积比.
将5.6LCO2气体缓慢通过一定量的Na2O2固体后,得到3.36L气体(气体体积均在标准状况下测定),所得气体的质量为( )
A . 5.4g
B . 4.8g
C . 3.8g
D . 6.6g
在18.6g Fe和Zn合金中加入200mL某浓度的稀硫酸恰好完全反应,生成0.3mol H2 . 则原合金中有mol Fe,稀硫酸的物质的量浓度为 mol/L.
下列微粒的表达式中正确的是 ( )
A . Be原子的结构示意图:  B . S2-的结构示意图:
B . S2-的结构示意图:  C . F原子的结构示意图:
C . F原子的结构示意图:  D . Na+的结构示意图:
D . Na+的结构示意图: 
取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2 , 再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:

-
(1) 原NaOH溶液的物质的量浓度为.
-
(2) 曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是,其物质的量之比为.
-
(3) 曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为 mL.
m mol C2H2跟n mol H2在密闭容器中反应,当该可逆反应达到平衡时,生成p mol C2H4 . 将反应后的混合气体完全燃烧生成CO2和H2O,所需要氧气的物质的量是( )
A . (3m+n)mol
B . ( 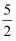 m+
m+  ﹣3p)mol
C . (3m+n+2p)mol
D . (
﹣3p)mol
C . (3m+n+2p)mol
D . ( 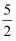 m+
m+  )mol
)mol
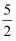 m+
m+  ﹣3p)mol
C . (3m+n+2p)mol
D . (
﹣3p)mol
C . (3m+n+2p)mol
D . ( 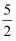 m+
m+  )mol
)mol
32.5g的Zn与足量的稀盐酸完全反应,最多可收集到H2多少升(标准状况)?生成ZnCl2的物质的量是多少?
使1mol乙烯与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照的条件下发生取代反应全部生成C2H2Cl4 , 则两个过程中消耗的氯气的总的物质的量是( )
A . 3mol
B . 4mol
C . 5mol
D . 6mol
钾是比钠活泼的金属,与水反应的产物与钠相似:2K+2H2O=2KOH+H2↑.将少量金属钾投入下列物质的水溶液中,有气体放出且溶液质量减轻的是( )
A . CuSO4
B . NaOH
C . H2SO4
D . HCl
在  Li、
Li、  N、
N、  Na、
Na、  Mg、
Mg、 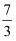 Li、
Li、  C中和互为同位素.
C中和互为同位素.
 Li、
Li、  N、
N、  Na、
Na、  Mg、
Mg、 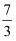 Li、
Li、  C中和互为同位素.
C中和互为同位素.
下列叙述中正确的是( )
A .  和
和 是中子数不同质子数相同的同种核素
B . 中子数为20的氯原子可以表示为
是中子数不同质子数相同的同种核素
B . 中子数为20的氯原子可以表示为 C . 同种元素的原子均有相同的质子数和中子数
D . F-的结构示意图可以表示为
C . 同种元素的原子均有相同的质子数和中子数
D . F-的结构示意图可以表示为
 和
和 是中子数不同质子数相同的同种核素
B . 中子数为20的氯原子可以表示为
是中子数不同质子数相同的同种核素
B . 中子数为20的氯原子可以表示为 C . 同种元素的原子均有相同的质子数和中子数
D . F-的结构示意图可以表示为
C . 同种元素的原子均有相同的质子数和中子数
D . F-的结构示意图可以表示为
铁是一种常见的金属,它在元素周期表中位于第四周期第Ⅷ族,原子序数为26,则Fe2+的结构示意图为( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
向含amol氯化铝的溶液中加入bmol氢氧化钾溶液,生成沉淀物质的量可能是( )
①amol ②bmol ③  mol ④
mol ④  mol ⑤0mol ⑥(4a﹣b)mol.
mol ⑤0mol ⑥(4a﹣b)mol.
A . ①②④⑤⑥
B . ①③⑤
C . ①②③⑤⑥
D . ①③④⑤⑥
下列微粒的结构示意图中,正确的是( )
A . Mg2+  B . Cl
B . Cl  C . Ar
C . Ar  D . K
D . K 
将等物质的量的金属Na、Mg、Al分别与100mL 2mol•L﹣1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如图所示,则下列说法错误的是( )

A . x=2.24
B . 钠的物质的量为0.2 mol
C . 反应时,Na、Mg、Al均过量
D . 曲线b为Mg与盐酸反应的图象
在某稀硝酸的溶液中,加入5.6g铁粉充分反应后,铁粉全部溶解,放出NO气体,溶液质量增加3.2g,所得溶液中Fe2+和Fe3+物质的量之比为( )
A . 1:1
B . 2:1
C . 3:2
D . 4:1
C、CH4是常用的燃料,它们每1mol分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量分别为393.5kJ、890.3kJ.计算说明:(写出必要的文字说明和重要演算步骤,只写出最后答案的不能得分.有数值计算的题,数值结果保留到小数点后1位.)
-
(1) 1g C完全燃烧时放出的热量.
-
(2) 完全燃烧相同质量的C和CH4 , 哪种燃料放出热量较多?
用锌,氧化铜,稀硫酸作原料制取铜时,有下列两种途径:
(1)锌  氢气
氢气  铜
铜
(2)氧化铜  硫酸铜
硫酸铜 
若用这两种方法制得相同质量的铜时,下列叙述符合实际实验结果的是( )
A . 消耗相同质量的硫酸
B . 消耗相同质量的锌
C . 消耗相同质量的氧化铜
D . 生成的硫酸锌质量相同
向一定量的FeO和Fe2O3的混合物中加入120mL 4mol•L﹣1的稀硝酸,恰好使混合物完全溶解,放出1.344L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现.若用足量的氢气在加热条件下还原相同质量的混合物,能得到铁的物质的量为( )
A . 0.24 mol
B . 0.21 mol
C . 0.16 mol
D . 0.14 mol
将70g过氧化钠和氧化钠的混合物跟98g水充分反应,所得气体在标准状况下为5.6L,试分别写出过氧化钠和氧化钠跟水反应的化学方程式,并计算所得溶液质量分数为多少?
最近更新
- 如图所示,是中国第五代隐形重型歼击机—歼20。2011年1月11日12时50分,歼20在成都实现首飞,历时18分钟。下列
- 图是“水循环示意图”。读图回答题。甲、乙、丙三类水循环均有的环节是 ( ) A.径流 B.下渗 C
- 资产阶级维新派的施政纲领是( ) A.《孔子改制考》
- PauI doesn't have to be made______.He always works hard.
- 一正电荷仅在电场力作用下,从A点运动到B点,速度大小随时间变化的图象如图6-2-3所示.下列关于A、B两点电场强度E的大
- 有X、Y、Z三种元素,已知:①X2-、Y-均与Y的气态氢化物分子具有相同的电子数; ②Z与Y可组成化合物ZY3,ZY3溶
- 化石证明许多物种只存活了相当短暂的时代就逐步灭绝了,最能解释这一现象的是( ) A.缺乏能适应环境变化的可遗传变
- 一束光线从空气斜射到玻璃表面,当入射角逐渐减小时,折射角将( ) A、保持不变 B、
- 一段通电导线平行于磁场方向放入匀强磁场中,导线上的电流方向由左向右,如图6-1-16所示.在导线以其中心点为轴转动90°
- 如图所示,竖直平面内边长为a的正方形ABCD是磁场的分界线,在正方形的四周及正方形区域内存在方向相反、磁感应强度的大小均
- — — Nothing serious, but a bittired. — Better have
- 关于钠离子和钠原子的认识不正确的是() A.它们的质子数相同 B.它们的电子层数不同 C.Na比Na+少一个电子 D.N
- 下图是文艺复兴时期的代表作品的是 A B
- .用科学计数法表示-1200000=_________________. 1.4249万≈______(精确到百位
- 下列物质中既能与盐酸又能与氢氧化钠溶液反应的是() A.CuO
- 计算(0.5×105)3×(4×103)2的结果是A. 2×1013 B. 0.5×1014
- 一质点做匀速圆周运动,下列物理量不变的是A.转速 B.线速度 C.合外力 D.向心加速度
- 在离体的植物细胞形成愈伤组织的过程中,不需要 A.消毒灭菌 B.适宜的温度
- 斜率为k的直线l过点P(,0)且与圆C:存在公共点,则k2≤的概率为 A. B.
- 二次函数的图象上有两点(3,-8)和(-5,-8),则此抛物线的对称轴是( )A、x=4 B、x=3



