原子核外电子排布 知识点题库
氮族元素和卤族元素都能形成许多种物质.
-
(1) 基态P原子中,电子占据的最高能级符号为 ,基态N原子核外有 种运动状态不同的电子,基态Br原子的价电子排布式为
-
(2) HCN的结构式为 ;其中心C原子的杂化类型为 杂化.氮、磷、氟三种元素的电负性由大到小的顺序为 (用元素符号表示).
-
(3) 已知PCl3是不稳定的无色液体,遇水反应可生成两种酸,该反应的化学方程式 为 ,所得含氧酸(已知该含氧酸的各步电离平衡常数分别为Ka1=1.6×10﹣2和Ka2=7×10﹣7)和足量的NaOH溶液反应生成盐的化学式为
-
(4) 根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子 (填元素名称)
F
Cl
Br
I
第一电离能((kJ•mol﹣1))
1681
1251
1140
1008
含氮化合物种类繁多,卟吩(图A)连有取代基时即称为卟啉,卟啉的四个氮原子易与金属离子结合生成叶绿素(图B)等多种物质.请回答:

-
(1) 卟吩中N原子采用的轨道杂化方式是
-
(2) 下列有关叶绿素分子的说法正确的是 (填选项序号).A . 图1中1﹣5号C中有三个具有手性 B . 分子中存在配位键 C . 图1中1、2、3、4号C共面 D . N的第一电离能大于O
-
(3) 卟啉与Fe2+合即可形成血红素,Fe2+的电子排布式为
-
(4) 氰化氢(HCN)是一种含氮剧毒化合物,其分子中σ键与π键的个数比为.由分子结构推测,氰化氢(填“易”或“不易”)溶于水,原因是.氰化氢进人人体后产生的CN﹣能使人迅速中毒,请举出两种CN﹣的等电子体.
-
(5) N与B能够形成一种硬度接近金刚石的物质,其晶体结构如图2,若其晶胞边长为apm,则其密度为g.cm﹣3(只列算式).
张亭栋研究小组受民间中医启发,发现As2O3(俗称砒霜)对白血病有明显的治疗作用.氮(N)、磷(P)、砷(As)等都是VA族的元素,该族元素的化合物在研究和生产中有许多重要用途.回答下列问题:
-
(1) As原子的核外电子排布式为.
-
(2) P和S是同一周期的两种元素,P的第一电离能比S大,原因是.
-
(3) NH4+中H﹣N﹣H的键角比NH3中H﹣N﹣H的键角(填“大”或“小”),原因是.
-
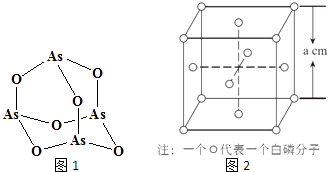
(4) Na3AsO4中含有的化学键类型包括;AsO43﹣的空间构型为,As4O6的分子结构如图1所示,则在该化合物中As的杂化方式是.
-
(5) 化合物NH5中的所有原子最外层都满足稳定结构,则NH5是晶体.
-
(6) 白磷(P4)的晶体属于分子晶体,其晶胞结构如图2(小圆圈表示白磷分子).已知晶胞的边长为a cm,阿伏加德罗常数为NA mol﹣l , 则该晶胞中含有的P原子的个数为,该晶体的密度为 g•cm﹣3(用含NA、a的式子表示).
请回答下列问题:
-
(1) N、Al、Si、Zn、Fe五种元素中,有一种元素的电离能数据如下:
电离能
I1
I2
I3
I4
…
Im/kJ•mol﹣1
578
1817
2745
11578
…
则该元素是(填写元素符号).N原子的价电子排布图为.
-
(2) 已知Zn2+能与氨分子形成配离子[Zn(NH3)4]2+ , 1mol该离子含有σ键的数目为;
-
(3) K3[Fe(CN)6]可用来检验Fe2+ , 向硫酸亚铁溶液中加入几滴K3[Fe(CN)6],观察到的现象是,与CN﹣互为等电子体的微粒有(填化学式,写2种)
C、N、O三种元素第一电离能由大到小的顺序为;三种元素形成的简单氢化物分子中键角由大到小依次为(用分子式表示).
-
(4) 已知Fe的相对原子质量为M,阿伏加德罗常数用NA表示,已知金属Fe为体心立方堆积,若Fe原子半径为acm,密度为ρg/cm3 . 则M=(用ρ、a、NA表达式表示)
“摩尔盐”是分析化学中的重要试剂,化学式为(NH4)2Fe(SO4)2·6H2O。“摩尔盐”在一定条件下分解的方程式为:4[(NH4)2Fe(SO4)2·6H2O]  2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
 2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
-
(1) 铁元素在元素周期表中的位置为,其价层电子排布图为。
-
(2) 组成“摩尔盐”的非金属元素中第一电离能最大的元素为。“摩尔盐”的分解产物中属于非极性分子的化合物是。
-
(3) NH3的沸点比N2O的沸点(填“高”或“低”),其主要原因是。
-
(4) K3[Fe(CN)6]常用于检验Fe2+ , K3[Fe(CN)6]中除了离子键以外还存在的化学键为,与CN—互为等电子体的单质的分子式为。HCN分子中σ键和π键的个数之比为。
-
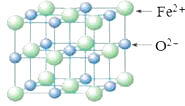
(5) FeO晶胞结构如下图所示,FeO晶体中Fe2+配位数为,若该晶胞边长为acm,则该晶胞密度为g/cm3。
下列各项叙述中,正确的是( )
A . 电子层序数越大,s原子轨道的形状相同、半径越小
B . 在同一电子层上运动的电子,其自旋方向肯定不同
C . 镁原子由1s22s22p63s2→ls22s22p63p2时,原子吸收能量,由基态转化成激发态
D . 原子最外层电子排布是5s1的元素,其氢氧化物不能使氢氧化铝溶解
一个价电子构型为2s22p5的元素,下列有关它的描述正确的有( )
A . 原子序数为8
B . 电负性最大
C . 原子半径最大
D . 第一电离能最大
下列表示不正确的是( )
A . Na+的轨道表示式: 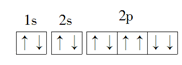 B . Na+的结构示意图:
B . Na+的结构示意图: 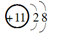 C . Na的电子排布式:1s22s22p63s1
D . Na的简化电子排布式:[Ne] 3s1
C . Na的电子排布式:1s22s22p63s1
D . Na的简化电子排布式:[Ne] 3s1
 B . Na+的结构示意图:
B . Na+的结构示意图:
下列说法正确的是( )
A . 原子核外各电子层最多能容纳的电子数为 n2
B . 同一主族中,第三周期和第四周期元素原子的核电荷数都相差 8
C . 门捷列夫在 1869 年提出了元素的性质随着原子序数的递增而呈现周期性变化的规律
D . 位于第四周期第ⅣA 族的元素为金属元素
下列说法正确的是( )
A . p电子云都是哑铃形的,每个p能级有3个原子轨道,它们相互垂直,能量相同
B . 基态氮原子的价电子排布图: 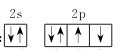 C . 甲醛(HCHO)和光气(COCl2)分子中:键角∠H—C—H<∠Cl—C—Cl
D . 四硼酸根离子Xm-(含B、O、H)的球棍模型如图,配位键存在于4、5和4、6原子之间
C . 甲醛(HCHO)和光气(COCl2)分子中:键角∠H—C—H<∠Cl—C—Cl
D . 四硼酸根离子Xm-(含B、O、H)的球棍模型如图,配位键存在于4、5和4、6原子之间 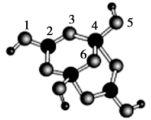
 C . 甲醛(HCHO)和光气(COCl2)分子中:键角∠H—C—H<∠Cl—C—Cl
D . 四硼酸根离子Xm-(含B、O、H)的球棍模型如图,配位键存在于4、5和4、6原子之间
C . 甲醛(HCHO)和光气(COCl2)分子中:键角∠H—C—H<∠Cl—C—Cl
D . 四硼酸根离子Xm-(含B、O、H)的球棍模型如图,配位键存在于4、5和4、6原子之间 
随原子序数的递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。
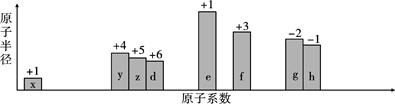
根据判断出的元素回答问题:
-
(1) f在元素周期表的位置是。
-
(2) 比较d、e常见离子半径大小(用化学式表示,下同):>;比较g、h的最高价氧化物对应的水化物的酸性强弱是>。
-
(3) 画出x2d2的电子式:。
-
(4) 已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:。
-
(5) 写出用惰性电极电解eh溶液的化学方程式:。
2020年12月17日嫦娥五号返回器带回月球土壤样品。研究发现,月球土壤样品中存在铁、金、银、铅、锌、铜等矿物颗粒。请回答下列问题:
-
(1) 基态Fe原子的价电子排布式为,其核外填充有电子的原子轨道数目为,基态Fe2+与Fe3+中未成对电子数之比为。邻二氮菲(
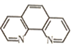 )中N原子可与Fe2+通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定Fe2+浓度,该反应的适宜pH范围为2~9,试解释若pH<2会产生什么影响。
)中N原子可与Fe2+通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定Fe2+浓度,该反应的适宜pH范围为2~9,试解释若pH<2会产生什么影响。
-
(2) Zn元素在元素周期表中的位置为,它的基态原子的M电子层中电子占据的最高能级是,该能级有对成对电子。
-
(3) 我国科学家研究发现,十八胺在较高温度下具有一定的还原性,由于从十八胺中获得电子的能力不同,不同的金属盐在十八胺体系中反应可以得到不同的产物:
单一金属盐
Zn2+
Ag+
在十八胺体系中的产物
ZnO
Ag
已知元素的电负性数据:
元素
Zn
Ag
Au
电负性(鲍林标度)
1.6
1.9
2.4
据此推测单一的金属(Au3+)盐在十八胺体系中反应的产物为(写化学式)。
红砷镍矿(NiAs)是常见的镍矿之一、回答下列问题:
-
(1) 对具有下列价电子排布的Ni或As进行光谱实验,用光谱仪一定能摄取到原子发射光谱的是___________(填字母)。A .
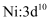 B .
B .  C . As:
C . As: 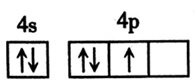 D . Ni:
D . Ni: 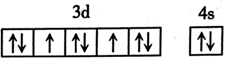
-
(2) 镍及其化合物常用作有机合成的催化剂,如
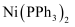 (
( 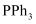 为三苯基磷,其结构为
为三苯基磷,其结构为 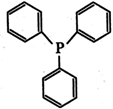 ),在该化合物中,配体的空间构型为;
),在该化合物中,配体的空间构型为; 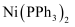 晶体中存在的化学键类型有(填字母)。
晶体中存在的化学键类型有(填字母)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
-
(3) 鉴定
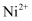 的特征反应如下:
的特征反应如下:
Ni2++2
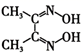 →
→ 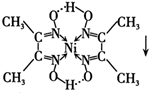 (鲜红色)+2H+
(鲜红色)+2H+在1mol鲜红色沉淀中,含有
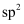 杂化原子的数目为。(
杂化原子的数目为。(  为阿伏加德罗常数的值,下同)
为阿伏加德罗常数的值,下同) -
(4) 红砷镍矿是一种六方晶体(底面为60°和120°的菱形),其晶胞如图所示,图中深色小球为Ni,浅色大球为As。
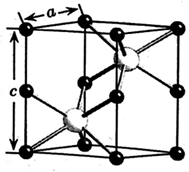
①晶体中As的配位数是,Ni周围距离最近且等距的As有个。
②已知NiAs的晶胞棱长分别为
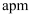 和
和 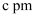 ,则红砷镍矿晶体的理论密度为
,则红砷镍矿晶体的理论密度为 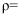
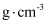 。(写出计算式)
。(写出计算式)
四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p3;④1s22s22p5。则下列有关比较中正确的是( )
A . 原子半径:④>③>②>①
B . 第一电离能:④>③>②>①
C . 电负性:④>③>②>①
D . 最高正化合价:④>③=②>①
下列化学用语使用正确的是( )
A . 甲醛的电子式 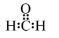 B . 硫原子的价电子排布式 3s23p4
C . 中子数为18的氯原子
B . 硫原子的价电子排布式 3s23p4
C . 中子数为18的氯原子 D . 明矾的化学式 Al2(SO4)3
D . 明矾的化学式 Al2(SO4)3
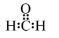 B . 硫原子的价电子排布式 3s23p4
C . 中子数为18的氯原子
B . 硫原子的价电子排布式 3s23p4
C . 中子数为18的氯原子 D . 明矾的化学式 Al2(SO4)3
D . 明矾的化学式 Al2(SO4)3
下列关于原子核外电子排布与元素在周期表中位置关系的表述错误的是( )
A . 基态原子的p能级上半充满的元素一定位于p区
B . 基态原子的p能级上有5个电子的元素一定是第VIIA族元素
C . 原子的价电子排布式为ns2np1~6的元素一定是主族元素
D . 基态原子的N层上只有一个电子的元素,不一定是第IA族元素
我国科学家研究发现,在KOH催化下,CO(NH2)2和LiTPSI还原形成稳定的LiF/高分子双层SEI,使LiMn2O4//Li4T15O12电池稳定工作。请回答下列问题:
-
(1) 基态Mn2+的电子排布式为[Ar]。基态K原子核外电子云轮廓图呈球形的能级上占据的电子总数为。
-
(2) Mn的第三电离能大于Fe的第三电离能的主要原因是。
-
(3) CO(NH2)2中元素电负性由大到小的顺序为(用元素符号表示)。CO(NH2)2分子中碳原子的杂化方式为。
-
(4) 几种钛的卤化物的熔点如表所示:
卤化物
TiF4
TiCl4
TiBr4
TiI4
熔点/℃
377
-25
39
150
钛的卤化物熔点呈上述变化的主要原因是。
-
(5) 一种钛的氧化物晶胞如图1所示,其化学式为。
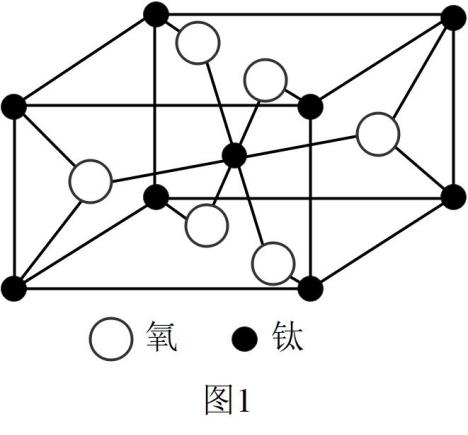
-
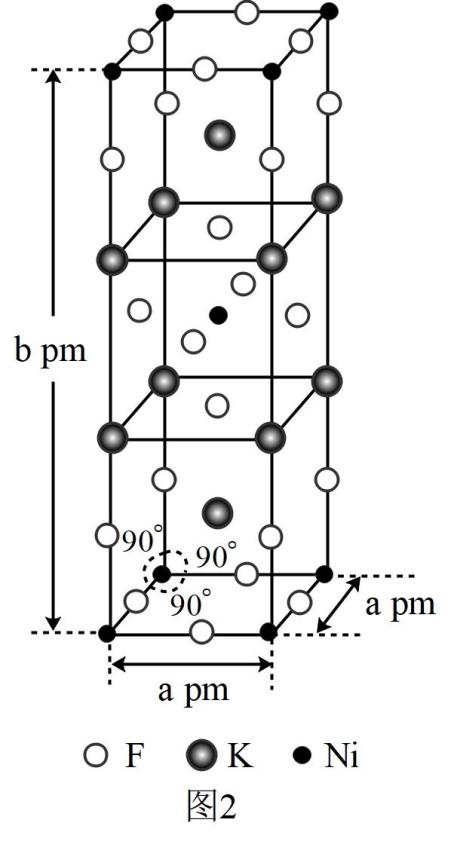
(6) 由钾、镍、氟组成的一种晶体结构如图2所示,该晶体密度为g·cm-3(只列计算式即可)。
铝、锌、铁在人类生产和生活中有重要作用,也是人体必需的微量元素。回答下列问题:
-
(1) 基态
 的价电子排布图为。
的价电子排布图为。
-
(2) 已知Al的第一电离能为
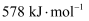 、Mg的第一电离能为
、Mg的第一电离能为 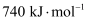 ,请解释Mg的第一电离能比Al大的原因。
,请解释Mg的第一电离能比Al大的原因。
-
(3)
 可形成
可形成  络合物,其阴离子中心原子的杂化方式是,1mol
络合物,其阴离子中心原子的杂化方式是,1mol  配离子中含
配离子中含 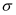 键mol,
键mol,  的沸点高于
的沸点高于  的原因是。
的原因是。
-
(4) S和Fe形成的某化合物,其晶胞如图所示,则该物质的化学式为。假设该晶胞的密度为
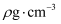 ,用
,用  表示阿伏加德罗常数的值。则该晶胞中距离最近的S原子之间的中心距为(列出计算式即可)cm。
表示阿伏加德罗常数的值。则该晶胞中距离最近的S原子之间的中心距为(列出计算式即可)cm。 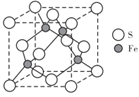
以下有关元素性质的说法正确的是( )
A . 具有下列电子排布式的原子中,① ;②
;② ;③
;③ ;④
;④ , 原子半径最大的是④
B . 具有下列价电子排布式的原子中,①
, 原子半径最大的是④
B . 具有下列价电子排布式的原子中,① ;②
;② ;③
;③ , 第一电离能最大的是①
C . ①Na、K、Rb;②N、P、As;③O、S、Se;④Na、P、Cl,元素的电负性随原子序数增大而递增的是④
D . 元素X气态基态原子的逐级电离能(kJ∙mol-1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是
, 第一电离能最大的是①
C . ①Na、K、Rb;②N、P、As;③O、S、Se;④Na、P、Cl,元素的电负性随原子序数增大而递增的是④
D . 元素X气态基态原子的逐级电离能(kJ∙mol-1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是
 ;②
;② ;③
;③ ;④
;④ , 原子半径最大的是④
B . 具有下列价电子排布式的原子中,①
, 原子半径最大的是④
B . 具有下列价电子排布式的原子中,① ;②
;② ;③
;③ , 第一电离能最大的是①
C . ①Na、K、Rb;②N、P、As;③O、S、Se;④Na、P、Cl,元素的电负性随原子序数增大而递增的是④
D . 元素X气态基态原子的逐级电离能(kJ∙mol-1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是
, 第一电离能最大的是①
C . ①Na、K、Rb;②N、P、As;③O、S、Se;④Na、P、Cl,元素的电负性随原子序数增大而递增的是④
D . 元素X气态基态原子的逐级电离能(kJ∙mol-1)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是
下列说法或化学用语表达正确的是( )
A .  比
比 稳定是因为N-H的键能比P-H的大
B . 基态
稳定是因为N-H的键能比P-H的大
B . 基态 的价层电子排布式为
的价层电子排布式为 C .
C . 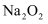 和
和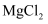 所含化学键类型完全相同
D . 基态N原子的每个能层上电子的能量均不同
所含化学键类型完全相同
D . 基态N原子的每个能层上电子的能量均不同
 比
比 稳定是因为N-H的键能比P-H的大
B . 基态
稳定是因为N-H的键能比P-H的大
B . 基态 的价层电子排布式为
的价层电子排布式为 C .
C . 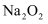 和
和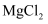 所含化学键类型完全相同
D . 基态N原子的每个能层上电子的能量均不同
所含化学键类型完全相同
D . 基态N原子的每个能层上电子的能量均不同
最近更新
- 下列注音全都正确的一项是( ) A.赡(shàn)养 桎梏(kù) 斡(wò)旋 含情脉脉(
- 根据泉州市委、市政府实施“五大战役”的工作部署,全市社会事业民生战役计划投资 3 653 000 000元,将3 653
- —Are those ______shoes ? — No,they’re not ______
- 根据下面材料,在你了解了人物的心事后,请你以同学的身份,写一句有分寸的宽慰、鼓励对方的短信。(4分) 晓敏时常表现得与
- What he regrets is that more than a chance .A.were
- 16.有一个学习小组在探究某种淀粉酶的最适温度时,设计了如下实验步骤: 1 取10支试管分成5组,编号,向每组的1支试管
- 关于城市化的错误叙述是 A.城市化过程是农村人口向城市集聚 B.城市化是社会经济发展的必然结果 C.城市化水平体现
- 下列关于力的说法中,正确的是( )A.只有直接接触的物体之间才可能有力的作用B.力可以脱离物体而单独存在C.只施力
- 函数的值域是( ) A. B. C. D.
- (二)文言文阅读(15分) 阅读下面的文言文,完成2—5题。 先生金姓,采名,若采字,吴县诸生也。为人倜傥
- Everyone had a form in his hand, but no one knew which offic
- 下列关于反射弧和兴奋传导的叙述,不正确的是() A.神经受刺激的部位膜外先变为正电位,接着又恢复负电位,形成电信号在神经
- 黄宗羲认为:“秦变封建而为郡县,以郡县得私于我也;汉建庶孽(指诸侯王国),以其可以藩屏于我也;宋解方镇之兵,以方镇之不利
- During the ten-day vacation, they traveled to France their o
- 石灰石是我省的主要矿产之一.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸2
- 下列是扬州瘦西湖风景区的几幅图片,关于图片的说法正确的是A.雾是液化现象,吸热B.霜是凝华现象,放热C.雪是凝华现象,吸
- 甲、乙、丙三辆赛车同时从起点出发,做匀速直线运动,最先到达终点的是丙车.甲、乙两车的路程和时间的s—t图像如图所示,下列
- 某芳香烃A有如下转化关系: 按要求填空:(1)写出反应②和⑤的反应条件:②___________________;⑤__
- 演示自感现象的实验电路如图所示,L是电感线圈,A1、A2是规格相同的灯泡,R的阻值与L的直流电阻值相同.当开关S由断开到
- 西周统治末期,所面临的矛盾有( ) ①阶级矛盾 ②民族盾 ③统治



