含氮物质的综合应用 知识点题库
(2)在军事术语上把核潜艇在海里的连续航行叫长行.为了保证长时间潜行,在潜艇里要配备氧气的化学再生装置.制氧气方法有以下几种:①加热高锰酸钾 ②电解水 ③在常温下使过氧化钠(Na2O2)与二氧化碳反应生成碳酸钠和氧气 ④加热氧化汞.其中最适宜在潜艇里制氧气的方法是(填标号) ,反应的化学方程式为 2Na2O2+2H2O=4NaOH+O2↑ 与其他几种方法相比该方法具有的优点是(至少写两点):① ;②
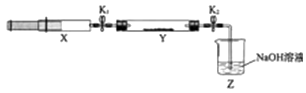
操作步骤 | 实验现象 | 解释原因 |
打开K1 , 推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中 | ②反应的化学方程式 |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
打开K2 | ③ | ④ |
-
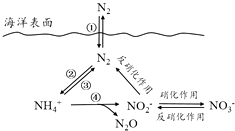
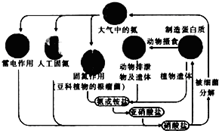
(1) 海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是(填图中数字序号).
-
(2) 下列关于海洋氮循环的说法正确的是(填字母序号).
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO3﹣的废水会影响海洋中NH4+的含量
-
(3) 有氧时,在硝化细菌作用下,NH4+可实现过程④的转化,将过程④的离子方程式补充完整:
NH4++5O2═2NO2﹣+H+++
-
(4) 有人研究了温度对海洋硝化细菌去除氨氮效果的影响,下表为对10L人工海水样本的监测数据:
温度/℃
样本氨氮含量/mg
处理24h
处理48h
氨氮含量/mg
氨氮含量/mg
20
1008
838
788
25
1008
757
468
30
1008
798
600
40
1008
977
910
硝化细菌去除氨氮的最佳反应温度是,在最佳反应温度时,48h内去除氨氮反应的平均速率是 mg•L﹣1•h﹣1 .
-
(5) 为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放.图是间接氧化工业废水中氨氮(NH4+)的示意图.
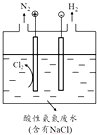
①结合电极反应式简述间接氧化法去除氨氮的原理:.
②若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将(填“增大”、“不变”或“减小”),请简述理由:.
-
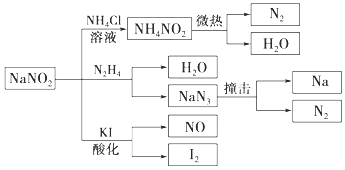
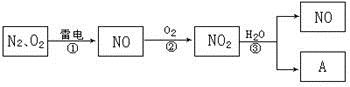
(1) 通常状况下,NO2的颜色是;
-
(2) 反应①的化学方程式是;
-
(3) NO2易溶于水,并和水发生化学反应。该反应中,氧化剂是;
-
(4) 化合物A的化学式是;
-
(5) 治理汽车尾气的一种方法是用催化剂使NO与CO发生反应:
2NO + 2CO = 2CO2 + N2。当生成2mol N2时,被还原的NO为mol。
| A | B | C | D | |
| 物质 | 硅(Si) | 生石灰(CaO) | 液氨(NH3) | 亚硝酸钠(NaNO2) |
| | | | | |
| 用途 | 半导体材料 | 抗氧化剂 | 制冷剂 | 食品防腐剂 |
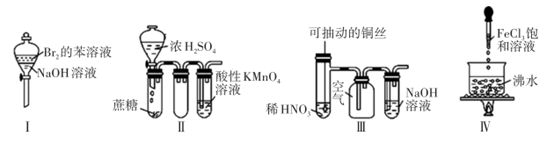
①实验 I :振荡后静置,上层溶液颜色变浅
②实验 II :酸性 KMnO4溶液中出现气泡,溶液的颜色无变化
③实验III:微热稀HNO3片刻,溶液中有气泡产生 ,广口瓶内始终保持无色
④实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应
 )采用微生物脱氮法、化学沉淀法均可除去,具体原理如下:
)采用微生物脱氮法、化学沉淀法均可除去,具体原理如下: ①微生物脱氮法: 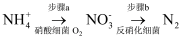
②化学沉淀法:向废水中加入含MgCl2、Na3PO4的溶液,生成  沉淀从而去除氨氮。
沉淀从而去除氨氮。
下列有关说法正确的是( )
 D . 化学沉淀法脱氮时,氨氮的去除率随着溶液碱性的增强而上升
D . 化学沉淀法脱氮时,氨氮的去除率随着溶液碱性的增强而上升
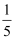 计算),夹住弹簧夹,让内外大气压相同,观察。下列叙述不正确的是( )
计算),夹住弹簧夹,让内外大气压相同,观察。下列叙述不正确的是( ) ![]()
-
(1) 氮在元素周期表的位置为,其非金属性比磷(填“强”或“弱”)。氮气的化学性质很稳定,原因是。
-
(2) 1909年,德国科学家哈伯利用氮气和氢气在500~600℃、18.5~20.0
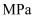 和锇为催化剂的条件下合成氨气。下列关于工业上合成氨的说法合理的是____。
A . 合成氨属于人工固氮 B . 合成原料氢气主要通过电解水获得 C . 将生成的氨气分离,可加快反应速率 D . 通过改良催化剂,可使反应更易发生
和锇为催化剂的条件下合成氨气。下列关于工业上合成氨的说法合理的是____。
A . 合成氨属于人工固氮 B . 合成原料氢气主要通过电解水获得 C . 将生成的氨气分离,可加快反应速率 D . 通过改良催化剂,可使反应更易发生 -
(3) 某兴趣小组在实验室中探究氮的氧化物的性质。
①利用铜和稀硝酸制取NO,化学方程式为,该反应中还原剂与氧化剂物质的量之比为。
②探究氮的氧化物性质的实验步骤及预期现象如下表:
步骤
预期现象
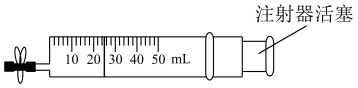
i.在一支注射器中吸入22.4mLNO(标准状况下),然后吸入5mL水,用乳胶管和弹簧夹封住管口,振荡注射器
无明显现象
ii.打开弹簧夹,快速吸入10mL空气后夹上弹簧夹,固定住注射署活塞
iii.松开注射器活塞,再振荡注射器
重复操作ii和iii,充分反应后,注射器中的溶液浓度为mol/L(假设反应前后液的体积几乎不变)。
-
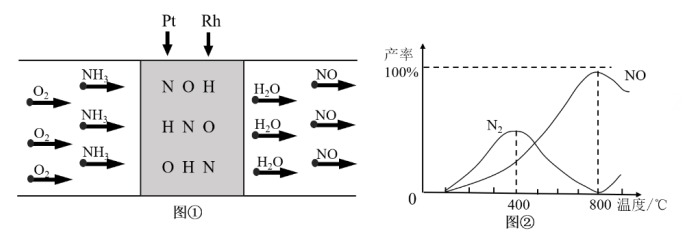
(4) 利用
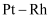 合金催化氧化
合金催化氧化 制取
制取 , 图①是反应的微观模型,含氮生成物产率反应温度的变化曲线如图②所示。下列说法正确的是____。
, 图①是反应的微观模型,含氮生成物产率反应温度的变化曲线如图②所示。下列说法正确的是____。
 A . 可用湿润的蓝色石蕊试纸检验
A . 可用湿润的蓝色石蕊试纸检验 是否反应完全
B . 400℃时,生成的产物只有
是否反应完全
B . 400℃时,生成的产物只有 、
、 C . 800℃以上,可能发生反应:
C . 800℃以上,可能发生反应: D .
D . 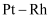 合金催化氧化
合金催化氧化 制取
制取 , 适宜的温度为800℃
, 适宜的温度为800℃
已知:碎玻璃中的各成分均不与HNO3发生反应。
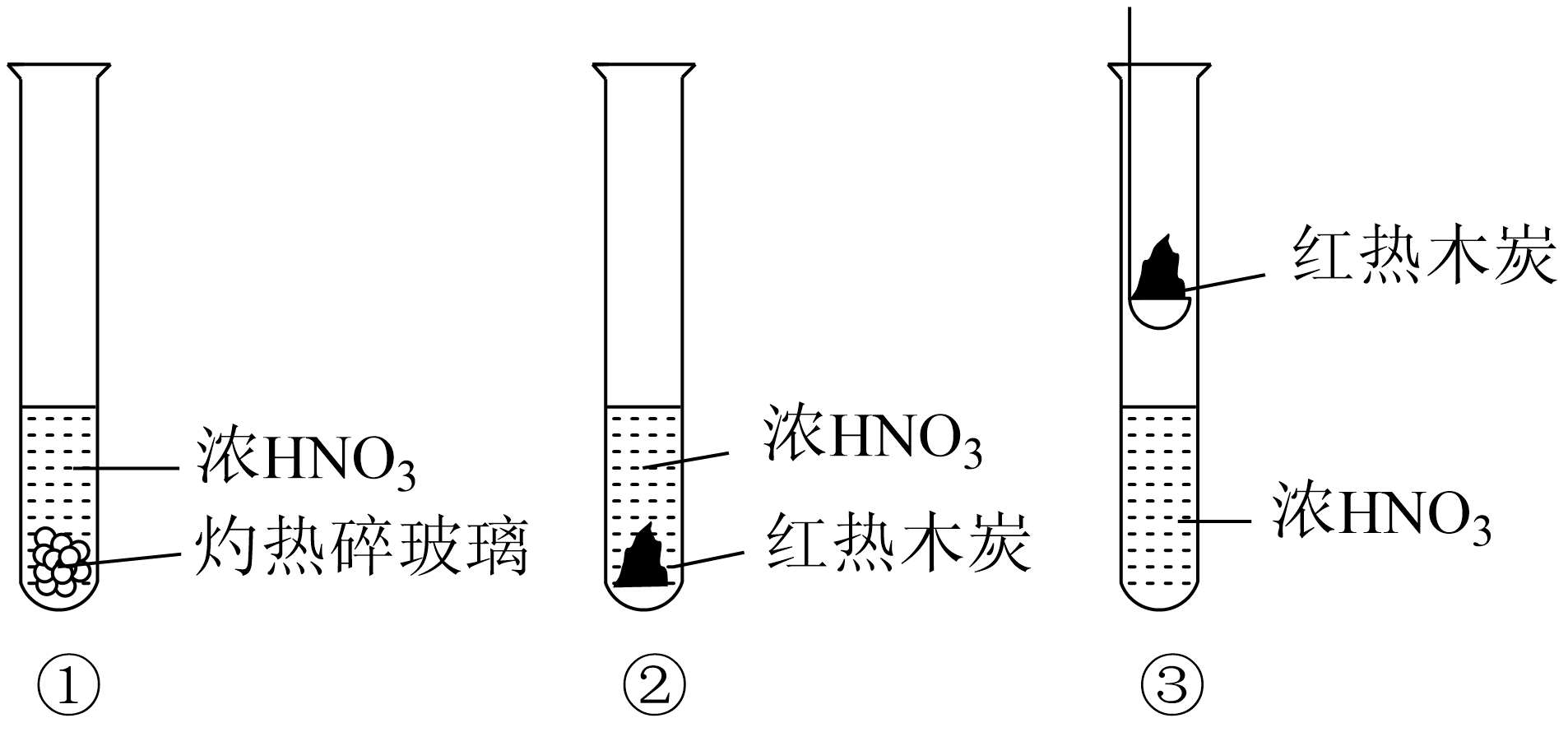
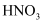 反应时的主要还原产物如图所示。下列说法正确的是( )
反应时的主要还原产物如图所示。下列说法正确的是( )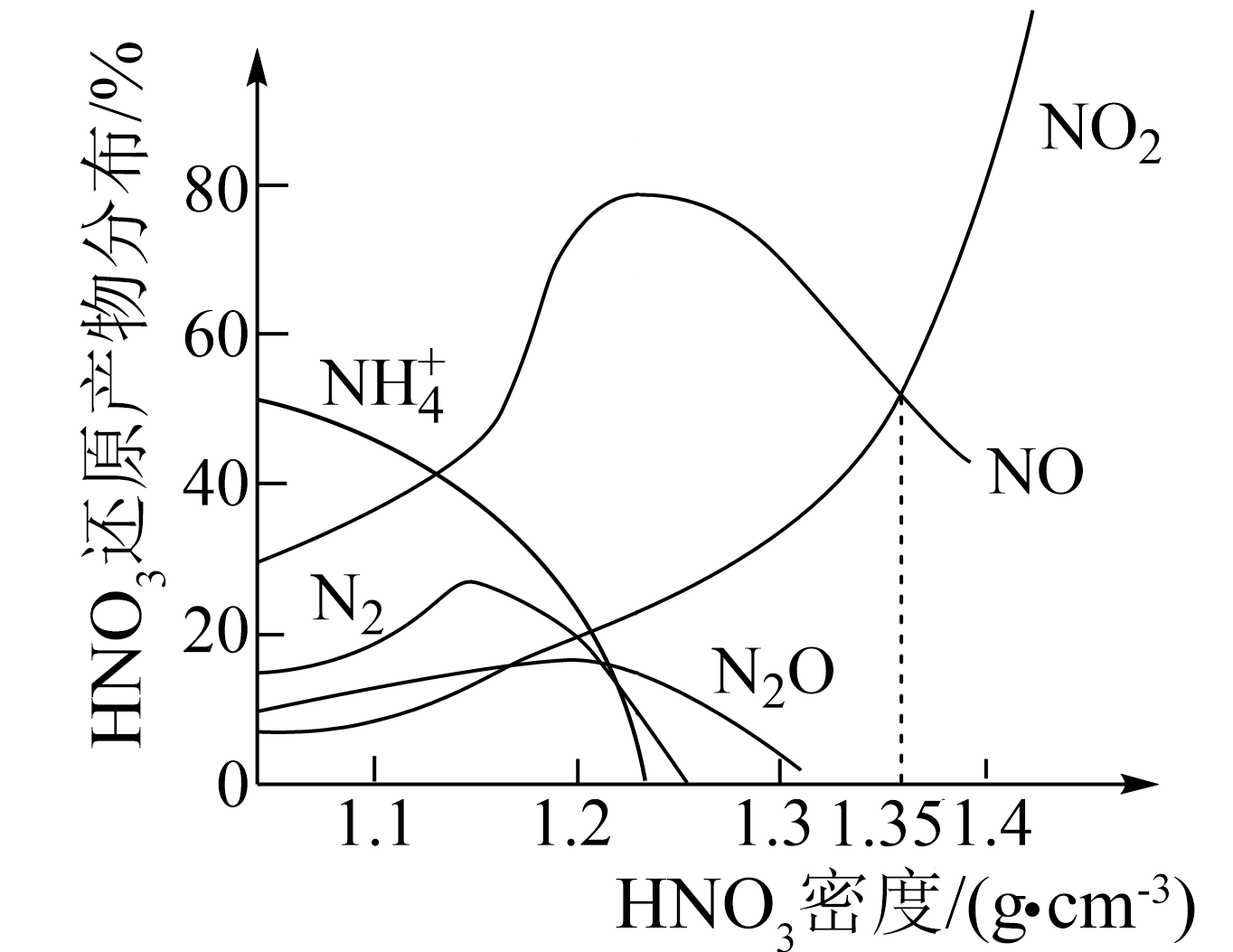
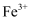 B . 浓硝酸为
B . 浓硝酸为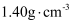 时,反应的主要还原产物为
时,反应的主要还原产物为 C . 浓硝酸为
C . 浓硝酸为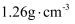 时,反应生成
时,反应生成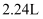 (标准状况下)气体,则参加反应的
(标准状况下)气体,则参加反应的 D . 铁与过量浓硝酸
D . 铁与过量浓硝酸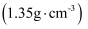 反应可表示为:
反应可表示为:
 的速率先快后慢,速率加快的主要因素是温度升高
B . 取
的速率先快后慢,速率加快的主要因素是温度升高
B . 取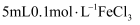 溶液,向其中滴加
溶液,向其中滴加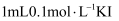 溶液,取上层清液滴加KSCN溶液,溶液变成血红色,该反应是可逆反应
C . 将红热的铂丝插入到盛有氨气和氧气的集气瓶,铂丝一直保持红热,集气瓶出现红棕色气体,氨气与氧气反应放热,无一氧化氮生成
D . 分别向蛋白质溶液中加入饱和
溶液,取上层清液滴加KSCN溶液,溶液变成血红色,该反应是可逆反应
C . 将红热的铂丝插入到盛有氨气和氧气的集气瓶,铂丝一直保持红热,集气瓶出现红棕色气体,氨气与氧气反应放热,无一氧化氮生成
D . 分别向蛋白质溶液中加入饱和 和
和 溶液,均析出固体,蛋白质都发生变性
溶液,均析出固体,蛋白质都发生变性
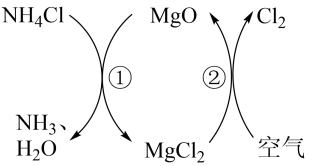
 可循环使用
B . 反应①实现了氮的固定
C . 高温下发生反应②的化学方程式为
可循环使用
B . 反应①实现了氮的固定
C . 高温下发生反应②的化学方程式为 D . 图示转化可实现用
D . 图示转化可实现用 获得
获得 和
和
- Weare in great need of a more capable monitor , ______ with
- 如下图所示:甲图中①②表示目镜,③④表示物镜,⑤⑥表示物镜与载玻片之间的距离,乙和丙分别表示不同物镜下观察到的图像。下面
- 如图甲所示,电源电压恒为9V,滑动变阻器的最大阻值为100Ω,电流在0.1﹣0.4A之间时电子元件均能正常工作.若通过此
- 五四运动爆发的导火线是 A、巴黎和会的召开B、巴黎和会上列强拒绝中国的正义要求,中国外交失败 C、中国人民与帝国主义、封
- 已知△ABC中,2(∠B+∠C)=3∠A,则∠A的度数是( ) A.54° B.72° C.108°
- 43.果蝇白眼为伴X隐性遗传,显性性状为红眼.在下列哪组杂交后代中,通过眼色就可直接判断子代果蝇的性别( ) A.白
- When I finally got up to leave, we both knew that a real fri
- 两个电热丝R1、R2,其电阻关系为R1∶R2=2∶3,若将它们串联在电路中,它们两端的电压之比U1∶U2=_____,在
- 在不使用酸碱指示剂的前提下,欲除去氯化钙溶液中的少量盐酸,得到纯的氯化钙溶液,最适宜选用的一种试剂是A.硝酸银溶液
- 下列物质中,既能与强酸反应,又能与强碱反应的是 ①NaHCO3 ②Al ③Al2O3 ④Al(OH)3
- (7分)水泥的成分中含有碳酸盐,张南同学为了验证水泥中的碳酸盐,设计了下列方案,请帮助他完成实验方案:(1)验证水泥中含
- 等浓度的下列溶液中,NH4+浓度最大的是( ) A.(NH4)2SO4 B.NH4Cl C.(NH4)2CO
- “旧时王榭堂前燕,飞入寻常百姓家。”常被用来形容过去的一些昂贵商品现在变成了大众消费品,造成这种变化的主要原因是(
- 有些化学反应反应速率很慢且副反应较多,测定这些反应的焓变可运用 A.盖斯定律 B.勒夏特列原理 C
- “Up until about five years ago, students at this school coul
- 华兰生物工程股份有限公司成立于1992年,是从事血液制品研发和生产的国家级重点高新技术企业。从所有制性质上看,华兰生物属
- 根据以下3个热化学方程式: 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=﹣Q1 kJ/mol 2H
- 在半径为1的⊙O中,弦AB、AC分别是、,则∠BAC的度数为 _____ .
- 已知曲线y=,则曲线的切线斜率取得最小值时的直线方程为( ) A.x+4y-2=0 B.x-4y+2=0 C.
- 下列每组加点字读音不同的是: A.诘难 奉命于危难之间 B.狭隘 挟天子而令诸侯 C.载歌载







